
- •Міністерство освіти і науки України
- •Передмова
- •Робоча програма
- •Приклади виконання завдань
- •Контрольні завдання
- •Основні класи неорганічних сполук основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Термохімія та термохімічні розрахунки основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Ентропія, енергія гіббса та напрямленість процесів основні поняття та визначення
- •Приклади виконання завдань
- •Визначити можливість перебігу реакції
- •Визначити, за якої температури настане рівновага в системі
- •Контрольні завдання
- •Хімічна кінетика основні поняття та визначення
- •Приклади виконання завдань
- •Визначити швидкість реакції
- •Контрольні завдання
- •Хімічна рівновага основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •II модуль розчини. Концентрації розчинів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Властивості розчинів неелектролітів. Основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електролітична дисоціація ступінь та константа дисоціації основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Іонний добуток води. Водневий показник основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Іонна рівновага в гетерогенних системах добуток розчинності основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Реакції в розчинах електролітів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Гідроліз солей основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Колоїдні розчини основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Будова атома основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •III модуль окисно-відновні реакції основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Гальванічні елементи основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Корозія металів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Электроліз розплавів і водних розчинів електролітів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Твердість води основні поняття та визначення
- •Приклади виконання завдань
- •Приклад 2. Визначення маси солі, розчиненої в певному об’ємі води, за величиною твердості води.
- •Контрольні завдання
- •Карбонатна рівновага. Форми існування со2 у воді. Основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Список рекомендованої літератури Основна література
- •Додаткова література
- •Додаток абудова речовини а1.Будова атома
- •А2.Періодична система елементів д. І.Менделєєва та електронна теорія будови атомів
- •Головна підгрупа Побічна група
- •Двох періодів.
- •Відносні електронегативності елементів(за шкалою Полінга)
- •А3. Хімічний зв’язок і будова молекул
- •2 Відштовхування rзв.Е, кДж/моль
- •Елементів д.І.Менделєєва
- •Навчальне видання
Приклади виконання завдань
Приклад 1. Скільки солей можна одержати при взаємодії натрій гідроксиду NaOH з фосфатною кислотою?
Відповідь. Якщо взяти реагуючі речовини в еквівалентних кількостях, одержимо середню або нормальну сіль натрій фосфат Na3PO4
![]()
а якщо взяти надлишок кислоти, то одержимо кислі солі, які є продуктом неповного заміщення атомів Гідрогену в молекулі кислоти на метал

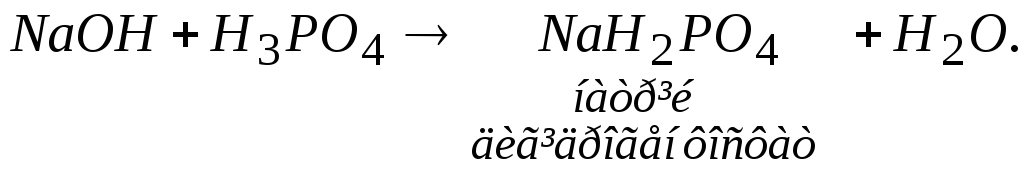
Відповідь: 3 солі.
Приклад 2. Скільки солей можна одержати при взаємодії ферум(III)гідроксиду з хлоридною кислотою?
Відповідь. Якщо взяти реагуючі речовини в еквівалентних кількостях, одержимо середню сіль ферум(III) хлорид:
![]() ,
,
а якщо взяти надлишок Fe(OH)3, одержимо основні солі, які є продуктом неповного заміщення гідроксидних груп ОН- на кислотний залишок. Саме тому в їхніх молекулах крім атомів металу і кислотних залишків містяться одна або дві групи ОН-:
![]()
![]()
Відповідь: 3 солі.
Контрольні завдання
61. Скільки солей можна одержати при взаємодії кальцій гідроксиду з сульфатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 3 солі.
62. Скільки солей можна одержати при взаємодії магній гідроксиду з фосфатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 4 солі.
63. Скільки солей можна одержати при взаємодії купрум(II) гідроксиду з фосфатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 4 солі.
64. Скільки солей можна одержати при взаємодії цинк гідроксиду з карбонатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 3 солі.
65. Скільки солей можна одержати при взаємодії ферум(II) гідроксиду з силікатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 3 солі.
66. Скільки солей можна одержати при взаємодії алюміній гідроксиду з хлоридною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 3 солі.
67. Скільки солей можна одержати при взаємодії алюміній гідроксиду з сульфатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 4 солі.
68. Скільки солей можна одержати при взаємодії алюміній гідроксиду з бромідною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 3 солі.
69. Скільки солей можна одержати при взаємодії алюміній гідроксиду з фосфатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 5 солей.
70. Скільки солей можна одержати при взаємодії барій гідроксиду з нітритною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 2 солі.
71. Скільки солей можна одержати при взаємодії барій гідроксиду з силікатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 3 солі.
72. Скільки солей можна одержати при взаємодії барій гідроксиду з сульфідною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 3 солі.
73. Скільки солей можна одержати при взаємодії барій гідроксиду з фосфатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 4 солі.
74. Скільки солей можна одержати при взаємодії хром(Ш) гідроксиду з іодидною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 3 солі.
75. Скільки солей можна одержати при взаємодії хром(Ш) гідроксиду з сульфатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 4 солі.
76. Скільки солей можна одержати при взаємодії хром(Ш) гідроксиду з сульфітною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 4 солі.
77. Скільки солей можна одержати при взаємодії хром(Ш) гідроксиду з фосфатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 5 солей.
78. Скільки солей можна одержати при взаємодії ферум(Ш) гідроксиду з сульфатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 4 солі.
79. Скільки солей можна одержати при взаємодії ферум(П) гідроксиду з фосфатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 4 солі.
80. Скільки солей можна одержати при взаємодії ферум(Ш) гідроксиду з карбонатною кислотою? Скласти рівняння реакцій утворення відповідних солей.
Відповідь: 4 солі.
