
- •Міністерство освіти і науки України
- •Передмова
- •Робоча програма
- •Приклади виконання завдань
- •Контрольні завдання
- •Основні класи неорганічних сполук основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Термохімія та термохімічні розрахунки основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Ентропія, енергія гіббса та напрямленість процесів основні поняття та визначення
- •Приклади виконання завдань
- •Визначити можливість перебігу реакції
- •Визначити, за якої температури настане рівновага в системі
- •Контрольні завдання
- •Хімічна кінетика основні поняття та визначення
- •Приклади виконання завдань
- •Визначити швидкість реакції
- •Контрольні завдання
- •Хімічна рівновага основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •II модуль розчини. Концентрації розчинів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Властивості розчинів неелектролітів. Основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електролітична дисоціація ступінь та константа дисоціації основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Іонний добуток води. Водневий показник основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Іонна рівновага в гетерогенних системах добуток розчинності основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Реакції в розчинах електролітів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Гідроліз солей основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Колоїдні розчини основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Будова атома основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •III модуль окисно-відновні реакції основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Гальванічні елементи основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Корозія металів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Электроліз розплавів і водних розчинів електролітів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Твердість води основні поняття та визначення
- •Приклади виконання завдань
- •Приклад 2. Визначення маси солі, розчиненої в певному об’ємі води, за величиною твердості води.
- •Контрольні завдання
- •Карбонатна рівновага. Форми існування со2 у воді. Основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Список рекомендованої літератури Основна література
- •Додаткова література
- •Додаток абудова речовини а1.Будова атома
- •А2.Періодична система елементів д. І.Менделєєва та електронна теорія будови атомів
- •Головна підгрупа Побічна група
- •Двох періодів.
- •Відносні електронегативності елементів(за шкалою Полінга)
- •А3. Хімічний зв’язок і будова молекул
- •2 Відштовхування rзв.Е, кДж/моль
- •Елементів д.І.Менделєєва
- •Навчальне видання
Визначити, за якої температури настане рівновага в системі
![]()
За якої температури рівновага системи зміститься вправо?
Розв’язання.
Термодинамічною
умовою рівноваги є рівність
![]() .
Знаходимо температуру, за якої встановиться
рівновага в системі, із співвідношення
.
Знаходимо температуру, за якої встановиться
рівновага в системі, із співвідношення
![]()
Оскільки
умовою рівноваги є
![]() ,
то і
,
то і![]() .
Тоді
.
Тоді![]() і
і![]() .
.
Починаючи
з цієї температури можливий самочинний
перебіг реакції. Використовуючи перший
наслідок із закону Гесса, знаходимо
![]() і
і![]() за рівняннями
за рівняннями![]() і
і![]() ,
підставивши взяті з таблиць теплоти
утворення і ентропії компонентів
реакції:
,
підставивши взяті з таблиць теплоти
утворення і ентропії компонентів
реакції:
![]()
![]()
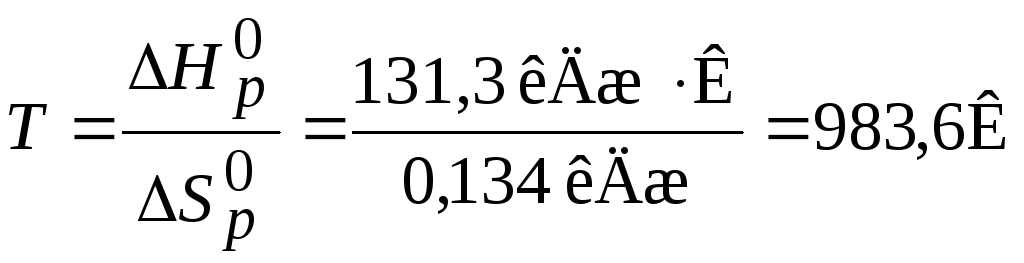 .
.
Отже, при Т=983,6 К - в системі встановиться рівновага, тобто однаково ймовірні прямий та зворотний напрямки реакцій. При температурах, що перевищують 983,6 К, рівновага зміщуватиметься вправо, тобто відбуватиметься пряма реакція, а при температурах нижче 983,6 К рівновага зміститься вліво, відбуватиметься зворотна реакція.
Контрольні завдання
Не виконуючи розрахунків, встановити знак ΔS наступних процесів:
141.
![]()
142.
![]()
143.
![]()
144.
![]()
145.
![]()
146.
![]()
147.
![]()
148.
![]()
149.
![]()
150.
![]()
151.
![]()
152.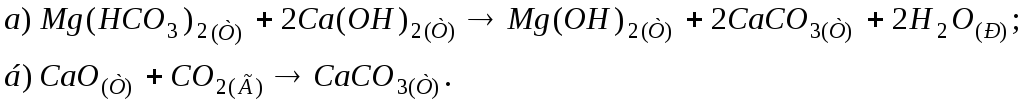
153.
![]()
154.
![]()
155.
![]()
156.
![]()
157.
![]()
158.
![]()
159.
![]()
160.
![]()
161. Зробити висновок про можливість самочинного перебігу реакції за стандартних умов
![]() .
.
Відповідь
обґрунтувати розрахунком
![]() реакції.
реакції.
Відповідь: – 959,5 кДж.
162.
За якої температури настане рівновага
в системі
![]()
Відповідь: 325 К.
163.
Визначити
![]() утворення натрій алюмінату
утворення натрій алюмінату![]() на підставі
на підставі![]() реакції:
реакції:
![]()
Відповідь: –1076,0 кДж/моль.
164.
При якій температурі настане рівновага
в системі
![]()
Відповідь: 385,5 К.
165. Визначити зміну стандартної енергії Гіббса реакції окиснення етилового спирту
![]() .
.
Зробити висновок про можливість самочинного перебігу реакції за стандартних умов.
Відповідь: –1326,5 кДж.
166. При якій температурі однаково ймовірні прямий та зворотний напрямки реакції
![]()
Відповідь: 882,3 К.
167.
Визначити
![]() утворенняС2Н4(Г),
виходячи з рівняння реакції окиснення
його:
утворенняС2Н4(Г),
виходячи з рівняння реакції окиснення
його:
![]()
Відповідь: 68,12 кДж/моль.
168. За якої температури настає рівновага в системі
![]() кДж?
кДж?
Відповідь: 884,5 К.
169. В якому напрямку відбувається оборотна реакція
![]()
за
стандартних умов? Відповідь обґрунтувати
розрахунком
![]() реакції.
реакції.
Відповідь: 130,22 кДж.
170. За якої температури настане рівновага в системі
![]() кДж?
кДж?
Відповідь: 389,2 К.
171.
Визначити
![]() утворенняСО(Г)
на підставі рівняння реакції відновлення
алюмінію з його оксиду за допомогою СО
утворенняСО(Г)
на підставі рівняння реакції відновлення
алюмінію з його оксиду за допомогою СО
![]()
Відповідь: –137,27 кДж/моль.
172. Реакція відновлення FeO відбувається за рівнянням
![]()
При якій температурі почнеться відновлення FeO.?
Відповідь: понад 867,9 К.
173. Визначити
![]() утворення сірководню, виходячи з рівняння
реакції:
утворення сірководню, виходячи з рівняння
реакції:
![]()
Відповідь: –33,02 кДж/моль.
174. При якій температурі настане рівновага в системі
![]()
Відповідь: 466,8 К.
175. Зробити висновок про можливість самочинного перебігу реакції відновлення Fe3O4 воднем:
![]()
Відповідь обґрунтувати
розрахунком
![]() реакції.
реакції.
Відповідь: 99,6 кДж.
176. Визначити, при якій температурі можливий перебіг реакції
![]()
Відповідь: 6445,1К.
177. Виходячи з рівняння реакції
![]()
визначити
![]() утворенняFe3O4(К).
утворенняFe3O4(К).
Відповідь: –1014,8 кДж/моль.
178. При якій температурі однаково ймовірні прямий та зворотний напрямки реакції
![]()
Відповідь: 965,5 К.
179. В якому напрямку проходить оборотна реакція згоряння хлороводню
![]()
за стандартних умов?
Відповідь обґрунтувати розрахунком
![]() реакції.
реакції.
Відповідь: -79,6 кДж.
180. При якій температурі стає термодинамічно можливою реакція відновлення титан(IV) оксиду до вільного металу за рівнянням:
![]()
Відповідь: 1987,6 К.
