
- •Міністерство освіти і науки України
- •Передмова
- •Робоча програма
- •Приклади виконання завдань
- •Контрольні завдання
- •Основні класи неорганічних сполук основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Термохімія та термохімічні розрахунки основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Ентропія, енергія гіббса та напрямленість процесів основні поняття та визначення
- •Приклади виконання завдань
- •Визначити можливість перебігу реакції
- •Визначити, за якої температури настане рівновага в системі
- •Контрольні завдання
- •Хімічна кінетика основні поняття та визначення
- •Приклади виконання завдань
- •Визначити швидкість реакції
- •Контрольні завдання
- •Хімічна рівновага основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •II модуль розчини. Концентрації розчинів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Властивості розчинів неелектролітів. Основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електролітична дисоціація ступінь та константа дисоціації основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Іонний добуток води. Водневий показник основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Іонна рівновага в гетерогенних системах добуток розчинності основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Реакції в розчинах електролітів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Гідроліз солей основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Колоїдні розчини основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Будова атома основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •III модуль окисно-відновні реакції основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Гальванічні елементи основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Корозія металів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Электроліз розплавів і водних розчинів електролітів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Твердість води основні поняття та визначення
- •Приклади виконання завдань
- •Приклад 2. Визначення маси солі, розчиненої в певному об’ємі води, за величиною твердості води.
- •Контрольні завдання
- •Карбонатна рівновага. Форми існування со2 у воді. Основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Список рекомендованої літератури Основна література
- •Додаткова література
- •Додаток абудова речовини а1.Будова атома
- •А2.Періодична система елементів д. І.Менделєєва та електронна теорія будови атомів
- •Головна підгрупа Побічна група
- •Двох періодів.
- •Відносні електронегативності елементів(за шкалою Полінга)
- •А3. Хімічний зв’язок і будова молекул
- •2 Відштовхування rзв.Е, кДж/моль
- •Елементів д.І.Менделєєва
- •Навчальне видання
Ентропія, енергія гіббса та напрямленість процесів основні поняття та визначення
|
Ентропія S |
-
міра невпорядкованості системи,
функція стану системи.
|
|
Вільна енергія Гіббса (ізобарно-ізотермічний потенціал) G
|
- вільна енергія системи при Р,Т = const. G=H-TS або ΔG = ΔH-TΔS. Розмірність кДж. |
|
Стандартна
енергія Гіббса утворення речовини
|
- зміна енергії Гіббса системи при утворенні 1 моль речовини з простих речовин стійких за стандартних умов. Розмірність кДж/моль.
|
|
Зміна вільної енергії Гіббса хімічного процесу |
-
різниця між сумою вільних енергій
продуктів реакції та вихідних речовин
з урахуванням стехіометричних
коефіцієнтів
|
|
Критерії можливості перебігу реакції: |
ΔG < 0 – реакція відбувається в прямому напрямку; ΔG >0 – реакція відбувається у зворотному напрямку; ΔG = 0 – стан хімічної рівноваги. |
Приклади виконання завдань
При виконанні завдань цього розділу див табл. 5.
Приклад 1. Залежність ентропії від агрегатного стану речовин.
Як зміниться ентропія при перетвореннях:
а) води в пару;
б) води в лід;
в)
![]()
Чому?
Відповідь.
а) Перехід Н2О(р) → Н2О(г) супроводжується збільшенням невпорядкованості системи і тому зростанням ентропії S2 > S1.
Оскільки
![]() ,
то Δ S > 0
,
то Δ S > 0
б)
Перехід
![]()
супроводжується збільшенням впорядкованості системи і тому зменшенням ентропії S2 < S1. Оскільки ΔS = S2 – S1, то ΔS < 0.
в)
Перехід
![]() супроводжується збільшенням
невпорядкованості системи, тому що
утворюється газоподібна речовина СО2.
Ентропія системи збільшується, тобто
S2 >
S1 і
ΔS > 0.
супроводжується збільшенням
невпорядкованості системи, тому що
утворюється газоподібна речовина СО2.
Ентропія системи збільшується, тобто
S2 >
S1 і
ΔS > 0.
Приклад 2. Визначення можливості перебігу процесу за величиною зміни вільної енергії Гіббса.
Визначити можливість перебігу реакції
![]()
якщо
відомі
![]() утворення (стандартна вільна енергія
Гіббса або ізобарно-ізотермічний
потенціал) усіх речовин:
утворення (стандартна вільна енергія
Гіббса або ізобарно-ізотермічний
потенціал) усіх речовин:![]() кДж/моль;
кДж/моль;![]() кДж/моль;
кДж/моль;![]() кДж/моль;
кДж/моль;![]() кДж/моль.
Відповідь обґрунтувати розрахунком
кДж/моль.
Відповідь обґрунтувати розрахунком![]() реакції.
реакції.
Розв’язання.
Зміна вільної енергії
Гіббса
![]() реакції розраховується за формулою:
реакції розраховується за формулою:
![]() ,
,
де n і m – кількість молів певної речовини, моль;
![]() і
і
![]() - стандартні вільні енергії Гіббса
утворення продуктів реакції і вихідних
речовин відповідно, кДж/моль.
- стандартні вільні енергії Гіббса
утворення продуктів реакції і вихідних
речовин відповідно, кДж/моль.
Для даної реакції
![]()
![]()
![]()
Оскільки
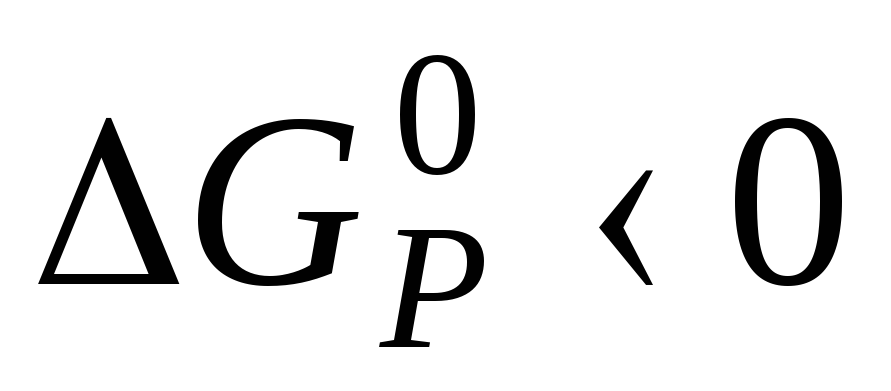 ,
то реакція можлива.
,
то реакція можлива.
Приклад 3. Визначення стандартної енергії Гіббса утворення речовини за відомою величиною зміни енергії Гіббса реакції.
Відновлення заліза з його оксиду за допомогою СО відбувається за рівнянням:
![]()
Розрахувати
![]() утворення карбон(IV)
оксиду, користуючись величинами
утворення карбон(IV)
оксиду, користуючись величинами
![]() утворення необхідних речовин.
утворення необхідних речовин.
Розв’язання.
Зв’язок між
![]() і
і![]() для всіх речовин, що увійшли в рівняння
реакції, визначається за формулою:
для всіх речовин, що увійшли в рівняння
реакції, визначається за формулою:
![]() ,
,
де n і m – числа молів кожної з речовин в рівнянні реакції, моль;
![]() і
і
![]() -
стандартні вільні енергії Гіббса
утворення продуктів реакції і вихідних
речовин відповідно, кДж/моль.
-
стандартні вільні енергії Гіббса
утворення продуктів реакції і вихідних
речовин відповідно, кДж/моль.
Для даної реакції
![]() .
.
Звідси
визначаємо
![]() :
:
![]() .
.
У
табл.4 є значення всіх ізобарно-ізотермічних
потенціалів для даної задачі:
![]() кДж/моль;
кДж/моль;![]() кДж/моль;
кДж/моль;
![]() кДж/моль.
Отже
кДж/моль.
Отже
![]() (кДж/моль).
(кДж/моль).
Приклад 4. Визначення температури встановлення рівноваги в системі за термодинамічними параметрами.
