
- •Печатается согласно редакционно-издательскону плану Военно-медицинской академии имени с. М. Кирова, утвержденному начальником Главного военно-медицинского управления
- •Глава 6. Антидоты. Общие принципы оказания неотложной помощи отравленным
- •Глава 11. Отравляющие и высокотоксичные вещества цитотоксического действия
- •Глава 12. Отравляющие и высокотоксичные вещества нейротоксического действия
- •Часть II. Радиобиология 337
- •Раздел IV. Военная радиобиология 380
- •Глава 17. Факторы, вызывающие поражения личного состава войск при ядерных
- •Глава 18. Лучевые поражения в результате внешнего облучения (н. В. Бутомо) 385
- •ГЛава 19. Лучевые поражения в результате общего (тотального) облучения
- •Глава 20. Медицинская защита от внешнего облучения (а. Н. Гребенюк,
- •Глава 21. Местные лучевые поражения (а. Н. Гребенюк, н. В. Бутомо) 418
- •Глава 22. Поражения в результате внутреннего радиоактивного заражения
- •Глава 23. Сочетанные и комбинированные радиационные поражения
- •Часть III. Средства и методы профилактики химических
- •Глава 24. Технические средства индивидуальной и коллективной защиты
- •Глава 25. Специальная обработка в подразделениях и частях медицинской службы
- •Глава 26. Радиационная и химическая разведка в частях и подразделениях
- •Часть I токсикология
- •Глава 1. Предмет, цель, задачи и структура токсикологии
- •1.1. Предмет токсикологии
- •Часть I. Токсикология
- •1.2L Цель и задачи токсикологии
- •Глава 1. Предмет, цель, задачи и структура токсикологии
- •1.3. Структура токсикологии
- •Часть I. Токсикология
- •Глава 2. Основные понятия токсикологии
- •2.1. Токсикант (яд)
- •2.2. Токсический процесс
- •Глава 3. Токсикометрия
- •Глава 4. Токсикокинетика
- •Признаки специфического транспорта
- •Транспорт веществ путем цитозов
- •1.2. Резорбция
- •Часть I. Токсикология
- •4.4.1. Экскреция
- •4.5» Количественные характеристики токсикокинетики
- •Глава 5. Токсикодинамика
- •5.1. Механизм токсического действия
- •5.1.1. Химизм реакции токсикант — рецептор
- •5.1.2. Взаимодействие токсикантов с белками
- •5.1.3» Взаимодействие токсикантов с нуклеиновыми кислотами
- •5.1.4. Взаимодействие токсикантов с липидами мембран
- •5.1.5. Взаимодействие с реактивными структурами возбудимых мембран
- •5.2. Общие механизмы цитотоксичности
- •5.2.1. Нарушение процессов биоэнергетики
- •5.2.2. Активация свободнорадикальных процессов в клетке
- •Энзиматическая и неэнзиматическая защита клеток ► супероксиддисмутаза ♦ катапаза ♦ gsh-пероксидаза ♦ gssg-редуктаза ♦ аскорбат ♦ глутатион ♦ мочевая кислота ♦ токоферол
- •Манифестация активации свободнорадикальных процессов
- •5.2.3* Повреждение мембранных структур
- •Экзогенные фосфолипазы (змеиные яды)
- •Фосфолипиды (гидролиз)
- •5.2*4. Нарушение гомеостаза внутриклеточного кальция
- •Часть I. Токсикология
- •5.2.5. Повреждение процессов синтеза белка и клеточного деления
- •Возможные точки приложения повреждающего действия токсикантов на процессы синтеза белка и клеточного деления
- •2. Синтез рнк. Транскрипция " .
- •5.3. Развитие токсического процесса
- •Глава 6. Антидоты. Общие принципы оказания неотложной помощи отравленным
- •6.1. Характеристика современных антидотов
- •Глава 6. Антидоты. Общие принци11ы оказании ньШлижпии I шмцщи и I гаш ItnnWm
- •6.2. Применение противоядий
- •6.3. Разработка новых антидотов
- •6.4. Основные принципы оказания первой, доврачебной и первой врачебной помощи при острых отравлениях
- •Раздел II. Военная токсикология
- •Глава 7. Основные понятия военной токсикологии
- •7.1. Предмет, цели, задачи военной токсикологии
- •7.2. Отравляющие и высокотоксичные вещества (овтв)
- •Часть I. Токсикология
- •Глава 7. Основные понятия военной токсикологии
- •7М. Медицинская противохимическая защита
- •Глава 8. Отравляющие
- •8.1. Общая характеристика
- •8.2. Физико-химические свойства. Токсичность
- •8.3. Методы изучения раздражающего действия
- •8.4. Основные проявления поражения
- •Часть I. Токсикология
- •Глава 8. Отравляющие и высокотоксичныь ньщсыок тдцт,»™—- „
- •8.5. Патогенез токсического процесса. Механизм действия
- •Часть I. Токсикология
- •Глава 8. Отравляющие и высоко! окютныь вьщьо I на гмцгплшщи и д_и_ I вин
- •8.6. Оказание помощи. Медицинская защита
- •Глава 9. Отравляющие
- •1Э«1» Основные формы
- •Перечень овтв, вызывающих раздражение и воспалительные процессы в дыхательных путях
- •Овтв, вызывающие отек легких
- •9.2. Овтв удушающего действия
- •9.2.1. Характеристика отдельных представителей овтв удушающего действия
- •9.2.1.2. Хлор
- •9.2.1.3. Оксиды азота
- •9.2.1.4. Паракват
- •Токсичность (ld50) параквата для грызунов, мг/кг
- •9.2.2. Диагностика поражения овтв удушающего действия
- •9.2.3. Медицинская защита
- •Показания к принятию решений по оказанию помощи пораженным овтв удушающего действия
- •Часть I. Юксикология
- •Глава 9. Отравляющие и высокотоксичные вещьсiьаi iyj IbMuhu I цксичьскцго действия
- •Глава 10. Отравляющие
- •Часть I. Iuitwvmujiui ия
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •10.1. Овтв, нарушающие кислородтранспортные функции крови
- •10.1.1. Овтв, нарушающие функции гемоглобина
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •10.1.1.1. Овтв, образующие карбоксигемоглобин
- •10*1.1.1.1. Карбонилы металлов
- •10.1.1.1.2. Оксид углерода (со)
- •10.1.1.2. Овтв, образующие метгемоглобин
- •10.1.1.2.1. Нитро- и аминосоединения ароматического ряда
- •10.1.1.2.2. Нитриты
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •10.1.12.3. Взрывные (пороховые) газы
- •Часть I. Токсикология
- •10.1.2. Овтв, разрушающие эритроциты (гемолитики)
- •Глава 10. Отравляющие и высоко I рКиичньи: вьщьо I ва ирщспццри ил и цсии I от»
- •10.1.21.1. Мышьяковистый водород (Арсин — AsH3)
- •10.2. Овтв, нарушающие тканевые процессы биоэнергетики
- •10.2.1. Ингибиторы ферментов цикла Кребса
- •10.2.1.1. Фторорганические соединения
- •10.2.1.2. Фторуксусная кислота
- •Часть I. Юксикология
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •10.21.2!. Ингибиторы цепи дыхательных ферментов
- •10.2.2.1. Синильная кислота и ее соединения
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •10.2.3. Разобщители тканевого дыхания
- •10.2.3.1. Динитро-орто-крезол Физико-химические свойства. Токсичность
- •Глава 11. Отравляющие
- •11.1.1.1. Иприты
- •Глава 11. Отравляющие и высокотоксичные вещества цит0т0ксическ0г0 действия
- •Глава 11. Отравляющие и высокотоксичные вещества цитотоксического действия
- •11.1.2. Ингибиторы синтеза белка, не образующие аддукты днк и рнк
- •Глава 11. Отравляющие и высокотоксичные вещества цитотоксического действия
- •11.2. Тиоловые яды
- •11.2.1. Соединения мышьяка
- •11.2.1.1. Неорганические соединения мышьяка
- •11.2.1.2. Галогенированные алифатические арсины
- •11.2.1.3. Галогенированные ароматические арсины
- •Глава 11. Отравляющие и высокотоксичные вещества цитотоксического действия
- •11.3. Токсичные модификаторы пластического обмена
- •11.3.1. Диоксины
- •Токсичность диоксина для разных видов животных при внутрибрюшинном введении
- •11.3.2. Полихлорированные бифенилы (пхб)
- •Глава 12. Отравляющие
- •12.1. Вещества, вызывающие преимущественно функциональные нарушения со стороны нервной системы
- •12.11. Отравляющие и высокотоксичные вещества нервно-паралитического действия
- •Возможные общие механизмы генерации судорожного синдрома
- •12.1.1.1. Отравляющие и высокотоксичные вещества судорожного действия
- •12.1.1*1.1.1. Ингибиторы холинэстеразы
- •0,006 Г/человека
- •Часть I. I и кии кили I ни
- •Глава 12. Отравляющие и высокотоксичные вещества неиротоксического действия
- •Основные направления разработки средств медицинской защиты от фосфорорганических отравляющих веществ (по с. Н. Голикову и соавт., 1972)
- •Основные направления патогенетической и симптоматической терапии
- •Группы препаратов
- •12.1.1.1.2.3. Антагонисты гамк
- •12.1.1.2. Отравляющие и высокотоксичные вещества паралитического действия
- •12.1.1*2.1. Пресинаптические блокаторы высвобождения ацетилхолина
- •12.1.2. Отравляющие и высокотоксичные вещества психодислептического действия
- •Химическая классификация психодислептиков
- •12.1.2.2. Делириогены
- •«Психотомиметические» дозы некоторых холинолитиков
- •12.1.2.2.2. Фенциклидин (сернил)
- •12.2. Вещества, вызывающие органические повреждения нервной системы
- •12.2.1. Таллий
- •12.2.2. Тетраэтилсвинец (тэс)
- •Часть II радиобиология
- •Раздел III. Общап радиобиология
- •Глава 13. Предмет, цель и задачи радиобиологии
- •Глава 14. Виды ионизирующих излучений и их свойства
- •14.1. Электромагнитные ионизирующие излучения
- •14.2. Корпускулярные ионизирующие излучения
- •Глава 15. Радионуклиды как источник радиационной опасности
- •15.1. Радиоактивность.
- •15.2. Количество радиоактивных веществ. Радиометрия
- •15.3. Источники радионуклидов. Радионуклиды в природе и народном хозяйстве
- •Глава 16. Радиобиологические эффекты
- •Глава 16.
- •16.1 Классификация радиобиологических эффектов
- •16.1.1. Уровень формирования
- •16.1.2» Сроки появления
- •16.1.3. Локализация
- •16.1.4. Характер связи с дозой облучения
- •16.1.5» Значение для судьбы облученного организма
- •16.2. Начальные этапы биологической стадии в действии ионизирующих излучений
- •16.2.1. Первичные стадии в действии излучений
- •16.2.2. Молекулярные механизмы лучевого повреждения биосистем
- •16.3. Реакции клеток на облучение
- •16.3.1, Биологическое усиление радиационного поражения
- •16.3.2. Репарация лучевых повреждений
- •16.3.3. Судьба облученной клетки
- •16.3.4. Количественные характеристики лучевого поражения клеток
- •16.4. Действие излучений на ткани, органы и системы. Радиочувствительность тканей
- •16.4.1. Радиационное поражение системы крови
- •16.4.2. Радиационное поражение органов желудочно-кишечного тракта
- •16.4.3. Лучевое поражение центральной нервной системы
- •Раздел IV. Военная радиобиология
- •Глава 17. Факторы, вызывающие поражения личного состава войск при ядерных взрывах и радиационных авариях
- •17.1. Поражающие факторы ядерного взрыва
- •17.1.1. Радиационные поражающие факторы ядерного взрыва
- •17.1.2. Нерадиационные поражающие факторы ядерного взрыва
- •17.21. Характеристика лучевых поражений
- •Глава 18. Лучевые поражения в результате внешнего облучения
- •18.1. Классификация лучевых поражений от внешнего облучения в зависимости от вида и условий воздействия
- •18.2. Зависимость эффекта облучения от его продолжительности
- •18.3. Зависимость эффекта облучения от распределения поглощенной дозы в объеме тела
- •Глава 19. Лучевые поражения в результате общего (тотального) облучения
- •19.1. Острая лучевая болезнь
- •19.1.2. Кишечная форма острой лучевой болезни
- •19.1.3. Токсемическая форма острой лучевой болезни
- •19.1.1. Церебральная форма острой лучевой болезни
- •19.2. Особенности поражений нейтронами
- •19.3. Отдаленные последствия общего (тотального) облучения
- •19.3.1. Неопухолевые отдаленные последствия облучения
- •19.3.2. Канцерогенные эффекты облучения
- •19.3.3. Сокращение продолжительности жизни
- •Глава 20. Медицинская защита от внешнего облучения
- •20.1. Радиопротекторы
- •20.1.1. Показатели защитной эффективности радиопротекторов
- •20.1.2. Механизмы радиозащитного действия
- •20.1.3. Краткая характеристика и порядок применения радиопротекторов, имеющих наибольшее практическое значение
- •20.2. Средства длительного поддержания повышенной радиорезистентности организма
- •Глава 20. Медицинская защита от внешнего облучения
- •20.3. Средства профилактики общей первичной реакции на облучение
- •Глава 20. Медицинская защита от внешнего облучения
- •20.4. Средства профилактики ранней преходящей недееспособности
- •20.5. Средства раннего (догоспитального) лечения острой лучевой болезни
- •Глава 21.
- •21.1. Местные лучевые поражения кожи
- •21.2. Местные лучевые поражения слизистых оболочек
- •21.3. Особенности местных лучевых поражений в результате наружного заражения кожных покровов р адионуклидами
- •Глава 22. Поражения в результате внутреннего радиоактивного заражения
- •22.1. Кинетика радионуклидов
- •22.1.1. Поступление радионуклидов в организм
- •22.1.2. Судьба радионуклидов, проникших в кровь
- •22.1.3. Выведение радионуклидов из организма
- •22.2. Биологическое действие радиоактивных веществ
- •22.2.2. Влияние на развитие поражения активности инкорпорированных радионуклидов и продолжительности их пребывания в организме
- •22.2.3. Последствия поступления
- •22.2.4. Лучевые поражения в результате алиментарного и ингаляционного поступления продуктов ядерного деления
- •Глава 22. Поражения в результате внутреннего радиоактивного заражения
- •22.3. Профилактика поражений радионуклидами. Медицинские средства защиты и раннего лечения
- •22.3.1. Специальные
- •Глава 22. Поражения в результате внутреннего радиоактивного заражения
- •22.3.2. Медицинские средства защиты и раннего (догоспитального) лечения при внутреннем заражении радиоактивными веществами
- •22.4. Ранняя диагностика и эвакуационные мероприятия при внутреннем заражении радиоактивными веществами
- •Глава 23. Сочетанные и комбинированные радиационные поражения
- •23.1* Сочетанные радиационные поражения
- •23.2. Комбинированные радиационные поражения
- •Глава 24. Технические средства индивидуальной и коллективной защиты
- •24.1. Средства индивидуальной защиты
- •24,1.1. Средства индивидуальной защиты органов дыхания
- •24.1.1.2. Факторы, определяющие порядок использования средств защиты органов дыхания
- •24.1.1.3. Использование сизод для защиты раненых и больных
- •24.1.2. Средства индивидуальной защиты кожи
- •24.1.2.1. Эксплуатационная характеристика
- •24.1.2.2. Факторы, определяющие порядок использования средств защиты кожных покровов
- •24*1.3. Средства индивидуальной защиты глаз
- •24.2. Коллективные средства защиты
- •Глава 25. Специальная обработка в подразделениях и частях медицинской службы
- •25.1. Основные понятия
- •25.2. Частичная специальная обработка
- •25.2.1. Средства, используемые
- •25.2.2. Организация и проведение частичной специальной обработки в медицинском пункте батальона
- •25.2.3. Организация и проведение частичной специальной обработки в медицинском пункте полка
- •25.3. Полная специальная обработка. Организация работы отделения специальной обработки (0с0)
- •Глава 26. Радиационная и химическая разведка в частях и подразделениях медицинской службы
- •26.1. Средства и методы радиационной разведки и контроля
- •26.2. Средства и методы химической разведки и контроля
- •26.3. Организация и проведение радиационной и химической разведки в подразделениях и частях медицинской службы
- •26.4. Организация и проведение контроля доз облучения личного состава, раненых и больных на этапах медицинской эвакуации
- •26.5. Организация и проведение экспертизы воды и продовольствия на зараженность отравляющими, высокотоксичными и радиоактивными веществами
- •Военная токсикология, радиобиология и медицинская защита
- •9785939290821Лицензия ид № 01081 от 28.02.2000 ооо «Издательство фолиант»
- •Ооо «Издательство фолиант»
- •190020, Санкт-Петербург, Нарвский пр., 18, оф. 501 тел./факс: (812) 325-39-86, 186-72-36 e-mail: foliant@peterlink.Ru
10.1.1.2. Овтв, образующие метгемоглобин
Как уже указывалось, железо, входящее в структуру гемоглобина, — двухвалентно, не зависимо от того, связан пигмент крови с кислородом (НЬО) или нет (НЬ). Более того, только находясь в двухвалентном состоянии (Fe+2), железо обладает необходимым для осуществления транспортных функций сродством к кислороду.
В нормальных условиях спонтанно и под влиянием различных патогенных факторов, в том числе химической природы, двухвалентное железо гемоглобина окисляется, переходя в трехвалентную форму. Образуется так называемый метгемоглобин (MetHb). Метгемоглобин не участвует в переносе кислорода от легких к тканям, поэтому значительное повышение его содержания в крови представляет опасность. Эволюционно сформировались механизмы обратного превращения метгемоглобина в гемоглобин. Благодаря этим механизмам у здорового человека уровень метгемоглобина в крови не превышает 0,5-2%. Существуют два основных механизма защиты железа гемоглобина от окисления.
Первый связан с «обезвреживанием» проникающих в эритроциты ксенобиотиков-окислителей до момента их действия на гемоглобин. Так, в присутствии энзима глутатионпероксидазы (ГПО) восстановленный глутатион взаимодействует с молекулами-окислителями, попавшими в клетки крови, предотвращая их метгемоглобинообразующее действие.
Несостоятельность этого механизма (снижение активности глутатионпе-роксидазы, содержания восстановленного глутатиона в эритроцитах) может привести к умеренной метгемоглобинемии и появлению в крови телец Гейнца (продукты денатурации гемоглобина).
Второй механизм обеспечивает восстановление уже образовавшегося в крови метгемоглобина при участии двух ферментативных систем: НАДН-зависимой и НАДФН-зависимой метгемоглобинредуктаз. В одной из них донорами электронов (восстанавливающих агентов) являются продукты анаэробного этапа метаболизма глюкозы (НАДН), в другой — гексозомонофосфатного превращения (НАДФН) (рис. 27).
Гексозомонофосфатный шунт
НАДФН-MetHbRed
НАДФН + HbFe(+3)-OH >■ HbFe(+2) + НАДФ + НЦО
кофактор
(5% общей восстановительной активности)
бой необратимый дериват Hb. Он никогда не встречается в нормальной крови и также не способен обратимо присоединять кислород, хотя и содержит двухвалентное железо.
Наиболее токсичные метгемоглобинообразователи относятся к одной
из следующих групп:
NH,
Соли азотистой кислоты (нитрит натрия)
Алифатические нитриты (амилнитрит, изопропилнитрит, бутил-нитрит)
Ароматические амины (анилин, аминофенол)
Ароматические нитраты (динитробензол, хлорнитробензол)
Производные гидроксиламина (фенилгидроксиламин)
Производные гидразина (фенилгидразин)
N0,
,N(CH3)2
Путь Эмбдена-Мейергофа
НАДН-MetHbRed
НАДН + HbFe(+3)-OH »► HbFe(+2) + НАД + Н20
(67% общей восстановительной активности)
Рис. 27. Механизмы восстановления метгемоглобина
В количественном отношении более значимым является механизм, связанный с гликолизом. Однако в процессе гексозомонофосфатного превращения под влиянием гексозо-6-фосфатдегидрогеназы (Г-6Ф-ДГ) образуется восстановленный никотинамидадениндинуклеотид фосфат (НАДФН), который не только участвует в превращении метгемоглобина в гемоглобин в присутствии НАДФН-метгемоглобинредуктазы, но и в восстановлении окисленного глутатиона при участии НАДФН-зависимой глутатионредуктазы. Поэтому значение этого механизма «защиты» гемоглобина также велико. По этой причине лица с врожденной недостаточностью Г-6Ф-ДГ весьма чувствительны даже к относительно невысоким дозам целого ряда токсикантов.
Основной причиной массивного образования метгемоглобина в крови до уровня, порой угрожающего жизни человека, является действие на организм химических веществ, так называемых метгемоглобинообразователей (оксидов азота, органических и неорганических нитро- и аминосоединений, фенолов, хлоратов, сульфонов и т. д.). Наряду с MetHb при интоксикациях подобными веществами в крови нередко появляется и другой продукт повреждения гемоглобина — сульфгемоглобин. В отличие от MetHb, который легко восстанавливается в организме за счет редуктазных ферментных систем обратно до гемоглобина, сульфгемоглобин представляет со
анилин
НО'
диметиламинфенол
нитробензол
NHNH,
CH3(CH2)2CHONO бутилнитрит
фенилгидразин
Некоторые из указанных веществ могут представлять интерес для военной медицины либо как возможные диверсионные агенты (нитрит натрия), либо как промышленные агенты, весьма опасные в плане образования зон химического заражения при авариях и катастрофах (анилин, динитробензол).
Попав в организм, метгемоглобинообразователи либо непосредственно активируют процессы, приводящие к окислению железа гемоглобина, либо первоначально метаболизируют с образованием реактивных продуктов, которые обладают этим свойством. Тяжесть развивающейся при этом патологии определяется дозой и скоростью поступления токсиканта в организм, а затем в эритроциты, их окислительно-восстановительным потенциалом, скоростью элиминации. Если действующим агентом является не исходное вещество, а продукт его метаболизма, то глубина патологического процесса зависит также от интенсивности процесса биоактивации ксенобиотика в организме. Поэтому у различных экспериментальных животных при введении им веществ, подвергающихся биоактивации, скорость образования метгемоглобина, как правило, существенно различается (табл. 28).
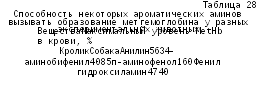 В
организме человека с большой скоростью
вызывают метгемоглоби-нообразование
соли азотистой кислоты (нитриты),
алкиламинофенолы (диэтил-, диметиламинофенол).
Медленно нарастает содержание MetHb
при отравлении анилином, нитробензолом.
В
организме человека с большой скоростью
вызывают метгемоглоби-нообразование
соли азотистой кислоты (нитриты),
алкиламинофенолы (диэтил-, диметиламинофенол).
Медленно нарастает содержание MetHb
при отравлении анилином, нитробензолом.
Проявления метгемоглобинемии
Выраженность симптомов отравления метгемоглобинообразователя-ми определяется глубиной формирующейся гипоксии (гемический тип), которая, в свою очередь, зависит от содержания метгемоглобина в крови. Симптомы, развивающиеся на фоне метгемоглобинообразования, представлены в табл. 29.
Таблица 29
Проявления метгемоглобинемии различной степени выраженности
|
Содержание метгемоглобина, % |
Проявления |
|
0-15 |
Отсутствуют |
|
15-20 |
Цианоз, возбуждение, состояние, напоминающее опьянение, 4 головная боль * |
|
20-45 |
Беспокойство, тахикардия, одышка при физической нагрузке, слабость, утомляемость, состояние оглушенности |
|
45-55 |
Угнетение сознания, ступор |
|
55-70 |
Судороги, кома, брадикардия, аритмии |
|
>70 |
Сердечная недостаточность, смерть |
Ранним проявлением интоксикации является цианоз кожных покровов и видимых слизистых оболочек. Цвет кожи — от синеватого до шоколадного; слизистые оболочки более коричневого, чем синего цвета. Цианоз развивается при содержании в крови метгемоглобина в количестве более 1,5 г на децилитр (около 10% НЬ). Наличие сульфгемоглобина резко усиливает цианоз, поскольку он в 3 раза темнее MetHb (артериальная кровь приобретает коричневатый оттенок). Поэтому изменение цвета кожных покровов и слизистых оболочек отмечается уже при содержании сульфгемоглобина в крови около 0,5 г на децилитр (около 3% НЬ). На фоне даже выраженного цианоза, вызванного сульфгемоглобинемией, отмечаются лишь незначительные признаки гипоксии. Как правило, су-льфгемоглобинемия не достигает уровня, опасного для жизни. Дифференцировать сульфгемоглобинемию от метгемоглобинемии можно с помощью спектрофотометрических методов исследования крови.
Цианоз при отравлении метгемоглобинообразователями иногда называют «центральным», поскольку развиваясь он сразу и относительно равномерно охватывает все участки кожных покровов, так как вся циркулирующая в организме отравленного кровь изменяет цвет. Необходимо отличать «центральный» цианоз от «периферического». Последний является признаком сердечной недостаточности и формируется вследствие нарушения гемодинамики и неадекватной гемоперфузии периферических органов. Наиболее ранние проявления такого цианоза — синюшная окраска носа и ногтевых лож. Причина «периферического» цианоза — избыточное содержание восстановленного гемоглобина вследствие усиленной экстракции кислорода тканями, плохо снабжаемыми кровью. Разлитой цианоз в таком случае развивается при содержании восстановленного гемоглобина в крови более 5 г на децилитр (около 30% НЬ).
При периферическом цианозе и повышенном содержании восстановленного гемоглобина в крови показана ингаляция кислорода. При наличии метгемоглобина или сульфгемоглобина в крови оксигенотерапия не приводит к устранению цианоза. Более того, назначение кислорода отравленным метгемоглобинообразователями может сопровождаться повышением уровня метгемоглобина в крови.
Определение метгемоглобина
Ряд простейших методических приемов позволяет иногда выявить наличие метгемоглобина в крови.
Если пигмента в крови более 15%, капля крови окрашивает фильтровальную бумажку в «шоколадный» цвет, хорошо выявляемый при сравнении с цветом нормальной крови.
Пропускание кислорода через венозную кровь изменяет ее вишневый цвет на алый. Кровь, содержащая метгемоглобин, не меняет при этом окраску. Наконец, добавление к разведенной в 100 раз крови, содержащей метгемоглобин, кристаллика цианистого калия приводит к ее окрашиванию в розовый цвет вследствие образования цианметгемоглобина.
Диагностическими признаками массивного метгемоглобинообразования является коричнево-черное окрашивание мочи, а также появление в ней белка.
С помощью спектрофотометрических исследований можно отличить метгемоглобин от сульфгемоглобина, а также определить процентное содержание метгемоглобина в крови. Если время, прошедшее от момента забора крови до исследования, продолжительное, результат может оказаться ложным, так как процессы окисления и восстановления гемоглобина проходят и in vitro. Необходимо помнить, что у больных с выраженной анемией даже незначительное содержание метгемоглобина в крови может
вызвать глубокую гипоксию. Поэтому обследование крови отравленного должно обязательно сопровождаться подсчетом эритроцитов и определением общего количества гемоглобина.
