
- •Печатается согласно редакционно-издательскону плану Военно-медицинской академии имени с. М. Кирова, утвержденному начальником Главного военно-медицинского управления
- •Глава 6. Антидоты. Общие принципы оказания неотложной помощи отравленным
- •Глава 11. Отравляющие и высокотоксичные вещества цитотоксического действия
- •Глава 12. Отравляющие и высокотоксичные вещества нейротоксического действия
- •Часть II. Радиобиология 337
- •Раздел IV. Военная радиобиология 380
- •Глава 17. Факторы, вызывающие поражения личного состава войск при ядерных
- •Глава 18. Лучевые поражения в результате внешнего облучения (н. В. Бутомо) 385
- •ГЛава 19. Лучевые поражения в результате общего (тотального) облучения
- •Глава 20. Медицинская защита от внешнего облучения (а. Н. Гребенюк,
- •Глава 21. Местные лучевые поражения (а. Н. Гребенюк, н. В. Бутомо) 418
- •Глава 22. Поражения в результате внутреннего радиоактивного заражения
- •Глава 23. Сочетанные и комбинированные радиационные поражения
- •Часть III. Средства и методы профилактики химических
- •Глава 24. Технические средства индивидуальной и коллективной защиты
- •Глава 25. Специальная обработка в подразделениях и частях медицинской службы
- •Глава 26. Радиационная и химическая разведка в частях и подразделениях
- •Часть I токсикология
- •Глава 1. Предмет, цель, задачи и структура токсикологии
- •1.1. Предмет токсикологии
- •Часть I. Токсикология
- •1.2L Цель и задачи токсикологии
- •Глава 1. Предмет, цель, задачи и структура токсикологии
- •1.3. Структура токсикологии
- •Часть I. Токсикология
- •Глава 2. Основные понятия токсикологии
- •2.1. Токсикант (яд)
- •2.2. Токсический процесс
- •Глава 3. Токсикометрия
- •Глава 4. Токсикокинетика
- •Признаки специфического транспорта
- •Транспорт веществ путем цитозов
- •1.2. Резорбция
- •Часть I. Токсикология
- •4.4.1. Экскреция
- •4.5» Количественные характеристики токсикокинетики
- •Глава 5. Токсикодинамика
- •5.1. Механизм токсического действия
- •5.1.1. Химизм реакции токсикант — рецептор
- •5.1.2. Взаимодействие токсикантов с белками
- •5.1.3» Взаимодействие токсикантов с нуклеиновыми кислотами
- •5.1.4. Взаимодействие токсикантов с липидами мембран
- •5.1.5. Взаимодействие с реактивными структурами возбудимых мембран
- •5.2. Общие механизмы цитотоксичности
- •5.2.1. Нарушение процессов биоэнергетики
- •5.2.2. Активация свободнорадикальных процессов в клетке
- •Энзиматическая и неэнзиматическая защита клеток ► супероксиддисмутаза ♦ катапаза ♦ gsh-пероксидаза ♦ gssg-редуктаза ♦ аскорбат ♦ глутатион ♦ мочевая кислота ♦ токоферол
- •Манифестация активации свободнорадикальных процессов
- •5.2.3* Повреждение мембранных структур
- •Экзогенные фосфолипазы (змеиные яды)
- •Фосфолипиды (гидролиз)
- •5.2*4. Нарушение гомеостаза внутриклеточного кальция
- •Часть I. Токсикология
- •5.2.5. Повреждение процессов синтеза белка и клеточного деления
- •Возможные точки приложения повреждающего действия токсикантов на процессы синтеза белка и клеточного деления
- •2. Синтез рнк. Транскрипция " .
- •5.3. Развитие токсического процесса
- •Глава 6. Антидоты. Общие принципы оказания неотложной помощи отравленным
- •6.1. Характеристика современных антидотов
- •Глава 6. Антидоты. Общие принци11ы оказании ньШлижпии I шмцщи и I гаш ItnnWm
- •6.2. Применение противоядий
- •6.3. Разработка новых антидотов
- •6.4. Основные принципы оказания первой, доврачебной и первой врачебной помощи при острых отравлениях
- •Раздел II. Военная токсикология
- •Глава 7. Основные понятия военной токсикологии
- •7.1. Предмет, цели, задачи военной токсикологии
- •7.2. Отравляющие и высокотоксичные вещества (овтв)
- •Часть I. Токсикология
- •Глава 7. Основные понятия военной токсикологии
- •7М. Медицинская противохимическая защита
- •Глава 8. Отравляющие
- •8.1. Общая характеристика
- •8.2. Физико-химические свойства. Токсичность
- •8.3. Методы изучения раздражающего действия
- •8.4. Основные проявления поражения
- •Часть I. Токсикология
- •Глава 8. Отравляющие и высокотоксичныь ньщсыок тдцт,»™—- „
- •8.5. Патогенез токсического процесса. Механизм действия
- •Часть I. Токсикология
- •Глава 8. Отравляющие и высоко! окютныь вьщьо I на гмцгплшщи и д_и_ I вин
- •8.6. Оказание помощи. Медицинская защита
- •Глава 9. Отравляющие
- •1Э«1» Основные формы
- •Перечень овтв, вызывающих раздражение и воспалительные процессы в дыхательных путях
- •Овтв, вызывающие отек легких
- •9.2. Овтв удушающего действия
- •9.2.1. Характеристика отдельных представителей овтв удушающего действия
- •9.2.1.2. Хлор
- •9.2.1.3. Оксиды азота
- •9.2.1.4. Паракват
- •Токсичность (ld50) параквата для грызунов, мг/кг
- •9.2.2. Диагностика поражения овтв удушающего действия
- •9.2.3. Медицинская защита
- •Показания к принятию решений по оказанию помощи пораженным овтв удушающего действия
- •Часть I. Юксикология
- •Глава 9. Отравляющие и высокотоксичные вещьсiьаi iyj IbMuhu I цксичьскцго действия
- •Глава 10. Отравляющие
- •Часть I. Iuitwvmujiui ия
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •10.1. Овтв, нарушающие кислородтранспортные функции крови
- •10.1.1. Овтв, нарушающие функции гемоглобина
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •10.1.1.1. Овтв, образующие карбоксигемоглобин
- •10*1.1.1.1. Карбонилы металлов
- •10.1.1.1.2. Оксид углерода (со)
- •10.1.1.2. Овтв, образующие метгемоглобин
- •10.1.1.2.1. Нитро- и аминосоединения ароматического ряда
- •10.1.1.2.2. Нитриты
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •10.1.12.3. Взрывные (пороховые) газы
- •Часть I. Токсикология
- •10.1.2. Овтв, разрушающие эритроциты (гемолитики)
- •Глава 10. Отравляющие и высоко I рКиичньи: вьщьо I ва ирщспццри ил и цсии I от»
- •10.1.21.1. Мышьяковистый водород (Арсин — AsH3)
- •10.2. Овтв, нарушающие тканевые процессы биоэнергетики
- •10.2.1. Ингибиторы ферментов цикла Кребса
- •10.2.1.1. Фторорганические соединения
- •10.2.1.2. Фторуксусная кислота
- •Часть I. Юксикология
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •10.21.2!. Ингибиторы цепи дыхательных ферментов
- •10.2.2.1. Синильная кислота и ее соединения
- •Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
- •10.2.3. Разобщители тканевого дыхания
- •10.2.3.1. Динитро-орто-крезол Физико-химические свойства. Токсичность
- •Глава 11. Отравляющие
- •11.1.1.1. Иприты
- •Глава 11. Отравляющие и высокотоксичные вещества цит0т0ксическ0г0 действия
- •Глава 11. Отравляющие и высокотоксичные вещества цитотоксического действия
- •11.1.2. Ингибиторы синтеза белка, не образующие аддукты днк и рнк
- •Глава 11. Отравляющие и высокотоксичные вещества цитотоксического действия
- •11.2. Тиоловые яды
- •11.2.1. Соединения мышьяка
- •11.2.1.1. Неорганические соединения мышьяка
- •11.2.1.2. Галогенированные алифатические арсины
- •11.2.1.3. Галогенированные ароматические арсины
- •Глава 11. Отравляющие и высокотоксичные вещества цитотоксического действия
- •11.3. Токсичные модификаторы пластического обмена
- •11.3.1. Диоксины
- •Токсичность диоксина для разных видов животных при внутрибрюшинном введении
- •11.3.2. Полихлорированные бифенилы (пхб)
- •Глава 12. Отравляющие
- •12.1. Вещества, вызывающие преимущественно функциональные нарушения со стороны нервной системы
- •12.11. Отравляющие и высокотоксичные вещества нервно-паралитического действия
- •Возможные общие механизмы генерации судорожного синдрома
- •12.1.1.1. Отравляющие и высокотоксичные вещества судорожного действия
- •12.1.1*1.1.1. Ингибиторы холинэстеразы
- •0,006 Г/человека
- •Часть I. I и кии кили I ни
- •Глава 12. Отравляющие и высокотоксичные вещества неиротоксического действия
- •Основные направления разработки средств медицинской защиты от фосфорорганических отравляющих веществ (по с. Н. Голикову и соавт., 1972)
- •Основные направления патогенетической и симптоматической терапии
- •Группы препаратов
- •12.1.1.1.2.3. Антагонисты гамк
- •12.1.1.2. Отравляющие и высокотоксичные вещества паралитического действия
- •12.1.1*2.1. Пресинаптические блокаторы высвобождения ацетилхолина
- •12.1.2. Отравляющие и высокотоксичные вещества психодислептического действия
- •Химическая классификация психодислептиков
- •12.1.2.2. Делириогены
- •«Психотомиметические» дозы некоторых холинолитиков
- •12.1.2.2.2. Фенциклидин (сернил)
- •12.2. Вещества, вызывающие органические повреждения нервной системы
- •12.2.1. Таллий
- •12.2.2. Тетраэтилсвинец (тэс)
- •Часть II радиобиология
- •Раздел III. Общап радиобиология
- •Глава 13. Предмет, цель и задачи радиобиологии
- •Глава 14. Виды ионизирующих излучений и их свойства
- •14.1. Электромагнитные ионизирующие излучения
- •14.2. Корпускулярные ионизирующие излучения
- •Глава 15. Радионуклиды как источник радиационной опасности
- •15.1. Радиоактивность.
- •15.2. Количество радиоактивных веществ. Радиометрия
- •15.3. Источники радионуклидов. Радионуклиды в природе и народном хозяйстве
- •Глава 16. Радиобиологические эффекты
- •Глава 16.
- •16.1 Классификация радиобиологических эффектов
- •16.1.1. Уровень формирования
- •16.1.2» Сроки появления
- •16.1.3. Локализация
- •16.1.4. Характер связи с дозой облучения
- •16.1.5» Значение для судьбы облученного организма
- •16.2. Начальные этапы биологической стадии в действии ионизирующих излучений
- •16.2.1. Первичные стадии в действии излучений
- •16.2.2. Молекулярные механизмы лучевого повреждения биосистем
- •16.3. Реакции клеток на облучение
- •16.3.1, Биологическое усиление радиационного поражения
- •16.3.2. Репарация лучевых повреждений
- •16.3.3. Судьба облученной клетки
- •16.3.4. Количественные характеристики лучевого поражения клеток
- •16.4. Действие излучений на ткани, органы и системы. Радиочувствительность тканей
- •16.4.1. Радиационное поражение системы крови
- •16.4.2. Радиационное поражение органов желудочно-кишечного тракта
- •16.4.3. Лучевое поражение центральной нервной системы
- •Раздел IV. Военная радиобиология
- •Глава 17. Факторы, вызывающие поражения личного состава войск при ядерных взрывах и радиационных авариях
- •17.1. Поражающие факторы ядерного взрыва
- •17.1.1. Радиационные поражающие факторы ядерного взрыва
- •17.1.2. Нерадиационные поражающие факторы ядерного взрыва
- •17.21. Характеристика лучевых поражений
- •Глава 18. Лучевые поражения в результате внешнего облучения
- •18.1. Классификация лучевых поражений от внешнего облучения в зависимости от вида и условий воздействия
- •18.2. Зависимость эффекта облучения от его продолжительности
- •18.3. Зависимость эффекта облучения от распределения поглощенной дозы в объеме тела
- •Глава 19. Лучевые поражения в результате общего (тотального) облучения
- •19.1. Острая лучевая болезнь
- •19.1.2. Кишечная форма острой лучевой болезни
- •19.1.3. Токсемическая форма острой лучевой болезни
- •19.1.1. Церебральная форма острой лучевой болезни
- •19.2. Особенности поражений нейтронами
- •19.3. Отдаленные последствия общего (тотального) облучения
- •19.3.1. Неопухолевые отдаленные последствия облучения
- •19.3.2. Канцерогенные эффекты облучения
- •19.3.3. Сокращение продолжительности жизни
- •Глава 20. Медицинская защита от внешнего облучения
- •20.1. Радиопротекторы
- •20.1.1. Показатели защитной эффективности радиопротекторов
- •20.1.2. Механизмы радиозащитного действия
- •20.1.3. Краткая характеристика и порядок применения радиопротекторов, имеющих наибольшее практическое значение
- •20.2. Средства длительного поддержания повышенной радиорезистентности организма
- •Глава 20. Медицинская защита от внешнего облучения
- •20.3. Средства профилактики общей первичной реакции на облучение
- •Глава 20. Медицинская защита от внешнего облучения
- •20.4. Средства профилактики ранней преходящей недееспособности
- •20.5. Средства раннего (догоспитального) лечения острой лучевой болезни
- •Глава 21.
- •21.1. Местные лучевые поражения кожи
- •21.2. Местные лучевые поражения слизистых оболочек
- •21.3. Особенности местных лучевых поражений в результате наружного заражения кожных покровов р адионуклидами
- •Глава 22. Поражения в результате внутреннего радиоактивного заражения
- •22.1. Кинетика радионуклидов
- •22.1.1. Поступление радионуклидов в организм
- •22.1.2. Судьба радионуклидов, проникших в кровь
- •22.1.3. Выведение радионуклидов из организма
- •22.2. Биологическое действие радиоактивных веществ
- •22.2.2. Влияние на развитие поражения активности инкорпорированных радионуклидов и продолжительности их пребывания в организме
- •22.2.3. Последствия поступления
- •22.2.4. Лучевые поражения в результате алиментарного и ингаляционного поступления продуктов ядерного деления
- •Глава 22. Поражения в результате внутреннего радиоактивного заражения
- •22.3. Профилактика поражений радионуклидами. Медицинские средства защиты и раннего лечения
- •22.3.1. Специальные
- •Глава 22. Поражения в результате внутреннего радиоактивного заражения
- •22.3.2. Медицинские средства защиты и раннего (догоспитального) лечения при внутреннем заражении радиоактивными веществами
- •22.4. Ранняя диагностика и эвакуационные мероприятия при внутреннем заражении радиоактивными веществами
- •Глава 23. Сочетанные и комбинированные радиационные поражения
- •23.1* Сочетанные радиационные поражения
- •23.2. Комбинированные радиационные поражения
- •Глава 24. Технические средства индивидуальной и коллективной защиты
- •24.1. Средства индивидуальной защиты
- •24,1.1. Средства индивидуальной защиты органов дыхания
- •24.1.1.2. Факторы, определяющие порядок использования средств защиты органов дыхания
- •24.1.1.3. Использование сизод для защиты раненых и больных
- •24.1.2. Средства индивидуальной защиты кожи
- •24.1.2.1. Эксплуатационная характеристика
- •24.1.2.2. Факторы, определяющие порядок использования средств защиты кожных покровов
- •24*1.3. Средства индивидуальной защиты глаз
- •24.2. Коллективные средства защиты
- •Глава 25. Специальная обработка в подразделениях и частях медицинской службы
- •25.1. Основные понятия
- •25.2. Частичная специальная обработка
- •25.2.1. Средства, используемые
- •25.2.2. Организация и проведение частичной специальной обработки в медицинском пункте батальона
- •25.2.3. Организация и проведение частичной специальной обработки в медицинском пункте полка
- •25.3. Полная специальная обработка. Организация работы отделения специальной обработки (0с0)
- •Глава 26. Радиационная и химическая разведка в частях и подразделениях медицинской службы
- •26.1. Средства и методы радиационной разведки и контроля
- •26.2. Средства и методы химической разведки и контроля
- •26.3. Организация и проведение радиационной и химической разведки в подразделениях и частях медицинской службы
- •26.4. Организация и проведение контроля доз облучения личного состава, раненых и больных на этапах медицинской эвакуации
- •26.5. Организация и проведение экспертизы воды и продовольствия на зараженность отравляющими, высокотоксичными и радиоактивными веществами
- •Военная токсикология, радиобиология и медицинская защита
- •9785939290821Лицензия ид № 01081 от 28.02.2000 ооо «Издательство фолиант»
- •Ооо «Издательство фолиант»
- •190020, Санкт-Петербург, Нарвский пр., 18, оф. 501 тел./факс: (812) 325-39-86, 186-72-36 e-mail: foliant@peterlink.Ru
Экзогенные фосфолипазы (змеиные яды)
|
эндогенный кальций |
|
ТОКСИКАНТЫ |
|
|
![]()
Фосфолипиды (гидролиз)
А —У\
—У\
инозитол трифосфат
фактор агрегации тромбоцитов
фосфатидиловая кислота
диацил-глицерол
простагландины
простациклины
тромбоксаны
COOH
COR,
COR,0 I -I СО—Р—О
I
R3
фактор агрегации тромбоцитов
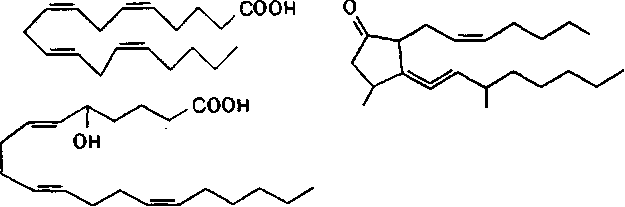
НО ОН
простагландин
ПП1ИПИПК1 -—
леикотриены
Рис. 17. Образование биологически активных веществ при участии фосфолипаз, активируемых в ходе токсического процесса
Поскольку система внутриклеточных мембран также является мишенью для действия многочисленных токсикантов, среди них можно выделить группу митохондриальных ядов, повреждающих различные звенья процессов биоэнергетики, — веществ, действующих на шероховатый (нарушение процессов синтеза белка) и гладкий эндоплазматический рети-кулум (индукция или угнетение метаболизма ксенобиотиков), лизосома-льные мембраны (провоцируют аутолиз клеток) и др.
5.2*4. Нарушение гомеостаза внутриклеточного кальция
Нарушение гомеостаза внутриклеточного кальция, сопровождающееся существенным повышением его концентрации в цитоплазме клетки, лежит, как полагают, в основе механизма клеточной гибели при различных патологических состояниях, в том числе при острых отравлениях. Цито-токсическое действие самых разных токсикантов (цианидов, четыреххло-ристого углерода, свинца, органических соединений олова и ртути, алки-лирующих агентов, диоксина и т. д.), как полагают, хотя бы отчасти связано с повышением уровня кальция внутри клеток.
2+
Са
АТФ
АДФ
1,3 мМ и
2+
2+
Са2+ 100 нМ
Са
КЛЕТКА
Са
митохондрии
Н+ Na+
АТФ
АТФ
эндоплазматический ретикулум
2+
АДФ
Са
ядро
Рис. 18. Схема регуляции ионов кальция в цитоплазме
Нарушение механизмов поддержания гомеостаза внутриклеточного кальция, как это видно из представленной схемы обмена иона, может стать следствием:
повреждения биологических мембран и усиления их проницаемости для ионов;
нарушения биоэнергетики клетки, приводящего к истощению запасов макроэрогов;
изменения функционального состояния белковых комплексов (в том числе путем действия на соответствующие рецепторы), образующих каналы для Са2+.
Все эти механизмы могут приводить к усилению инфлюкса кальция из внеклеточной жидкости и его высвобождению из депо в цитоплазму клетки. Примеры веществ, повреждающих механизмы поддержания гомеостаза кальция внутри клеток, представлены в табл. 11.
Таблица 11
Некоторые вещества, нарушающие внутриклеточный гомеостаз кальция
|
1. Высвобождение кальция из митохондрий: - динитрофенол » динитрокрезол • кадмий |
3. Усиление поступления кальция через плазматическую мембрану: * четыреххлористый углерод ♦ 2,3,7,8-тетрахлордибензо-п-диоксин |
|
2. Высвобождение кальция из эндоплазматического ретикулума: ♦ четыреххлористый углерод ♦ бромбензол ♦ перекиси ♦ альдегиды |
4. Угнетение эффлюкса кальция из клетки: ♦ цистамин ♦ хиноны ♦ паракват t, ♦ ванадий |
Цитотоксический эффект, опосредованный стойким повышением содержания свободного кальция в цитоплазме, в настоящее время связывают с развивающимся при этом повреждением целостности цитоскелета и неконтролируемой активацией катаболических энзимов (фосфолипаз, протеаз, эндонуклеаз).
Повреждение цитоскелета. Цитоплазма клетки помимо цитозоля и клеточных органелл, как правило, содержит еще и нитевидные белковые структуры, которые в массе формируют клеточный скелет. Это образование выполняет не только стабилизирующую и структурирующую, но и другие функции, среди которых обеспечение клеточного деления, внутриклеточный транспорт, секреция, обмен рецепторных белков, регуляция клеточной подвижности и формы.
При действии разнообразных веществ на изолированные клетки (культура ткани) выявляется отчетливое изменение формы их поверхности: появляются выпячивания цитоплазмы (пузырьками — blebs). Такое «пу-зырение» (или вскипание — blebbing) клеточной мембраны — один из ранних признаков разрушения сети цитоскелета, предшествующий разрушению клетки.
Кальций вовлечен в процесс поддержания структуры цитоскелета через ряд Са2+-связывающих протеинов и Са2+-зависимых энзимов, обеспечивающих ассоциацию белков цитоскелета с белками плазматической мембраны. Во-первых, стойкое увеличение концентрации кальция в ци-тозоле разрушает комплекс актина микрофиламентов с а-актинином, белком, связывающим микрофиламенты цитоскелета с белками плазматической мембраны. Во-вторых, Са2+ активирует протеазы (см. ниже), которые могут расщеплять актин-связывающие белки, разрушая тем самым места прикрепления филаментов цитоскелета к клеточной мембране. Отщепление цитоскелета от мембраны приводит к ослаблению фик-
7В
73
