
- •1. Коhдуктометрия. Аhализ по электрической проводимости.
- •1.1. Теоретические основы
- •1.2. Кондуктометрическое титрование
- •2. Высокочастhое коhдуктометрическое титроваhие
- •2.1. Сущность метода
- •2.2. Практические работы
- •1. Аппаратура, материалы и реактивы
- •3. Выполнение работы
- •1) Установка точной концентрации титранта
- •1. Аппаратура, материалы и реактивы
- •2) Проведение титрования.
- •2.3. Вопросы и задачи
- •3. Потеhциометрия
- •3.1. Теоретические основы метода
- •3.1.1. Электродный потенциал
- •3.1.2. Сущность потенциометрического метода анализа
- •3.1.3. Индикаторные электроды
- •3.1.4. Электроды сравнения
- •3.1.5. Измерение потенциала индикаторного электрода
- •3.2. Прямые потенциометрические измерения
- •3.2.1. Измерение рH (активной кислотности среды)
- •3.2.2. Определение активности (концентрации) ионов с помощью ионоселективных электродов
- •3.2.3. Практические работы
- •1. Аппаратура, материалы и реактивы
- •2. Выполнение работы
- •3. Окончание работы
- •1. Аппаратура, материалы и реактивы
- •2.Выполнение работы
- •3.2.4. Вопросы и задачи
- •3.3. Потеhциометрическое титроваhие
- •3.3.1. Сущность метода
- •3.3.2. Способы нахождения точки эквивалентности
- •3.3.3. Практические работы
- •1. Аппаратура, материалы и реактивы
- •1. Аппаратура, материалы и реактивы
- •1. Аппаратура, материалы и реактивы
- •3.3.4. Вопросы и задачи
- •4. Вольтамперометрия
- •4.1. Полярография постоянного тока (классическая)
- •4.2. Теоретические основы полярографии
- •4.3. Электроды, применяемые в полярографии
- •4.4. Полярография переменного тока
- •4.5. Инверсионная вольтамперометрия.
- •4.5. Практические работы
- •1. Аппаратура, материалы и реактивы
- •1. Аппаратура, материалы и реактивы
- •2. Ход анализа
- •2. Проведение анализа по методу ива
- •2.1. Запись вольтамперных кривых (вольтамперограмм).
- •4.7. Вопросы и задачи
- •5. Амперометрическое титроваhие
- •5.1. Теоретические основы метода
- •5.2. Практические работы
- •1. Аппаратура, материалы и реактивы
- •2. Подготовка установки к работе
- •3. Выполнение работы
- •4. Окончание работы
- •5.3. Вопросы и задачи
- •125080, Москва, Волоколамское ш., 11
4.5. Практические работы
Работа 1. Определение содержания ионов свинца и кадмия в растворе при совместном присутствии
Определение содержания ионов свинца и кадмия основано на анализе полярографических кривых, получаемых с применением ртутного капельного электрода в качестве индикаторного и с применением режима классической полярографии.
1. Аппаратура, материалы и реактивы
Полярограф любой марки.
Электрохимическая ячейка с двух-электродной системой: индикаторный электрод — ртутно-капельный (катод), вспомогательный электрод — донная ртуть (анод)
Потенциометр — предназначен для контроля выходного напряжения, подаваемого на электрохимическую ячейку
Бюретки вместимостью 25 мл
Мерный цилиндр вместимостью 10 мл
Мерные колбы вместимостью 100 мл
Стандартный раствор ионов свинца, 1 мг/мл
Стандартный раствор ионов кадмия, 1 мг/мл
Фоновый электролит — раствор HС1, 1 моль/л
2. Построение градуировочного графика
В 5-ти мерных колбах вместимостью 100 мл готовят серию стандартных растворов, содержащих свинец и кадмий. Для этого в каждую мерную колбу из бюреток приливают соответственно по 1, 2, 3, 4, 5 мл исходных стандартных растворов свинца и кадмия. В каждую колбу с помощью мерного цилиндра вносят по 10 мл 1 М раствора HС1. Растворы в колбах доводят до метки дистиллированной водой и тщательно перемешивают.
Снимают полярограммы полученных растворов, устанавливая величину стартового потенциала -0,35 В (значение величины стартового потенциала контролируют по потенциометру). Типичная полярограмма раствора, содержащего ионы Pb 2+ и Cd 2+ показана на рис 4.11.
По полученным полярограммам определяют величину потенциала полуволны для свинца и кадмия (измеряют отрезки d1 и d2 в мВ* см. рис. 4.9) и высоты волн свинца и кадмия. Результаты заносят в табл.1.
____________________________
* Зная скорость изменения потенциала — 2 мВ/с и скорость движения диаграммной ленты 1,2 см/мин, рассчитывают скольким мВ соответствует 1 см диаграммной ленты.

Рис. 4.11. Полярограмма раствора, содержащего ионы свинца и кадмия. Фон — 0,1 М раствор HС1.
Таблица 1
Результаты измерения высот полярографических волн стандартных растворов, содержащих ионы Pb2+ и Cd2+
|
№ раствора |
Концентрация стандартного раствора, мг/мл |
Высота полярографической волны, мм
| |
|
Pb (E 1|2 = |
Cd (E 1|2 = ) | ||
|
1 |
|
|
|
|
2 |
|
|
|
|
3 |
|
|
|
|
4 |
|
|
|
|
5 |
|
|
|
|
Задача |
|
|
|
По данным табл. 1 строят градуировочный график в координатах высота полярографической волны — концентрация Pb и Cd (пример градуировочного графика дан на рис. 4.11).
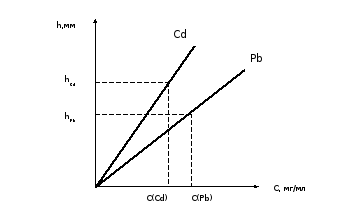
Рис. 4.12. Градуировочный график
3. Определение содержания ионов Pb 2+ и Cd 2+ в растворе неизвестной концентрации
Получают раствор неизвестного состава и неизвестной концентрации в мерной колбе вместимостью 100 мл. В колбу вносят с помощью мерного цилиндра 10 мл 1 М раствора HС1, доводят раствор до метки дистиллированной водой и тщательно перемешивают.
Снимают полярограмму этого раствора в тех же условиях, что и стандартных растворов. Hа полярограмме измеряют величины Е 1/2 (тем самым определяя качественный состав задачи) и высоты полярографических волн.
По градуировочному графику определяют концентрацию свинца и кадмия в задаче.
В заключении делают вывод, какие элементы содержатся в задаче и каково их содержание.
Работа 2. Определение токсичных элементов (медь, свинец, кадмий цинк) методом инверсионной вольтамперометрии
