
- •1. Коhдуктометрия. Аhализ по электрической проводимости.
- •1.1. Теоретические основы
- •1.2. Кондуктометрическое титрование
- •2. Высокочастhое коhдуктометрическое титроваhие
- •2.1. Сущность метода
- •2.2. Практические работы
- •1. Аппаратура, материалы и реактивы
- •3. Выполнение работы
- •1) Установка точной концентрации титранта
- •1. Аппаратура, материалы и реактивы
- •2) Проведение титрования.
- •2.3. Вопросы и задачи
- •3. Потеhциометрия
- •3.1. Теоретические основы метода
- •3.1.1. Электродный потенциал
- •3.1.2. Сущность потенциометрического метода анализа
- •3.1.3. Индикаторные электроды
- •3.1.4. Электроды сравнения
- •3.1.5. Измерение потенциала индикаторного электрода
- •3.2. Прямые потенциометрические измерения
- •3.2.1. Измерение рH (активной кислотности среды)
- •3.2.2. Определение активности (концентрации) ионов с помощью ионоселективных электродов
- •3.2.3. Практические работы
- •1. Аппаратура, материалы и реактивы
- •2. Выполнение работы
- •3. Окончание работы
- •1. Аппаратура, материалы и реактивы
- •2.Выполнение работы
- •3.2.4. Вопросы и задачи
- •3.3. Потеhциометрическое титроваhие
- •3.3.1. Сущность метода
- •3.3.2. Способы нахождения точки эквивалентности
- •3.3.3. Практические работы
- •1. Аппаратура, материалы и реактивы
- •1. Аппаратура, материалы и реактивы
- •1. Аппаратура, материалы и реактивы
- •3.3.4. Вопросы и задачи
- •4. Вольтамперометрия
- •4.1. Полярография постоянного тока (классическая)
- •4.2. Теоретические основы полярографии
- •4.3. Электроды, применяемые в полярографии
- •4.4. Полярография переменного тока
- •4.5. Инверсионная вольтамперометрия.
- •4.5. Практические работы
- •1. Аппаратура, материалы и реактивы
- •1. Аппаратура, материалы и реактивы
- •2. Ход анализа
- •2. Проведение анализа по методу ива
- •2.1. Запись вольтамперных кривых (вольтамперограмм).
- •4.7. Вопросы и задачи
- •5. Амперометрическое титроваhие
- •5.1. Теоретические основы метода
- •5.2. Практические работы
- •1. Аппаратура, материалы и реактивы
- •2. Подготовка установки к работе
- •3. Выполнение работы
- •4. Окончание работы
- •5.3. Вопросы и задачи
- •125080, Москва, Волоколамское ш., 11
1. Аппаратура, материалы и реактивы
Установка для ВЧ-титрования
Мерные колбы вместимостью 250 мл -- 2 шт.
Пипетка вместимостью 10 мл.
Ba(NO3)2 или BaCl2 ∙2H2O (квалификации х.ч. или о.с.ч.).
Ва(СН3СОО)2 ∙ Н2О (квалификации х.ч. или о.с.ч.).
Этиловый спирт.
2. Выполнение работы
1) Приготовление титранта (стандартных растворов Ba(NO3)2 или BaCl2 и Ba(СН3СОО)2.
Растворы готовят по точной навеске в мерных колбах вместимостью 250 мл. Концентрация титранта должна быть 0,01 н.
М[Ba(NO3)2] = 261.34 г/моль
M(BaCl2 Н2О) = 244.26 г/моль
М[Ba(СН3СОО)2 Н2О] = 273,43 г/моль.
По точной навеске рассчитывают концентрацию С[1/2 Ba(NO3)2]; C[1/2BaCl2 ∙2Н2О]; C[1/2Ba(СН3СОО)2 ∙Н2 O:
 ;
;

где: m - масса навески соли, г; Vк - вместимость мерной колбы, мл; M(Э) - молярная масса эквивалента соли, г/моль.
Титрант заливают в бюретку.
2) Проведение титрования.
Полученный в мерной колбе исследуемый раствор Na2SO4 доливают до метки дистиллированной водой, тщательно перемешивают. В стаканчик для титрования отбирают пипеткой 10,00 мл этого раствора, добавляют 30 мл этилового спирта (для понижения растворимости BaSO4), помещают в измерительную ячейку и добавляют дистиллированную воду так, чтобы уровень раствора был на 3-5 мм выше верхнего электрода.
Для ускорения образования осадка можно добавить несколько кристалликов BaSO4.
Включают магнитную мешалку для перемешивания раствора. Обороты необходимо отрегулировать так, чтобы не oбразовывалась воздушная воронка. Устанавливают стрелку показывающего прибора на деление 50 (чувствительность 3), проводят прикидочное титрование, добавляя по 1 мл титранта, по которому выбирают начальное положение стрелки показывающего прибора для проведения точного титрования. Точное титрование исследуемого раствора осуществляют не менее трех раз, добавляя титрант по 0,5 мл. Показания записывают в табл.1.
Таблица 1
Результаты титрования исследуемого раствора
|
1 титрование |
2 титрование |
3 титрование | |||
|
Vтитранта, мл
|
Показания прибора |
Vтитранта, мл
|
Показания прибора |
Vтитранта,
мл
|
Показания Прибора |
|
1 |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
3 |
|
|
|
|
|
|
и т.д |
|
|
|
|
|
По результатам анализа строят 3 кривых титрования (для каждого титрования), находят объем титранта, соответствующий к.т.т. и рассчитывают среднее значение объема титранта V(BaCl2) (или V[Ba(NO3)2 и V[Ba(CH3СОО)2]), затраченного на титрование. Сравнивают характер кривых для разных титрантов.
Содержание SO42- в объеме V рассчитывают по формуле
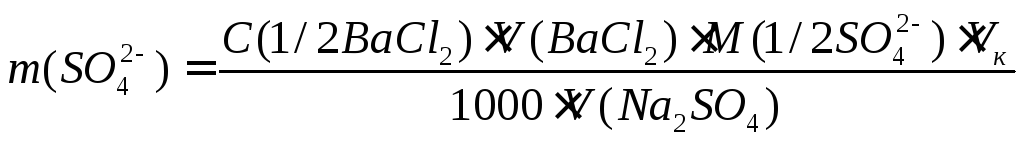 ,
,
где C(1/2BaCl2) - молярная концентрация эквивалента титранта, моль/л; V(BaCl2)-средний объем титранта, затраченный на титрование, мл; M(1/2 SO4 2-) - молярная масса эквивалента сульфат-иона, г/моль; Vк - вместимость мерной колбы, мл; V(Na2SO4) - объем исследуемого раствора, взятый на титрование, мл.
Сравнивают результат, полученный в случае применения титранта Ba(NO3)2 и Ba(CН3СОО)2.
3. Окончание работы. См. работу 1.
