
2683
.pdf
|
|
RT |
|
|
|
|
|
1 |
|
|
A |
|
|
1 |
V1 |
|
. |
(1) |
|||
1 |
|
|||||||||
12 |
|
|
V |
2 |
|
|
|
|||
|
|
|
|
|
|
|
|
|
||
Параметры |
первого |
состояния |
|
газа обозначим через |
||||||||||||
p0 ,V0 ,T1 , второго - |
p1,V1, T1 . Из уравнений адиабатического |
|||||||||||||||
процесса T V 1 |
TV 1 и |
p V |
pV |
находим: |
|
|
||||||||||
0 |
0 |
1 |
1 |
|
0 |
0 |
|
|
1 |
1 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
p1 |
|
|
|
|
||||||
|
|
|
|
1 ( 1) |
|
|
|
V0 |
|
|
|
V0 |
|
|
||
V0 V1 (T1 T0) |
, |
|
|
|
|
|
, |
|||||||||
p |
|
V |
|
|
V |
|
||||||||||
|
|
|
|
|
|
|
0 |
|
1 |
|
|
1 |
|
|
||
|
1 (T |
T )1 ( 1) |
T T ( 1)/ . |
|
(2) |
|||||||||||
|
|
|
1 |
0 |
|
|
|
1 |
|
0 |
|
|
|
|
||
Отношение объемов газа V |
0 |
/V 1 . Итак, работа, со- |
||||||||||||||
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
||
вершенная газом, равна
ART 1 ( 1)/ .
1
Для кислорода 1,4. При T0 290К и 10,0 темпе-
ратура конечного состояния газа T=290 100,4/1,4 560К , работа
A 1 8,31 290 1 100,4/1,4 5,6кДж . 1,4 1
6.38. Работа газа при адиабатическом и изотермическом процессах определяется выражениями:
Aад |
|
p1V1 |
1 (V1 |
V2 ) 1 , |
Aиз p1V1 ln(V2 V1). |
|
|||||
|
|
1 |
|
|
|
По условию V1 |
V2 (сжатие). Тогда отношение |
||||
Aад / Aиз 1 /( 1)lnn 1 1 /( 1)ln n .
Для азота 1,4; при 5,0 отношение работ
31
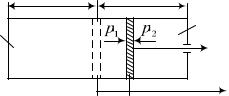
Aад |
|
1 |
[5 |
0,4 |
1]/ln5,0 1,4. |
|
|
|
Aиз 0,4
6.39. Цилиндрический сосуд теплоизолирован и, следовательно, содержащийся в нем газ в целом при перемещении поршня не обменивается теплом с окружающей средой (см. рисунок). Однако между частями газа происходит теплообмен, поскольку поршень теплопроводящий. Согласно рисунку часть 1 газа расширяется, часть 2- сжимается. При таком перемещении поршня возникает поток теплоты справа-налево. Благодаря медленному перемещению поршня, можно считать градиент температуры между поверхностями поршня бесконечно малым, а температуру частей 1 и 2 одинаковой, предположим
|
|
|
1 |
|
2 |
|
|
|
V1 |
S |
F |
|
V2 |
|
0 |
x |
x |
равной T. При этом сила, под действием которой осуществляется перемещение поршня, практически равна F (p2 p1 )S ,
где S – площадь поршня.
В условиях задачи массы и объемы частей газа одинаковы, т.е. 1 2 и V01 V02 V0 . Согласно вышеизложенному и первому началу термодинамики можем написать:
Q Q1 Q2 ( U1 A1) ( U2 A2' )
x
CV T CV T A2' A1 2 CV (T T0) Fdx
0
i R(T T0 ) (p2 |
p1)Sdx . |
(1) |
32 |
|
|
Из уравнений состояния частей газа
p |
RT |
|
RT |
, p |
|
|
|
RT |
|
RT |
|
|
|
|
|
|||||||
1 |
|
V |
( x)S |
|
|
2 |
|
|
V |
( x)S |
|
|
|
|
||||||||
|
1 |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
||
имеем: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
1 |
|
|
|
|
|
|
2 RTx |
|
||||||
(p2 p1)S |
RT |
|
|
|
|
|
|
|
(p2 p1)S |
|
|
|
|
. (2) |
||||||||
|
1 |
|
|
|
2 |
x2 |
||||||||||||||||
|
|
|
|
|
x |
|
|
|
|
|
|
|
||||||||||
Подставляя (2) и (1), получим |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
i(T T ) 2x |
|
Txdx |
. |
|
|
|
|
|
(3) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
0 |
|
|
|
2 x2 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
Интеграл вычислить не удается, поскольку T T(x). Поэтому возьмем дифференциалы от обеих частей равенства (3):
idT 2Txdx/( 2 x2). |
(4) |
При разделении уравнения (4) по переменным, будем иметь:
|
|
|
|
|
|
dT |
|
|
2 |
|
|
|
xdx |
|
, |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
2 |
x2 |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
T |
|
|
|
i |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dT |
1 |
|
|
|
d( |
2 x |
2 ) |
. |
|
|
(5) |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
2 |
x2 |
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
i |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Интегрирование (5) |
дает:T |
|
|
|
|
|
|
c |
|
|
. При x=0 T T0 , от- |
||||||||||||||||||
|
( 2 x2)1/i |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
сюда c T 2/i . Следовательно, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
l2/i |
|
|
|
|
|
|
|
l2 |
|
|
1/i |
|
|
|
|
T0 |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
T T0 |
|
2 |
|
2 1/i T0 |
|
2 |
|
|
|
|
|
|
|
2 |
|
2 1/i |
|||||||||||||
(l |
x |
|
x |
2 |
|
(1 x |
/l |
||||||||||||||||||||||
|
|
|
) |
|
|
l |
|
|
|
|
|
|
|
|
|
) |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
33 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
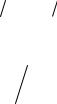
|
|
|
|
|
|
|
|
2 1/i |
|
|
|
|
|
|
|
|
|
||||
|
|
T / 1 |
|
Sx |
|
|
|
T |
1 ( V V )2 |
1/i . |
(6) |
||||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
0 |
|
|
|
|
|
2 |
|
|
0 |
|
|
|
0 |
|
|
|
|
||
|
|
|
|
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
||||
Отношение V /V0 |
найдем из условий |
|
|
|
|
|
|
||||||||||||||
V V |
0 |
V,V |
2 |
V |
0 |
V и V |
V |
|
: |
V |
|
1 |
. (7) |
||||||||
2 |
|
|
|||||||||||||||||||
1 |
|
|
|
|
|
|
|
|
|
|
1 |
|
|
V0 |
1 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Подставляя (7) и (6), получаем: |
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
T T |
( 1)2 |
1/i . |
|
|
(8) |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
0 |
4 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Число степеней свободы молекулы и показатель адиабаты газа находятся в соотношении i 2/( 1). Тогда формулу
(8) можно переписать в виде:
T T |
( 1)2 |
( 1)/2 . |
(9) |
|
|
|
|||
0 |
4 |
|
|
|
|
|
|
|
|
6.40. Левую часть свободного объема цилиндра назовем первой, правую – второй. Длины частей цилиндра при равновесном положении поршня обозначим . При смещении вправо на относительно равновесного положения возникает возвращающая сила F (p2 p1)S , где p1 и p2 - давление газа в левой и правой частях цилиндра. При быстрых колебаниях поршня по обеим сторонам от него периодические процессы сжатия и расширения газа практически являются адиабатическими.
Исходя из этого, напишем выражения давления газа у поверхностей поршня: p1 p0 /( x) , p2 p0 /( x) . При этом возвращающая сила
34

|
|
|
F (p |
2 |
p )S p |
S[(1 x/ ) (1 x/ ) ]. |
|
||
|
|
|
|
1 |
0 |
|
|
|
|
|
При малых колебаниях |
|
|
|
|
||||
|
|
|
F p0S[1 x/ (1 x/ )] 2p0S x/ . |
|
|||||
|
Дифференциальное уравнение |
колебаний поршня |
(без |
||||||
учета |
затухания) |
|
получает |
вид |
|
т.е. |
|||
|
mx (2 p0S / )x 0, |
||||||||
|
|
2 |
/mV0)x 0. Отсюда имеем частоту колебаний |
|
|||||
x (2 p0S |
|
|
|||||||

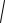 2 p0S2
2 p0S2 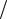 mV0 .
mV0 .
6.41.Левую половину полуцилиндра будем считать первой, правую – второй (см.рисунок 6.1 сборника).
Повернем перегородку вправо на некоторый угол . При
этом объем |
левой части полуцилиндра увеличится на |
V R2h /2 |
(R – радиус поверхности цилиндра), объем пра- |
вой части уменьшится на ту же величину. Если равновесное
давление газа в полуцилиндре |
p0 , то давление газа в частях |
||||||||||||||||
объема будут равны |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
V0 |
|
|
p0 |
|
|
|
|
p0 |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
(1 V V ) |
(1 2 / ) |
, |
|
|
|||||||||||
p1 p0 V V |
|
|
|
||||||||||||||
|
|
0 |
|
|
|
|
0 |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
V0 |
|
|
|
p0 |
|
|
|
|
p0 |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
. |
|||||||||
p2 p0 |
|
|
|
|
|
(1 V /V0 ) |
(1 2 / ) |
||||||||||
|
V0 V |
|
|
|
|
|
|
||||||||||
Здесь V0 R2h/4. Для малого угла |
|
|
|
|
|
|
|
|
|||||||||
|
|
|
1 |
|
|
|
(1 2 / ) |
1 2 / . |
|
|
|
||||||
|
(1 2 /m) |
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
На вертикальную полоску перегородки |
шириной dr и |
||||||||||||||||
высотой h будет действовать результирующая сила |
|
|
|
||||||||||||||
F(p2 p1)dS p0[(1 2 / ) (1 2 / )]hdr
(4 p0h / )dr .
35

Момент силы dF относительно оси поворота
dM rdF (4 p0h / )rdr. Полный возвращающий момент
сил |
давления |
на |
перегородку |
равен |
M dM |
(2 p0h / )R2 . |
Момент инерции |
пластинки |
|
I1 mR2 . Дифференциальное уравнение вращательных коле- 3
баний перегородки получает вид
1 |
2 |
2 |
h/ ) 0 |
|
|
|
|||
3 |
mR (2 p0R |
или (6 p0h/ m) 0. |
||
|
|
|
|
|
Отсюда имеем квадрат частоты 02 6 p0h , а затем показатель
m
адиабаты m 02 /6p0h.
6.42. Согласно первому началу термодинамики напишем:
Q dU A. (1)
Учитывая условия задачи, равенство (1) представим в
виде:
|
|
Q |
R |
dT pdV . |
|||||
|
|
|
|||||||
|
|
|
|
1 |
|
|
|||
Здесь p RT /V RT2 |
/a , dV |
a |
dT . Следовательно, |
||||||
|
|
||||||||
|
|
|
|
|
T 2 |
|
|
||
Q |
R |
|
dT RdT |
(2 )R |
dT . |
||||
|
|
|
|||||||
|
1 |
|
|
|
|
1 |
|||
Отсюда
Q(2 )R T .
1
36

6.43. По условию задачи A dU , где - некоторая
постоянная. |
Далее |
учтем |
|
следующие |
моменты: |
|||||||||||||
A pdV, |
dU |
d(pV) |
. |
|
Тогда |
|
pdV |
|
|
d(pV), или |
||||||||
|
|
|
1 |
|||||||||||||||
|
|
|
|
1 |
|
|
|
|
|
|
|
|
||||||
pdV |
|
|
(Vdp pdV). |
Разделяя |
|
по |
переменным, |
сначала |
||||||||||
1 |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
получим уравнение |
dp |
|
1 |
|
dV |
, |
а затем его |
решение |
||||||||||
|
|
|
||||||||||||||||
|
|
|
|
|
p |
|
|
V |
|
|
|
|
|
|||||
p cV( 1)/ , где c – постоянная интегрирования. Получен-
ный результат перепишем в виде pV( 1 )/ c, введем обо-
значение n ( 1 )/ , и получим соответствующий закон процесса pVn const.
6.44. Политропическим называется процесс, при котором теплоемкость остается постоянной (c = const). Уравнение по-
литропы имеет вид pVn const, где показатель степени n но-
сит название показателя политропы.
Установим связь между c и n. Напишем первое начало
термодинамики для моля газа: |
|
Qм CV dT pdV . |
(1) |
Поделим (1) на dT и учтем, что Qм /dT C - теплоем-
кость газа. Тогда вместо (1) будем иметь C CV p dV , или dT
(C CV )dT pdV . |
(2) |
Из уравнения состояния pV RT получим
dT 1 (pdV Vdp). (3) R
37
Подставим (3) и (2):
C C |
|
|
|
|
C C |
|
|
C C |
|
|||||
V |
(pdV Vdp) pdV |
|
V |
Vdp 1 |
V |
pdV |
||||||||
|
|
R |
R |
|||||||||||
R |
|
|
|
|
|
|
|
|
||||||
|
|
dp |
|
Cp C dV |
|
, или |
|
dp |
|
dV |
, |
(4) |
||
|
|
|
|
|
|
|
p |
V |
||||||
|
p |
C CV V |
|
|||||||||||
|
|
|
|
|
|
|
|
|
||||||
где (Cp C)/(C CV ).
Уравнение (4) дает: |
|
p |
|
|
|
V |
или |
pV |
const. |
Введем |
|||||||||||||
const |
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
обозначение n (C C |
p |
)/(C C ). |
Тогда |
pVn const. |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
V |
|
|
|
|
|
|
|
|
|
||
Итак показатель политропы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
n (C Cp )/(C CV ). |
|
|
|
|
|
|
(5) |
||||||||||||||||
Из равенства (5) можно найти теплоемкость газа: |
|
|
|
||||||||||||||||||||
|
C |
nCV |
Cp |
. |
|
|
|
|
|
|
|
|
|
(6) |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
n 1 |
|
|
|
|
|
|
|
|
|
|||||
Если учесть соотношения C |
|
|
C |
R и C |
|
|
|
|
R |
, |
то выра- |
||||||||||||
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
p |
|
|
V |
|
|
|
|
|
V |
|
1 |
|
||||
жение (6) можно привести к виду |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
C |
|
|
|
|
(n )R |
. |
|
|
|
|
|
|
|
(7) |
||||||||
|
(n 1)( 1) |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
Выражение (6) представим в виде |
|
|
|
|
|
|
|
|
|
||||||||||||||
C C |
V |
|
|
|
|
|
R |
|
|
R |
|
|
R |
|
. |
|
|
|
(8) |
||||
|
n 1 |
1 |
n 1 |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Если положить n , то C 0. На основании (8) можно сделать вывод, что для 1 n теплоемкость c 0.
6.45. Обобщенную молярную теплоемкость газа в произ-
вольном процессе вычислим по формуле C |
(n )R |
|
(n 1)( 1) |
||
|
||
38 |
|
(см.формулу (7) задачи 6.44). Для аргона |
5/3. По уравне- |
|||||||||||||
нию pVn |
const и заданным условиям найдем показатель по- |
|||||||||||||
литропы: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
pV n |
p Vn p / p |
; |
V /V , |
|
||||||||
|
|
1 |
1 |
|
2 |
2 |
|
1 |
2 |
|
2 |
1 |
. |
|
|
|
p / p |
|
n n ln /ln |
||||||||||
|
|
2 |
|
|||||||||||
|
|
1 |
|
|
|
|
|
|
|
|
|
|
||
Для 4 и |
8 показатель |
|
n 3/2. Располагая зна- |
|||||||||||
чениями |
и n получим: |
|
|
|
|
|
|
|
|
|||||
C |
(3/2 5/3)R |
|
R/2 |
4,15Дж / К моль . |
||||||||||
(3/2 1)(5/3 1) |
||||||||||||||
|
|
|
|
|
|
|
|
|||||||
6.46. |
|
С |
помощью |
уравнения |
состояния газа |
|||||||||
pV RT |
( 1) |
уравнение |
политропического процесса |
|||||||||||
представим в виде |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
TV n 1 |
const. |
|
(1) |
||||||
Удовлетворив имеющимся условиям, на основании (1)
получим T2 T1(V1 /V2 )n 1(2). Работа, совершенная газом в хо-
де политропического процесса, равна
A12 |
|
p1V1 |
1 (V1 |
/V2 )n 1 |
p1V1 |
|
(1 T2 /T1) |
p1V1 T |
|
R T |
. |
|||||
|
|
|
|
|||||||||||||
|
|
n 1 |
|
|
n 1 |
(n 1)T |
|
n 1 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
Для |
заданных |
значений |
T 26К и |
n 1,50 |
работа |
|||||||||||
A12 0,43кДж . |
Количество |
полученного |
газа тепла |
|
равна |
|||||||||||
|
|
|
|
n |
|
|
|
|
|
|
|
|
||||
Q C T |
|
|
|
R T . Для аргона |
5/3, тогда |
|||||||||||
|
|
|
||||||||||||||
|
|
|
|
(n 1)( 1) |
|
|
|
|
|
|
|
|
||||
|
|
|
|
Q |
|
1,5 5/3 |
|
|
8,31( 26) 0,11кДж . |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
(1,5 1)(5/3 1) |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
39 |
|
|
|
|
|
||
6.47. В законе расширения газа p V заменим давле-
ние p на vRT/V и получим
|
|
|
|
|
|
|
|
V 2 |
RT . |
|
|
|
|
|
|
(1) |
||||||||||
Перейдем в (1) к дифференциалам: 2 VdV RdT. От- |
||||||||||||||||||||||||||
сюда имеем |
dT |
2 V |
dV . Элементарное приращение внут- |
|||||||||||||||||||||||
|
||||||||||||||||||||||||||
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ренней энергии dU C |
dT |
i |
R |
2 V |
dV i VdV , т.е. |
|||||||||||||||||||||
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
V |
|
|
|
|
|
|
2 |
|
|
|
R |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
dU i VdV . |
|
|
|
|
|
|
(2) |
|||||||||||
Интегрируя (2), получим: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
U U |
2 |
U |
1 |
|
|
i V2 |
|
V |
|
i |
|
(V |
2 V2) |
|
|||||||||
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
2 |
|
2 |
|
|
0 |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
V |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
||||
|
i |
V2(V2 V2 1) |
i |
V 2 |
( 2 1) ( 2 1)V2 /( 1), |
|||||||||||||||||||||
2 |
0 |
0 |
|
|
|
2 |
|
|
0 |
|
|
|
|
|
|
|
|
|
|
0 |
|
|||||
поскольку i 2 ( 1). |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Совершенная газом работа |
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
V1 |
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
||
A |
pdV VdV |
|
V0 |
2 (V12 /V02 |
1) |
V02 ( 2 |
1). |
|||||||||||||||||||
2 |
|
|||||||||||||||||||||||||
|
(0 1) |
V0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Далее |
обратимся |
|
|
|
|
к |
|
|
|
первому |
началу |
|||||||||||||||
Q CV dT pdV CV dT VdV |
и |
|
учтем соотношения: |
|||||||||||||||||||||||
pV RT V 2 RT 2 VdV RdT VdV RdT /2.
Тогда
Q CV dT Rdt/2. |
(3) |
40
