
- •Предмет, содержание, задачи токсикологической химии.
- •Краткий исторический очерк развития токсикологической химии.
- •Связь токсикологической химии с другими химическими, фармацевтическими и биологическими науками.
- •Вклад отечественных учёных в развитие токсикологической химии.
- •Организация судебно-медицинской и химико-токсикологической (судебно-химической) экспертизы в России.
- •Объекты химико-токсикологического исследования и вопросы, решаемые химико-токсикологическим анализом. Понятие «яд», «ядовитое вещество». Классификация ядов и отравлений.
- •Специфические особенности химико-токсикологического анализа.
- •Пути поступления чужеродных соединений в организм. Основные факторы, оказывающие влияние на всасываемость и распределение веществ в тканях и биологических средах организма.
- •Превращение и выделение чужеродных веществ из организма. Общая характеристика.
- •Общая характеристика методов исследования, применяемых в токсикологической химии (методы изолирования, очистки, качественного и количественного анализа).
- •11. Судебная химия – основной раздел токсикологической химии.
- •Документация химико-токсикологических экспертиз и правила её
- •Источники ошибок на основных этапах химико-токсикологического анализа.
- •Правила приёма вещественных (химических) доказательств на экспертизу.
- •Значение данных дознания, истории болезни и результатов судебно-медицинского исследования трупов для судебно-химической экспертизы.
- •Микрокристаллоскопия и кристаллооптика в токсикологической химии.
- •Методы количественного определения. Значение этих определений для оценки результатов исследования (показать на примере «металлических ядов»).
- •Реакции отрицательного судебно-химического значения.
- •Классификация ядовитых и сильнодействующих веществ в токсикологической химии.
- •Охрана окружающей среды и перспективы развития токсикологической химии на современном этапе.
- •Классификация наркотических и психотропных веществ. Основные особенности их химико-токсикологического анализа.
- •Современные физико-химические методы, применяемые в анализе наркотических и психотропных веществ. Основные требования к ним.
- •Фармакокинетика, метаболизм, особенности химико-токсикологического анализа опиатов.
- •Фармакокинетика, метаболизм, особенности химико-токсикологического анализа каннабиноидов.
- •Перспективы развития и совершенствования методов судебно-химических исследований вещественных доказательств.
- •26. Теоретические основы изолирования ядовитых и сильнодействующих веществ из биологического материала дистилляцией водяным паром.
- •27.Синильная кислота. Качественное обнаружение и количественное определение.
- •28. Химико-токсикологическое значение синильной кислоты и её производных.
- •29. Ядовитые галогенпроизводные (хлороформ, хлоралгидрат). Изолирование.
- •30. Ядовитые галогенпроизводные (четыреххлористый углерод, 1,2-дихлорэтан).
- •31. Альдегиды (формалин, формальдегид). Изолирование, качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •32. Ацетон. Изолирование, качественное обнаружение и количественное
- •33. Метиловый спирт. Изолирование, качественное обнаружение и количественное
- •34. Этиловый спирт. Изолирование. Качественное обнаружение и количественное
- •35. Физико-химические методы количественного определения этилового спирта, применение в судебно-химическом анализе.
- •36. Значение этапа количественного определения этилового спирта при химико-токсикологическом исследовании биологических объектов.
- •37. Реакции отличия метилового и этилового спирта. Методы экспресс-анализа спирта. Пробы Раппопорта и Шинкаренко.
- •38.Спирты (амиловый, этиленгликоль). Качественное обнаружение. Токсикологическое значение. Метаболизм.
- •39. Уксусная кислота. Изолирование. Качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •40. Нитробензол в химико-токсикологическом отношении.
- •41. Фенолы (фенол, трикрезол) в химико-токсикологическом отношении.
- •42. Анилин в химико-токсикологическом отношении.
- •43. Метод изолирования подкисленным спиртом. Его достоинства и недостатки.
- •44. Метод изолирования подкисленной водой. Вклад отечественных учёных в разработку этого метода, его достоинства и недостатки.
- •45. Частный метод изолирования подкисленной водой в.Ф. Крамаренко. Влияние рН среды и др. Факторов на изолирование и экстрагирование алкалоидов.
- •46. Метод изолирования подщелоченной водой, его достоинства и недостатки.
- •47. Салициловая кислота. Изолирование, качественное обнаружение и количественное обнаружение. Токсикологическое значение и метаболизм.
- •48. Химико-токсикологическое значение производных барбитуровой кислоты. Методы изолирования, очистки барбитуратов.
- •49. Качественное обнаружение барбитуратов в судебно-химическом анализе.
- •50. Количественное определение барбитуратов в судебно-химическом анализе.
- •51. Спектрофотометрическое определение производных барбитуровой кислоты в химико-токсикологическом анализе.
- •52. Токсикологическое значение и метаболизм барбитуратов.
- •53. Фенацетин. Качественное обнаружение и количественное определение.
- •54. Предварительные химико-токсикологические исследования при наличии алкалоидов (общеалкалоидные реакции).
- •55. Методы изолирования, очистки и обнаружение алкалоидов.
- •56. Алкалоиды, производные пиридина и пиперидина (кониин, ареколин). Изолирование, качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •57. Алкалоиды, производные пиридина и пиперидина (никотин, анабазин) в химико-токсикологическом отношении.
- •58. Пахикарпин в химико-токсикологическом отношении.
- •59. Алкалоиды, производные тропана (атропин, гиосциамин) в химико-токсикологическом отношении.
- •60. Алкалоиды, производные тропана (кокаин) в химико-токсикологическом отношении.
- •61. Производные аминокислот ароматического ряда (новокаин, дикаин) в химико-токсикологическом отношении.
- •62. Алкалоиды, производные хинолина (хинин и его соли). Изолирование, качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •63. Алкалоиды, производные изохинолина (морфин). Изолирование. Качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •64. Заменители морфина (кодеин, этилморфина гидрохлорид, апоморфин) в химико-токсикологическом отношении.
- •65. Доказательства отравления опием.
- •66. Алкалоиды, производные бензилизохинолина (папаверин, наркотин) в химико-токсикологическом отношении.
- •67. Алкалоиды, производные индола (резерпин, секуренин) в химико-токсикологическом отношении.
- •69. Алкалоиды, производные пирролизидина (платифиллин) в химико-токсикологическом отношении.
- •70. Алкалоиды, производные пиримидина (кофеин, теобромин, теофиллин) в химико-токсикологическом отношении.
- •71. Ациклические алкалоиды (эфедрин). Изолирование, обнаружение, определение, значение, метаболизм.
- •72. Производные пиразола (антипирин, амидопирин) в химико-токсикологическом отношении.
- •73. Производные 1,4 - бензодиазепина в химико-токсикологическом отношении.
- •74. Производные фенотиазина в химико-токсикологическом отношении.
- •75. Общая характеристика пестицидов (ядохимикатов) в химико-токсикологическом отношении. Классификация.
- •76. Пестициды из группы галогенпроизводных (ддт, гхцг, гептахлор) в химико-токсикологическом отношении.
- •77. Пестициды из класса фенолов (днок, диносеб, зоокумарин). Качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •78. Пестициды класса фосфорорганических соединений (хлорофос, карбофос) в химико-токсикологическом отношении.
- •79. Пестициды, производные карбаминовой кислоты (севин) в химико-токсикологическом отношении.
- •80. Пестициды, производные тиокарбаминовой, дитиокарбаминовой кислот (крысид, тмтд) в химико-токсикологическом отношении.
- •81. Металлоорганические пестициды (гранозан, меркуран, меркургексан) в химико-токсикологическом отношении.
- •82. Неорганические ядохимикаты (фосфид цинка, фторид натрия) в химико-токсикологическом отношении.
- •83. Общая характеристика сероводородного и дробного методов анализа «металлических» ядов.
- •84. Вклад отечественных учёных в разработку химико-токсикологического анализа «металлических ядов».
- •85. Теоретические и методологические основы дробного метода анализа «металлических» ядов, разработанные а.Н. Крыловой.
- •86. Органические реагенты, предложенные а.Н. Крыловой для анализа «металлических» ядов дробным методом.
- •87. Последовательность проведения дробного метода анализа на «металлические» яды.
- •88. Частые методы минерализации органических веществ.
- •89. Минерализация серной и азотной кислотами органических веществ. Достоинства и недостатки.
- •90. Минерализация органических веществ азотной, серной, хлорной кислотами. Достоинства и недостатки метода.
- •91. Методы удаления окислителей из минерализата.
- •92. Исследование осадка после минерализации азотной, серной кислотами (свинец, барий).
- •93. Свинец и тетраэтилсвинец. Качественное обнаружение и количественное определение. Токсикологическое значение.
- •94. Барий в химико-токсикологическом отношении.
- •95. Марганец в химико-токсикологическом отношении.
- •96. Хром в химико-токсикологическом отношении.
- •97. Серебро. Изолирование, качественное обнаружение и количественное определение, поступление, распределение, выведение из организма, токсикологическое значение.
- •98. Медь в химико-токсикологическом отношении.
- •99. Висмут в химико-токсикологическом отношении.
- •100. Сурьма и таллий в химико-токсикологическом отношении.
- •101. Кадмий в химико-токсикологическом отношении.
- •102. Цинк в химико-токсикологическом отношении.
- •103. Ртуть, деструктивные методы изолирования. Качественное и количественное значение. Органические препараты ртути (этилмеркурхлорид).
- •104. Мышьяк в химико-токсикологическом отношении. Общая схема анализа.
- •105. Определение мышьяка в аппарате Марша.
- •106. Определение мышьяка в аппарате Зангер-Блека.
- •107. Изолирование веществ из биологического материала диализом (серная, азотная, соляная кислоты). Качественное обнаружение и количественное определение, токсикологическое значение.
- •108. Изолирование веществ из биологического материала диализом (аммиак, едкий натр, щелочные соли). Качественное обнаружение и количественное определение, токсикологическое значение.
64. Заменители морфина (кодеин, этилморфина гидрохлорид, апоморфин) в химико-токсикологическом отношении.
Кодеин
Кодеин представляет собой монометиловый эфир морфина. Он является одним из алкалоидов опия. В опии, полученном из снотворного мака, содержится 0,2—2 % кодеина. В отдельных сортах индийского опия содержится около 6 % кодеина. Кодеин является сильным основанием, которое не осаждается аммиаком. Основание кодеина растворяется в холодной (1 : 120) и кипящей воде (1 :20), диэтиловом эфире (1 : 50), хлороформе (1:2) и этиловом спирте (1:2). Гидрохлорид кодеина слабо растворяется в хлороформе (1 : 800), лучше —в этиловом спирте (1:100) и воде (1 : 30). Фосфат кодеина плохо растворяется в этиловом спирте (1 : 450), диэтиловом эфире и хлороформе, лучше — в воде (1 :4), сульфат кодеина плохо растворяется в этиловом спирте (1:1300), диэтиловом эфире и хлороформе, лучше — в воде (1:30).
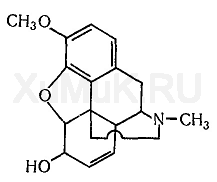
Кодеин экстрагируется органическими растворителями из подщелоченных водных вытяжек. Максимальные количества кодеина экстрагируются хлороформом при рН = 8,0...3,5.
Применение. Действие на организм. Кодеин применяется в медицине в виде основания и фосфата. По действию на организм кодеин близок к морфину. Однако болеутоляющее свойство кодеина выражено слабее, чем у морфина. Кодеин в меньшей степени, чем морфин, угнетает дыхание. Кодеин уменьшает возбудимость кашлевого центра, и поэтому назначается для успокоения кашля, в сочетании с анальгином, амидопирином, кофеином, фенобарбиталом и другими препаратами применяется при головных болях, невралгиях и т. д. Кодеин менее токсичен, чем морфин. Однако при частом, повторяющемся приеме кодеина возможно привыкание к нему.
Метаболизм. Кодеин подвергается метаболизму тремя путями. Часть кодеина связывается с глюкуроновой кислотой и выделяется из организма с мочой в виде глюкуронида. Некоторое количество кодеина подвергается О-деметилированию (образуется морфин) и N-деметилированию (образуется норкодеин). Образовавшиеся метаболиты (морфин и норкодеин) выделяется с мочой в виде глюкуронидов. Незначительная часть кодеина выделяется с мочой в несвязанном виде. Через 6 ч после поступления кодеина в кровь из организма выделяется около двух третих дозы этого алкалоида, а через 24 ч он почти полностью исчезает из организма.
Обнаружение кодеина
Предварительная проба на наличие кодеина в моче. В делительную воронку вносят 50 мл мочи, подщелачивают раствором аммиака до рН=10, прибавляют 50 мл хлороформа и взбалтывают в течение 5 мин. Хлороформную вытяжку отделяют от водной фазы, вытяжку взбалтывают с 3 мл воды в течение 3 мин. Водную фазу отделяют от хлороформа, фильтруют через безводный сульфат натрия и выпаривают досуха. Сухой остаток растворяют в 1 мл этилового спирта. Полученный спиртовой раствор используют для обнаружения кодеина одним из следующих способов:
а) на фильтровальную бумагу наносят каплю полученного спиртового раствора и прибавляют каплю реактива Марки. При наличии кодеина пятно приобретает красноватую окраску, переходящую в сине-фиолетовую;
б) на фильтровальную бумагу наносят каплю указанного выше спиртового раствора и прибавляют каплю 0,5%-го раствора ванадата аммония и каплю 2 %-го раствора серной кислоты. При наличии кодеина появляется зеленая окраска, переходящая в синюю.
Для подтверждения результатов указанных реакций необходимо призвести обнаружение кодеина в вытяжке методом хроматографии в тонком слое сорбента.
Реакция с реактивами группового осаждения алкалоидов. При взаимодействии кодеина с реактивами Драгендорфа, Бушарда, Майера и другими образуются осадки.
Цветные реакции. Кодеин с реактивами Манделина, Марки и Фреде дает окрашенные продукты реакции, которые описаны выше.
Реакция Пеллагри. При нагревании кодеина с концентрированной соляной кислотой, а затем с концентрированной серной кислотой происходит деметоксилирование этого алкалоида и образуется апоморфин, который дает реакцию со спиртовым раствором иода. Выполнение реакции Пеллагри описано выше.
Обнаружение кодеина методом хроматографии. На линию старта на хроматографической пластинке наносят каплю хлороформного раствора исследуемого вещества. Правее на расстоянии 2 см на линию старта наносят каплю раствора «свидетеля» (0,01 %-й раствор кодеина). Пятна нанесенных растворов подсушивают на воздухе, а затем пластинку вносят в камеру для хроматографирования, насыщенную парами растворителей (хлороформ-ацетон-диэтиламин в соотношении 50 : 30 : 2). После продвижения системы растворителей на 10 см выше линии старта пластинку вынимают из камеры, подсушивают на воздухе и опрыскивают реактивом Драгендорфа, модифицированным по Мунье.
При наличии кодеина в исследуемом растворе пятна этого алкалоида приобретают буровато-розовую окраску (Rf = 0,40± ±0,02).
Обнаружение кодеина по УФ- и ИК-спектрам. Основание кодеина в растворе этилового спирта имеет максимум поглощения при 286 нм; в ИК-области спектра основание кодеина (диск с бромидом калия) имеет основные пики при 1052 1268, 1500 см -1.
Способы идентификации, позволяющие отличить кодеин от морфина. Ввиду того что морфин и кодеин являются близкими по строению алкалоидами, они дают ряд реакций с одними и теми же реактивами. Однако кодеин не дает реакций с хлоридом железа (III), с НIO 3, с гексацианоферратом (III) калия и хлоридом железа (III), которые дает морфин. Кодеин можно отличить от морфина и по светопоглощению в ИК-области спектра.
Кодеин отличается от морфина и тем, что морфин не экстрагируется диэтиловым эфиром из щелочных растворов (образуется морфинат). Это свойство указанных алкалоидов используется для разделения их в ходе анализа.
Экстракционно-фотоколориметрический метод определения кодеина
Метод фотоколориметрического определения кодеина основан на реакции с тропеолином 00, при которой образуется ионный ассоциат, экстрагирующийся хлороформом:
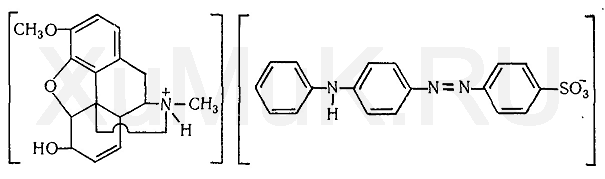
Техника определения. 1 мл исследуемого раствора вносят в делительную воронку, прибавляют 9 мл ацетатной буферной смеси (рН = 4,6), 5 мл 0,1 %-го водного раствора тропеолина 00 и 5 мл хлороформа. Содержимое делительной воронки взбалтывают в течение 5 мин. Через 3 мин от водного слоя отделяют хлороформную вытяжку. Водный слой взбалтывают с новыми порциями хлороформа (по 5 мл) до тех пор, пока 3—4 капли последней хлороформной вытяжки не перестанут давать окраску с 1—2 каплями 1 %-го раствора концентрированной серной кислоты в метиловом спирте. Хлороформные вытяжки соединяют и доводят хлороформом до 50 мл. К 5 мл полученного хлороформного раствора прибавляют 20 мл хлороформа и 2,5 мл 1 %-го раствора концентрированной серной кислоты в метиловом спирте. Затем измеряют оптическую плотность полученного фиолетово-красного раствора с помощью фотоэлектроколориметра ФЭК-М (светофильтр зеленый, кювета 10 мм). В качестве раствора сравнения берут хлороформную вытяжку из смеси, совтоящей из 5 мл 0,1 %-го раствора тропеолина 00, 9 мл ацетатной буферной смеси (рН = 4,6) и 1 мл воды. К полученной хлороформной вытяжке прибавляют 2,5 мл 1 %-го раствора концентрированной серной кислоты в метиловом спирте.
Расчет содержания кодеина в пробе производят по калибровочному графику. Для построения калибровочного графика берут делительные воронки, в которые вносят по 0,1; 0,2; 0,4; 0,6; 0,8 и 1 мл стандартного раствора (в 1 мл содержится 2 мг фосфата кодеина). В первые 5 делительных воронок прибавляют воду до 1 мл. Затем во все делительные воронки вносят по 9 мл ацетатной буферной смеси (рН = 4,6), по 5 мл 0,1 %-го раствора тропеолина 00 и поступают, как указано выше.
С помощью этого метода можно определить от 0,2 до 2,0 мг кодеина в пробе.
Этилморфина гидрохлорид
Апоморфин
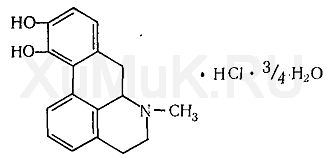
Апоморфин получают при нагревании морфина с концентрированной соляной кислотой. Апоморфин выпускается промышленностью в виде гидрохлорида, который представляет собой белый или слегка желтоватый кристаллический порошок без запаха. На воздухе и на свету апоморфин зеленеет. Под влиянием света и воздуха растворы апоморфина также зеленеют и теряют фармакологическую активность. Основание апоморфина растворяется в этиловом спирте и хлороформе, слабо растворяется в воде и диэтиловом эфире. Гидрохлорид апоморфина растворяется в воде (1 : 50) и этиловом спирте (1 :50), трудно растворяется в диэтиловом эфире и хлороформе.
Апоморфин экстрагируется органическими растворителями из кислых и щелочных водных растворов.
Применение. Действие на организм. Апоморфин применяется в медицине как рвотное средство для быстрого удаления из желудка ядовитых веществ и недоброкачественной пищи. Апоморфин вызывает рвоту через несколько минут после введения его под кожу. Он редко применяется как отхаркивающее средство. Его применяют для того, чтобы вызвать отвращение к алкоголю при лечении хронических алкоголиков.
Метаболизм. Апоморфин выводится из организма с мочой в виде глюкуронида. Небольшие количества апоморфина выводятся из организма в неизмененном виде.
Обнаружение апоморфина
Для обнаружения апоморфина, выделенного из биологического материала, применяют цветные реакции, а также методы УФ- и ИК-спектроскопии.
Реакция Пеллагри. В сухую пробирку вносят 5—б капель хлороформного раствора исследуемого вещества (или хлороформной вытяжки), который выпаривают при комнатной температуре. Сухой остаток растворяют в 0,5 мл воды и прибавляют 3—4 капли 10 %-го раствора карбоната натрия. Затем в пробирку (по каплям) вносят 5—6 капель спиртового раствора иода. Появление зеленой окраски указывает на наличие апоморфина в хлороформном растворе. Если к раствору, имеющему зеленую окраску, прибавить 0,5—1,0 мл диэтилового эфира и взболтать, то водный слой сохраняет эту окраску, а эфирный слой приобретает пурпурно-красную.
Реакция с концентрированной азотной кислотой:
а) несколько капель хлороформной вытяжки вносят в фарфоровую чашку и выпаривают досуха. К сухому остатку прибавляют 2 капли концентрированной азотной кислоты. Появление фиолетовой окраски, переходящей в красно-бурую, указывает на наличие апоморфина;
б) к сухому остатку прибавляют 2—3 капли концентрированной серной кислоты, а затем каплю концентрированной азотной кислоты. При наличии апоморфина появляется фиолетовая окраска, переходящая в кроваво-красную, а затем в желтовато-красную.
Реакция с реактивом Фреде. 3—5 капель хлороформной вытяжки помещают в маленькую фарфоровую чашку или в углубление на фарфоровой пластинке. После испарения вытяжки при комнатной температуре на сухой остаток наносят каплю реактива Фреде. При наличии апоморфина появляется грязно-зеленая окраска.
Реакция с реактивом Марки. Реакцию выполняют так же, как и реакцию с реактивом Фреде. При наличии апоморфина в хлороформной вытяжке появляется фиолетовая окраска, быстро переходящая в грязно-зеленую.
Реакция с хлоридом железа (III). Несколько капель хлороформной вытяжки вносят в пробирку и выпаривают досуха. Сухой остаток растворяют в 3—5 каплях разбавленной соляной кислоты, раствор выпаривают на водяной бане досуха. Сухой остаток растворяют в 3—5 каплях воды и к раствору прибавляют каплю 0,1 %-го раствора хлорида железа (III). При наличии апоморфина появляется синяя окраска. В зависимости от количества апоморфина может появиться розово-красная окраска, переходящая в фиолетовую, а затем в черную.
Обнаружение апоморфина по УФ- и ИК-спектрам. Апоморфин в 0,1 н. растворе серной кислоты имеет максимум поглощения при 273 нм и изгиб при 305 нм; в ИК-области основание апоморфина (диск с бромидом калия) имеет основные пики при 1265, 1460, 752 и 985 см -1.
