
- •Предмет, содержание, задачи токсикологической химии.
- •Краткий исторический очерк развития токсикологической химии.
- •Связь токсикологической химии с другими химическими, фармацевтическими и биологическими науками.
- •Вклад отечественных учёных в развитие токсикологической химии.
- •Организация судебно-медицинской и химико-токсикологической (судебно-химической) экспертизы в России.
- •Объекты химико-токсикологического исследования и вопросы, решаемые химико-токсикологическим анализом. Понятие «яд», «ядовитое вещество». Классификация ядов и отравлений.
- •Специфические особенности химико-токсикологического анализа.
- •Пути поступления чужеродных соединений в организм. Основные факторы, оказывающие влияние на всасываемость и распределение веществ в тканях и биологических средах организма.
- •Превращение и выделение чужеродных веществ из организма. Общая характеристика.
- •Общая характеристика методов исследования, применяемых в токсикологической химии (методы изолирования, очистки, качественного и количественного анализа).
- •11. Судебная химия – основной раздел токсикологической химии.
- •Документация химико-токсикологических экспертиз и правила её
- •Источники ошибок на основных этапах химико-токсикологического анализа.
- •Правила приёма вещественных (химических) доказательств на экспертизу.
- •Значение данных дознания, истории болезни и результатов судебно-медицинского исследования трупов для судебно-химической экспертизы.
- •Микрокристаллоскопия и кристаллооптика в токсикологической химии.
- •Методы количественного определения. Значение этих определений для оценки результатов исследования (показать на примере «металлических ядов»).
- •Реакции отрицательного судебно-химического значения.
- •Классификация ядовитых и сильнодействующих веществ в токсикологической химии.
- •Охрана окружающей среды и перспективы развития токсикологической химии на современном этапе.
- •Классификация наркотических и психотропных веществ. Основные особенности их химико-токсикологического анализа.
- •Современные физико-химические методы, применяемые в анализе наркотических и психотропных веществ. Основные требования к ним.
- •Фармакокинетика, метаболизм, особенности химико-токсикологического анализа опиатов.
- •Фармакокинетика, метаболизм, особенности химико-токсикологического анализа каннабиноидов.
- •Перспективы развития и совершенствования методов судебно-химических исследований вещественных доказательств.
- •26. Теоретические основы изолирования ядовитых и сильнодействующих веществ из биологического материала дистилляцией водяным паром.
- •27.Синильная кислота. Качественное обнаружение и количественное определение.
- •28. Химико-токсикологическое значение синильной кислоты и её производных.
- •29. Ядовитые галогенпроизводные (хлороформ, хлоралгидрат). Изолирование.
- •30. Ядовитые галогенпроизводные (четыреххлористый углерод, 1,2-дихлорэтан).
- •31. Альдегиды (формалин, формальдегид). Изолирование, качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •32. Ацетон. Изолирование, качественное обнаружение и количественное
- •33. Метиловый спирт. Изолирование, качественное обнаружение и количественное
- •34. Этиловый спирт. Изолирование. Качественное обнаружение и количественное
- •35. Физико-химические методы количественного определения этилового спирта, применение в судебно-химическом анализе.
- •36. Значение этапа количественного определения этилового спирта при химико-токсикологическом исследовании биологических объектов.
- •37. Реакции отличия метилового и этилового спирта. Методы экспресс-анализа спирта. Пробы Раппопорта и Шинкаренко.
- •38.Спирты (амиловый, этиленгликоль). Качественное обнаружение. Токсикологическое значение. Метаболизм.
- •39. Уксусная кислота. Изолирование. Качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •40. Нитробензол в химико-токсикологическом отношении.
- •41. Фенолы (фенол, трикрезол) в химико-токсикологическом отношении.
- •42. Анилин в химико-токсикологическом отношении.
- •43. Метод изолирования подкисленным спиртом. Его достоинства и недостатки.
- •44. Метод изолирования подкисленной водой. Вклад отечественных учёных в разработку этого метода, его достоинства и недостатки.
- •45. Частный метод изолирования подкисленной водой в.Ф. Крамаренко. Влияние рН среды и др. Факторов на изолирование и экстрагирование алкалоидов.
- •46. Метод изолирования подщелоченной водой, его достоинства и недостатки.
- •47. Салициловая кислота. Изолирование, качественное обнаружение и количественное обнаружение. Токсикологическое значение и метаболизм.
- •48. Химико-токсикологическое значение производных барбитуровой кислоты. Методы изолирования, очистки барбитуратов.
- •49. Качественное обнаружение барбитуратов в судебно-химическом анализе.
- •50. Количественное определение барбитуратов в судебно-химическом анализе.
- •51. Спектрофотометрическое определение производных барбитуровой кислоты в химико-токсикологическом анализе.
- •52. Токсикологическое значение и метаболизм барбитуратов.
- •53. Фенацетин. Качественное обнаружение и количественное определение.
- •54. Предварительные химико-токсикологические исследования при наличии алкалоидов (общеалкалоидные реакции).
- •55. Методы изолирования, очистки и обнаружение алкалоидов.
- •56. Алкалоиды, производные пиридина и пиперидина (кониин, ареколин). Изолирование, качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •57. Алкалоиды, производные пиридина и пиперидина (никотин, анабазин) в химико-токсикологическом отношении.
- •58. Пахикарпин в химико-токсикологическом отношении.
- •59. Алкалоиды, производные тропана (атропин, гиосциамин) в химико-токсикологическом отношении.
- •60. Алкалоиды, производные тропана (кокаин) в химико-токсикологическом отношении.
- •61. Производные аминокислот ароматического ряда (новокаин, дикаин) в химико-токсикологическом отношении.
- •62. Алкалоиды, производные хинолина (хинин и его соли). Изолирование, качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •63. Алкалоиды, производные изохинолина (морфин). Изолирование. Качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •64. Заменители морфина (кодеин, этилморфина гидрохлорид, апоморфин) в химико-токсикологическом отношении.
- •65. Доказательства отравления опием.
- •66. Алкалоиды, производные бензилизохинолина (папаверин, наркотин) в химико-токсикологическом отношении.
- •67. Алкалоиды, производные индола (резерпин, секуренин) в химико-токсикологическом отношении.
- •69. Алкалоиды, производные пирролизидина (платифиллин) в химико-токсикологическом отношении.
- •70. Алкалоиды, производные пиримидина (кофеин, теобромин, теофиллин) в химико-токсикологическом отношении.
- •71. Ациклические алкалоиды (эфедрин). Изолирование, обнаружение, определение, значение, метаболизм.
- •72. Производные пиразола (антипирин, амидопирин) в химико-токсикологическом отношении.
- •73. Производные 1,4 - бензодиазепина в химико-токсикологическом отношении.
- •74. Производные фенотиазина в химико-токсикологическом отношении.
- •75. Общая характеристика пестицидов (ядохимикатов) в химико-токсикологическом отношении. Классификация.
- •76. Пестициды из группы галогенпроизводных (ддт, гхцг, гептахлор) в химико-токсикологическом отношении.
- •77. Пестициды из класса фенолов (днок, диносеб, зоокумарин). Качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •78. Пестициды класса фосфорорганических соединений (хлорофос, карбофос) в химико-токсикологическом отношении.
- •79. Пестициды, производные карбаминовой кислоты (севин) в химико-токсикологическом отношении.
- •80. Пестициды, производные тиокарбаминовой, дитиокарбаминовой кислот (крысид, тмтд) в химико-токсикологическом отношении.
- •81. Металлоорганические пестициды (гранозан, меркуран, меркургексан) в химико-токсикологическом отношении.
- •82. Неорганические ядохимикаты (фосфид цинка, фторид натрия) в химико-токсикологическом отношении.
- •83. Общая характеристика сероводородного и дробного методов анализа «металлических» ядов.
- •84. Вклад отечественных учёных в разработку химико-токсикологического анализа «металлических ядов».
- •85. Теоретические и методологические основы дробного метода анализа «металлических» ядов, разработанные а.Н. Крыловой.
- •86. Органические реагенты, предложенные а.Н. Крыловой для анализа «металлических» ядов дробным методом.
- •87. Последовательность проведения дробного метода анализа на «металлические» яды.
- •88. Частые методы минерализации органических веществ.
- •89. Минерализация серной и азотной кислотами органических веществ. Достоинства и недостатки.
- •90. Минерализация органических веществ азотной, серной, хлорной кислотами. Достоинства и недостатки метода.
- •91. Методы удаления окислителей из минерализата.
- •92. Исследование осадка после минерализации азотной, серной кислотами (свинец, барий).
- •93. Свинец и тетраэтилсвинец. Качественное обнаружение и количественное определение. Токсикологическое значение.
- •94. Барий в химико-токсикологическом отношении.
- •95. Марганец в химико-токсикологическом отношении.
- •96. Хром в химико-токсикологическом отношении.
- •97. Серебро. Изолирование, качественное обнаружение и количественное определение, поступление, распределение, выведение из организма, токсикологическое значение.
- •98. Медь в химико-токсикологическом отношении.
- •99. Висмут в химико-токсикологическом отношении.
- •100. Сурьма и таллий в химико-токсикологическом отношении.
- •101. Кадмий в химико-токсикологическом отношении.
- •102. Цинк в химико-токсикологическом отношении.
- •103. Ртуть, деструктивные методы изолирования. Качественное и количественное значение. Органические препараты ртути (этилмеркурхлорид).
- •104. Мышьяк в химико-токсикологическом отношении. Общая схема анализа.
- •105. Определение мышьяка в аппарате Марша.
- •106. Определение мышьяка в аппарате Зангер-Блека.
- •107. Изолирование веществ из биологического материала диализом (серная, азотная, соляная кислоты). Качественное обнаружение и количественное определение, токсикологическое значение.
- •108. Изолирование веществ из биологического материала диализом (аммиак, едкий натр, щелочные соли). Качественное обнаружение и количественное определение, токсикологическое значение.
35. Физико-химические методы количественного определения этилового спирта, применение в судебно-химическом анализе.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ СПИРТОВ
Количественное определение спиртов базируется на их общих реакциях: окислении до альдегидов и образовании сложных эфиров.
Из всех спиртов, имеющих токсикологическое значение, только этиловый подлежит обязательному количественному определению при судебно-химических исследованиях.
Это обусловлено следующими причинами:
• чрезвычайно широкое распространение и особое токсикологическое значение этанола, о чем уже говорилось,
• возможность естественного образования этанола в организме, а именно: при брожении и гниении сахаристых веществ в желудке, при бактериальном распаде белковых веществ, при метаболическом превращении высших спиртов.
В судебно-химической практике для количественного определения этанола используют методы, основанные на окислении его до ацетальдегида и образовании сложного эфира с азотистой кислотой - этилнитрита. Известно много методов, в том числе химических, но в настоящее время наибольшее значение приобрели наиболее чувствительные и точные современные методы - биохимический и инструментальный (метод ГЖХ). На их рассмотрении мы и остановимся.
Метод биохимический (энзимный, ферментативный, метод АДГ) был разработан в 1951г. Бюхером и Родецки и применяется, в основном, в зарубежных лабораториях. Метод основан на реакции окисления этанола до ацетальдегида под действием фермента алкогольдегидрогеназы (АДГ).
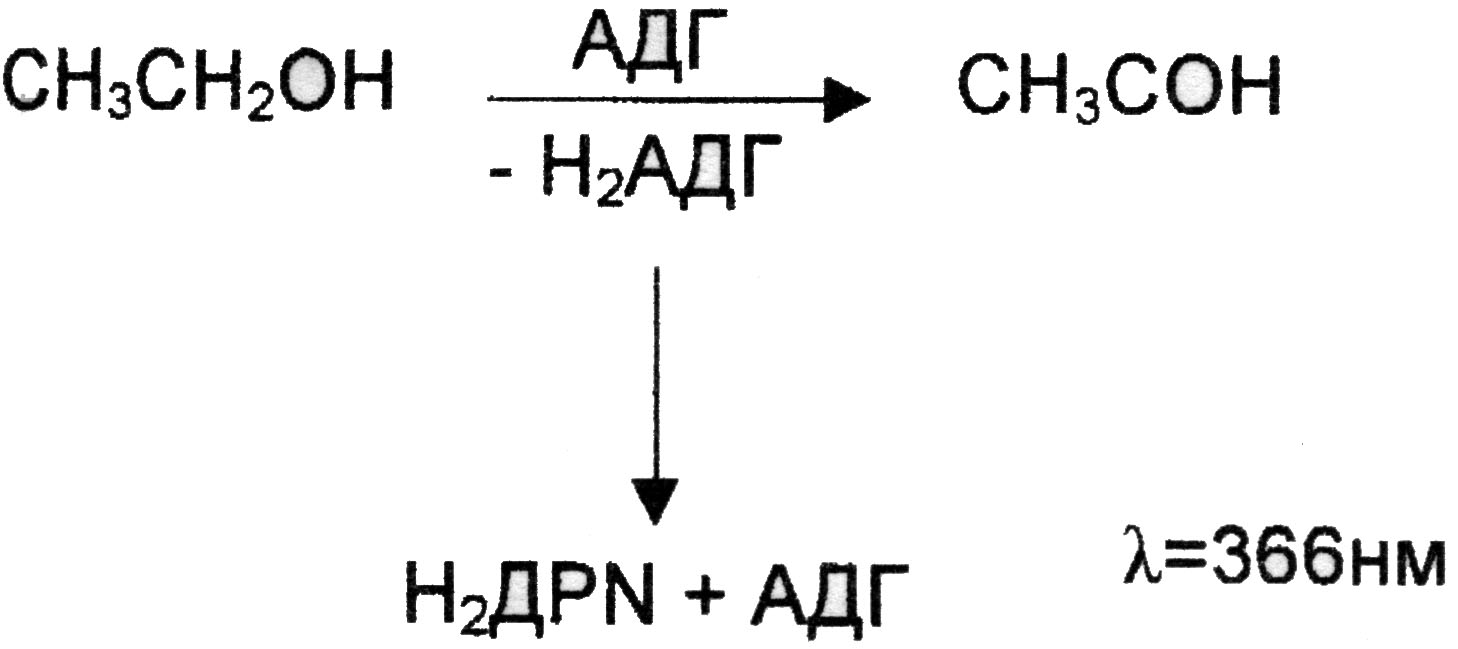
Акцептором водорода в реакции служит дифосфопиридин-нуклеотид (ДПН), восстановленная форма которого обладает характерным светопоглощением при длине волны 366 нм. Измеряя оптическую плотность продукта реакции, можно рассчитать содержание этанола в исследуемом объекте, т.к. количество восстановленной формы ДПН, т.е его оптическая плотность, пропорциональны количеству этанола. Расчет ведут по калибровочному графику, построенному по растворам этанола с известной концентрацией.
Судебно-химическая оценка метода.
Метод газожидкостной хроматографии (ГЖХ) основан на переведении этанола в более летучее соединение - этиловый эфир азотистой кислоты (этилнитрит).
Прежде, чем перейти к описанию этого метода, рассмотрим основные его теоретические положения и аппаратурное оформление и остановимся на преимуществах его перед химическими методами анализа.
Достоинства метода ГЖХ:
* Высокая разделяющая способность, что позволяет анализировать сложные многокомпонентные смеси. Это удобно при экспертных исследованиях в случаях комбинированных отравлений суррогатами алкоголя;
* Универсальность метода. Анализировать можно любые соединения при условии их летучести и термостабильности;
* Возможность качественного и количественного определения в одной пробе. Высокая чувствительность (10-5 – 10-9 г, т.е. на уровне естественного содержания этанола в организме);
* Возможность выполнения анализа в малом объеме образца (0,5-2 мл биожидкости). Точность метода (ошибка не превышает 1-2%);
* Экспрессность (время определения 3-5 минут) и возможность проведения, в связи с этим, серийных анализов;
* Простота и легкость выполнения;
* Доказательность и объективность. Результат в виде хроматограммы может быть приложен к акту судебно-химического исследования;
Определение этанола методом ГЖХ:
Определение этилового спирта в биологических жидкостях (крови и моче) методом ГЖХ при судебно-химических исследованиях было предложено в 1968 году судебным химиком Таджикского республиканского БСМЭ В.Ф.Пономаревым.
Метод основан на превращении спиртов в сложные эфиры азотистой кислоты - алкилнитриты, высоколетучие соединения, которые подвергаются газохроматографическому анализу.
В основе метода лежат реакции:
R-OH = R-ONO
ССl3СООН + NaNO2 = CCl3COONa + HNO2
HNO2 + C2H5OH = C2H5ONO↑ + H2O
избыток 2HNO2 = H2O +NO+NO2
Эти реакции выполняются в герметично укупоренном флаконе. Парогазовую фазу, содержащую алкилнитриты, в количестве 0,5 – З мл отбирают шприцем, прокалывая пробку флакона, и вводят в колонку хроматографа.
При определении спиртов технические параметры следующие газ-носитель - азот,
твердый носитель -инзенский кирпич или хроматон, неподвижная жидкая фаза
- винилин или триэтиленгликоль в количестве 5% от веса твердого носителя,
- колонка металлическая диаметром 3-бмм, длиной 2 м,
- детектор - катарометр.
Спирты выходят из колонки в порядке молекулярной массы в гомологическом ряду, причем изомеры выходят раньше нормальных спиртов.
Хроматограмма смеси спиртов C1 - C5 в виде их алкилнитритов выглядит следующим образом:

]
1-окислы азота NO и NO2
2-метилнитрит CH3ONO
3-этилнитрит С2Н5ONO
4-изопропилнитрит i-C3Н7ON О
5-пропилнитрит н- С3Н7ONO
6-изобутилнитрит i-C4H9ONO
7-бутилнитрит н-С4Н9ONO
8-изоамилнитрит i-C5H11ONO
9-амилнитрит н-С5H11ONO
Идентификацию спиртов проводят по относительному времени удерживания их алкилнитритов, используя в качестве метчика (стандарта) метанол.
Разделение веществ на колонке дает возможность определять индивидуально каждый спирт и другие «летучие» яды, т.е. делает метод специфичным.
Количественное определение этанола проводят по высоте или площади хроматографического пика, используя метод внутреннего стандарта. В качестве внутреннего стандарта используют нормальный или изопропанол, который добавляют в известном количестве во флакон с пробой.
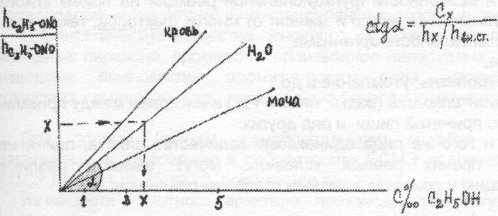
Расчет проводят по калибровочному графику, который строится заранее по растворам этанола с известной концентрацией (1, 3 или 5%о), или по методу котангенса. Калибровка строится по водным растворам этанола, поэтому при работе с биожидкостями вводят поправочные коэффициенты: 0,95 для крови и 1,05 для мочи.
Оценка результатов количественного определения этанола в крови человека
Данные о количественном содержании этанола в крови лежат в основе клинико-лабораторной диагностики степени опьянения. Установлена зависимость между содержанием этанола в крови и функциональным состоянием организма.
Критерии этой зависимости:
Содержание этанола в крови, промилле
|
Степень опьянения
|
Признаки
|
Менее 0,3
|
Отсутствие влияния аокоголя
|
|
0,3-0,5
|
Незначительное влияние алкоголя
|
Вождение автотранспорта запрещено
|
0,5-1,5
|
Легкая степень опьянения
|
Легкое нарушение координации движений
|
1,5-2,5
|
Опьянение средней степени
|
Возбуждение, иногда опасное для окружающих, шатающаяся походка, неясная речь, нарушение психики и ориентировки, иногда резкая сонливость
|
2,5-3,0
|
Сильное опьянение
|
Ступор (оглушение), снижение болевой чувствительности до полной анестезии Начальные признаки острого отравления Возможен смертельный исход
|
3,0-5,0
|
Тяжелое отравление алкоголем возможно наступление смерти
|
Кома, опасное для жизни состояние
|
Свыше 5,0
|
Смертельное отравление
|
|
Эта шкала имеет относительный характер, так как не всегда есть строгая корреляция между содержанием этанола в крови и функциональным состоянием организма. Степень и особенности функциональной реакции на прием алкоголя носят строго индивидуальный характер и зависят от многих факторов, таких, как:
-индивидуальная чувствительность организма,
-пол, возраст человека,
-состояние организма (болезнь, утомление и др ),
-форма, в которой принят алкоголь (водка, пиво и т д ) и интервал между приемами;
-характер и количество принятой пищи и ряд других;
Даже у одного и того же лица одинаковые количества спирта, принятые в разное время при прочих равных условиях, могут вызвать различную функциональную реакцию и привести к разным степеням опьянения.
При судебно-химической оценке результатов определения этанола следует учитывать также падение количества алкоголя в крови за 1 час, составляющее 0,1- 0,15%, поскольку между моментом происшествия и моментом смерти проходит обычно некоторый период времени, в течение которого протекают процессы метаболизма и выделения спирта из организма.
