- •Молекулярна фізика. Лабораторний практикум
- •Перелік лабораторних робіт
- •Список рекомендованої літератури
- •Частина і. Молекулярна фізика. Розділ 1. Будова речовини
- •1.1. Модель речовини. Маси атомів і молекул
- •1.2. Сили міжмолекулярної взаємодії. Агрегатні стани речовини
- •1.3. Енергія міжмолекулярної взаємодії. Потенціал Ленарда–Джонса
- •1.4. Структура речовини
- •1.4.1. Газоподібний стан
- •1.4.2. Рідини
- •1.4.3. Тверді тіла
- •Розділ 2. Основи молекулярно-кінетичної теорії газів
- •2.1. Ідеальний газ. Ізопроцеси. Рівняння стану ідеального газу
- •2.2. Тиск і температура ідеального газу. Основне рівняння молекулярно-кінетичної теорії
- •2.3. Поняття про статистичний розподіл. Функції розподілу
- •2.3.1. Закони розподілу молекул ідеального газу за швидкостями й енергіями теплового руху (розподіл Максвелла)
- •2.3.2. Барометрична формула. Розподіл Больцмана
- •2.3.3. Розподіл Максвелла–Больцмана
- •2.3.4. Квантові аспекти розподілів. Розподіли Бозе–Айнштайна і Фермі–Дірака
- •2.4. Середня кількість зіткнень молекул. Середня довжина вільного пробігу
- •Розділ 3. Основи термодинаміки
- •3.1. Головні поняття й означення
- •3.2. Внутрішня енергія ідеального газу Молекули ідеального газу не взаємодіють на відстані, тому
- •Вище доведено, що середня кінетична енергія теплового руху молекули ідеального газу
- •3.3. Теплоємність ідеального газу
- •Для ізобарного процесу
- •3.4. Теплоємність рідин
- •3.5. Теплоємність твердих тіл
- •3.5.1. Класична теорія теплоємності твердих тіл
- •3.5.2. Квантові теорії теплоємності твердих тіл.
- •3.6. Адіабатний процес
- •3.7. Політропні процеси
- •3.8. Робота в термодинамічних процесах
- •3.9. Стисливість газів
- •3.10. Ентропія
- •3.11. Циклічні процеси. Теплові машини
- •Розділ 4. Реальні гази
- •4.1. Рівняння стану реального газу. Рівняння Ван-дер-Ваальса
- •4.2. Внутрішня енергія і теплоємність реального газу
- •Розділ 5. Поверхневий натяг. Капілярні явища
- •На підставі (5.3) рівняння (5.4) запишемо у вигляді
- •Розділ 6. Фазові переходи
- •6.1. Агрегатні стани і фази речовини
- •6.2. Фазові переходи першого і другого роду
- •Розділ 7. Явища перенесення
- •7.1. Самодифузія і взаємна дифузія
- •7.2. Теплопровідність
- •7.4. Розріджені гази. Вакуум
- •Частина іі. Молекулярна фізика. Лабораторний практикум. Лабораторна робота № 201. Визначення коефіцієнта в’язкості рідини методом стокса
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 202. Дослідження залежності коефіцієнта в’язкості рідини від температури
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 203. Визначення коефіцієнта в’язкості рідини за допомогою капілярного віскозиметра оствальда
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №205. Визначення коефіцієнта поверхневого натягу рідини методом відривання кільця
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 206. Дослідження залежності коефіцієнта поверхневого натягу рідини від температури методом максимального тиску в бульбашці
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №208. Дослідження теплового розширення металів
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №209. Визначення питомої теплоємності металів методом охолодження
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 210. Визначення сталої больцмана та універсальної газової сталої
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №211. Визначення середньої довжини вільного пробігу та ефективного діаметра молекул повітря
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 212 визначення співвідношення теплоємностей повітря сp/сv методом клемана–дезорма
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 213. Визначення співвідношення теплоємностей повітря ср / сv методом стоячої хвилі
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 214. Вимірювання вологості повітря психрометром
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 215. Дослідження критичного стану речовини
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №216. Дослідження процесу плавлення кристалічних речовин
- •Порядок виконання роботи
- •Контрольні запитання
- •Додатки Головні фізичні сталі
- •Густина твердих тіл . За температури 20ºС
- •Густина рідин за температури 20ºС
- •Густина газів
- •Додаток 4 Теплофізичні коефіцієнти твердих тіл
- •Додаток 5 Пружні властивості твердих тіл
- •Додаток 6 Коефіцієнти лінійного теплового розширення твердих тіл в інтервалі 0–100 ºС
- •Додаток 7 Швидкість поширення звуку в різних середовищах
- •Додаток 8 Деякі фізичні характеристики рідин
- •Додаток 11 Коефіцієнт об’ємного теплового розширення деяких рідин
1.4.3. Тверді тіла
Структура твердого
тіла.
Рис. 1.8. Функція радіального розподілу
середньої густини молекул у твердому
тілі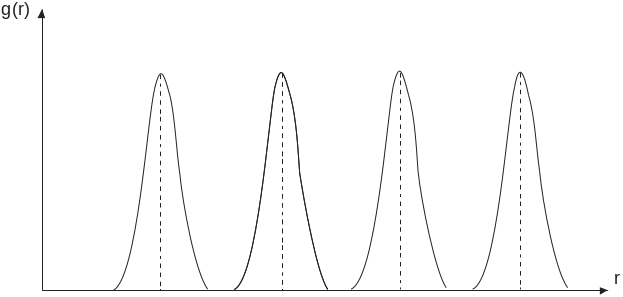
Очевидно, що умови рівноважного розташування молекул у твердому тілі поширюються на весь його об’єм і спричинюють виникнення просторової періодичної структури. Ця періодична структура має вигляд кристалічної ґратки. У кристалічній ґратці молекули (атоми, іони) розміщені у її вузлах –
точках, що відповідають положенню рівноваги. Характер руху молекул твердого тіла коливальний. Тверді тіла мають просторову структуру, для якої, на відміну від речовини, характерний як ближній, так і дальній порядок. Експериментальним підтвердженням кристалічної структури твердих тіл є результати рентгеноструктурного дослідження їхньої функції радіального розподілу g(r), показані на рис. 1.8. Як бачимо, просторова впорядкованість молекул, що утворюють кристалічну ґратку, є головною ознакою твердих тіл.
Зазначимо, що всі тверді тіла можна розділити на два типи – монокристалічні та полікристалічні. У монокристалах дальній порядок чітко витриманий у всьому об’ємі твердого тіла. Природні монокристали (гірський кришталь, сапфір, алмаз тощо) мають, здебільшого, правильну форму багатогранника і є анізотропними, тобто їхні фізичні властивості різні, залежно від напряму вимірювання. Полікристалічні тіла складаються з великої кількості дрібних монокристалів, розміри і просторова орієнтація яких є різними. Завдяки такій будові полікристалічні зразки ізотропні.
У розмаїтті речовин навколишнього світу є й такі, що поєднують властивості рідин і твердих тіл. Це так звані аморфні тіла (скло, бурштин, пластики та ін.), які, зазвичай, ми зачислюємо до твердих. За окремими властивостями вони справді мають ознаки твердого тіла (здатність зберігати форму й об’єм, механічну стійкість до деформацій, перехід у рідкий стан під час нагрівання та ін.). Водночас за структурою вони ближчі до рідин. Зокрема, для аморфних тіл характерний лише ближній порядок у розміщенні атомів. У них зовсім нема кристалічної структури. Саме тому аморфні тіла слід розглядати як переохолоджені рідини, що перебувають у метастабіль-ному (нестійкому) стані.
Надалі під поняттям тверде тіло ми розумітимемо лише кристалічні речовини.
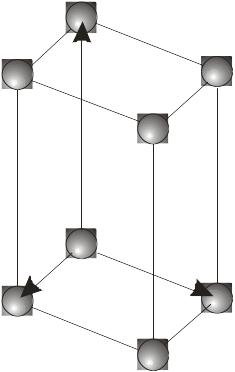
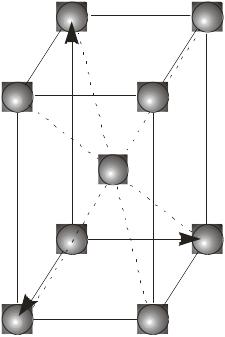
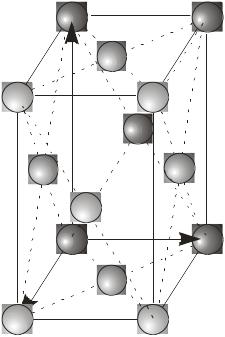
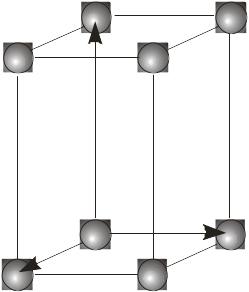
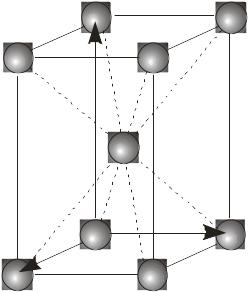
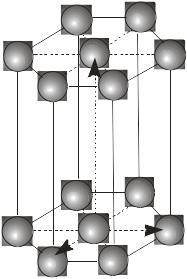
Кристалічна ґратка. У будь-якому кристалі елементарні структурні частинки (атоми, молекули, іони) розміщені періодично вздовж будь-якого напряму, утворюючи кристалічну ґратку (рис. 1.9).
Я
Рис. 1.9. Кристалічна ґратка.
Базисні вектори

![]() і вектор трансляції
і вектор трансляції
![]()
![]() називають базисними. За допомогою
базисних векторів можна записати
радіус-вектор
називають базисними. За допомогою
базисних векторів можна записати
радіус-вектор
![]() ,
який визначає положення будь-якого
атома в кристалічній ґратці:
,
який визначає положення будь-якого
атома в кристалічній ґратці:
![]() ,
(1.14)
,
(1.14)
де n1, n2, n3 – натуральні числа. Вектор називають вектором трансляції.
Кристалічну ґратку, яка задовольняє умову (1.14), називають примітивною ґраткою, а її елементарну комірку – примітивною коміркою.
Зазначимо, що складні кристалічні ґратки складаються з кількох примітивних.
Симетрія кристалів. Елементи симетрії. Закономірно, що просторова періодичність у розміщенні атомів кристала та його частин
зумовлює симетрію кристала. Надалі під поняттям симетрії розумітимемо здатність твердого тіла суміщатись із собою під час його рухів або певних операцій над його точками. До елементів симетрії твердих тіл належать:
1) площина симетрії Р;
2) поворотна вісь симетрії n-го порядку Ln;
3) центр симетрії, або центр інверсії С;
4)
дзеркально-поворотна вісь симетрії
n-го
порядку
![]() ;
;
5) вісь інверсії Lin.
Я
Рис. 1.10. Площини симетрії тіла Р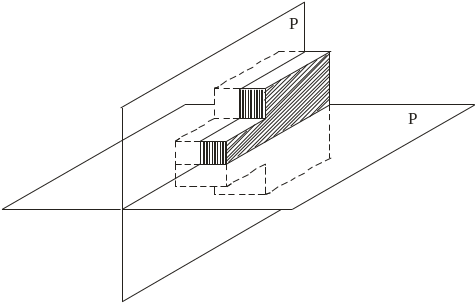
Віссю симетрії n-го порядку Ln називають вісь, під час повертання навколо якої на кут 2/n тіло суміщається з собою.
Якщо тіло можна сумістити з собою шляхом інверсії відносно точки С, то цю точку називають центром симетрії. Центр симетрії – це точка перетину трьох взаємо перпендикулярних площин симетрії тіла.
Дзеркально-поворотна
вісь симетрії n-го
порядку
![]() діє як сукупність осі симетрії n-го
порядку і площини симетрії, що
перпендикулярна до неї (рис.1.11).
діє як сукупність осі симетрії n-го
порядку і площини симетрії, що
перпендикулярна до неї (рис.1.11).
Рис. 1.11
Дзеркально-поворотна
вісь симетрії 2-го порядку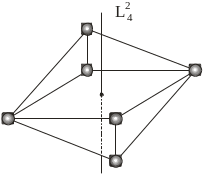
L1=1; C=1;
L2=2; Li2=3;
L3=3; Li4=4;
L4=4; Li4=6;
L6=6; p = m.
П’ять описаних вище елементів симетрії кристалів називають точковими, оскільки їхня дія завжди залишає нерухомою хоча б одну точку кристала. Крім точкових елементів симетрії, для складних кристалів характерні ще й два просторові елементи симетрії – гвинтова вісь n-го порядку та площина дзеркального ковзання. Гвинтова вісь симетрії n-го порядку – це та вісь, переміщенням уздовж якої з одночасним повертанням на кут 2/n кристалічну ґратку буде суміщено саму з собою. Площина дзеркального ковзання забезпечує таке суміщення кристалічної ґратки шляхом одночасного дзеркального відображення у площині та зсуву на певну відстань паралельно до площини.
Отже, поряд з елементами точкової симетрії кристалічна ґратка має трансляційну симетрію і просторові елементи симетрії. Сукупність усіх елементів симетрії ґратки називають її просторовою групою. Кристалограф Е. Федоров довів, що всього є 230 просторових груп симетрії кристалів.
У кристалографії сукупність елементів симетрії, притаманних конкретному кристалу, визначає його клас симетрії. У 1869 р. А. Гадолін, використовуючи закономірності складання елементів симетрії, довів, що в природі існує 32 класи симетрії кристалів. За параметрами елементарної комірки кристали поділяють на сім типів кристалографічних систем (сингоній). До однієї сингонії належать кристали з подібними елементарними комірками. У таких комірках співвідношення між довжинами векторів і відповідними кутами між ними однакові.
Ознаки кристалографічних систем (сингоній)
Тип сингонії |
Параметри елементарної комірки |
|
Кубічна |
а1=а2=а3 |
===90 |
Гексагональна |
а1=а2а3 |
==90, =120 |
Тетрагональна |
а1=а2а3 |
===90 |
Тригональна |
а1=а2=а3 |
==90 |
Ромбічна |
а1а2а3 |
===90 |
Моноклінна |
а1а2а3 |
==90, 90 |
Триклінна |
а1а2а3 |
90 |
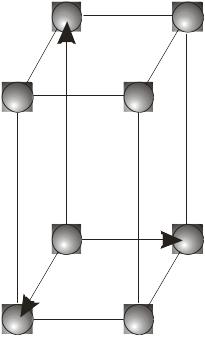
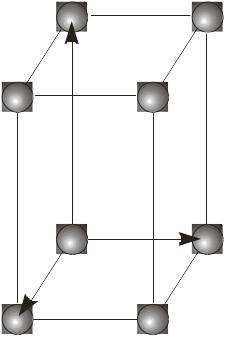
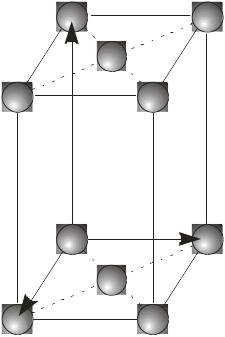
Ґратки Браве. Кристалографічні індекси. Автором сучасної теорії гратчастої будови кристалів є А. Браве, який 1855 р. математично довів існування 14 типів кристалічних ґраток. Учений виявив, що будь-яку просторову кристалічну ґратку можна відтворити шляхом трансляції одного паралелепіпеда вздовж кристалографічних напрямів. Такий елементарний паралелепіпед просторової ґратки називають ґраткою Браве. Чотирнадцять ґраток Браве розділені між сімома сингоніями так:
Сингонія |
Примі-тивна |
Базо- центрована |
Об’ємо- центрована |
Гране- центрована |
Триклінна |
|
|
|
|
Моноклінна |
|
|
|
|
Ромбічна |
|
|
|
|
Тригональна (ромбоедрична) |
|
|
|
|
Тетрагональна |
|
|
|
|
Гексагональна |
|
|
|
|
Кубічна |
|
|
|
|
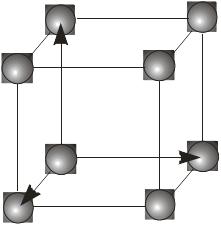
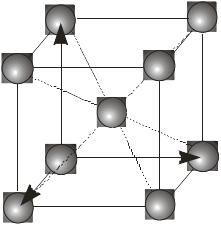
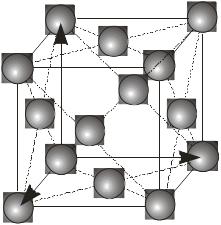
Кожна із семи сингоній має примітивну ґратку Браве. Базоцентровані ґратки є лише у моноклінній та ромбічній сингоніях, а гранецентровані – у ромбічній та кубічній. Об’ємоцентровані ґратки мають три сингонії – ромбічну, тетрагональну і кубічну.
П
Рис. 1.12. Вибір осей системи координат,
базисних векторів і кутів у паралелепіпеді
Браве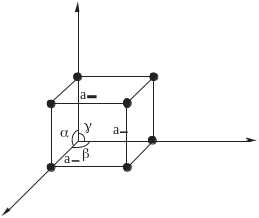
Для характеристики паралельних атомних площин у кристалі достатньо виразити одну з них. Рівняння будь-якої площини в прямокутних (або косокутних) координатах має вигляд
 ,
(1.15)
,
(1.15)
де ОА, ОВ і ОС – довжини відрізків (в одиницях масштабу), які площина відтинає на відповідних осях координат. Оскільки довжини цих відрізків є раціональними числами, то рівняння (1.15) можна записати у вигляді
![]() ,
(1.16)
,
(1.16)
д
Рис. 1.13. Кристалографічні площини
і кристалографічні напрями у кристалі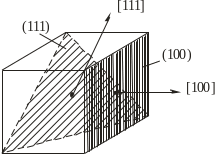
![]() kl).
Напрям у кристалі, перпендикулярний до
заданої атомної площини, позначають
тими ж індексами Міллера, записаними у
квадратних дужках – [hkl].
На рис. 1.13 показані, як приклад, дві
атомні площини і відповідні їм напрями
у кристалі кубічної сингонії.
kl).
Напрям у кристалі, перпендикулярний до
заданої атомної площини, позначають
тими ж індексами Міллера, записаними у
квадратних дужках – [hkl].
На рис. 1.13 показані, як приклад, дві
атомні площини і відповідні їм напрями
у кристалі кубічної сингонії.
Дефекти
кристалічної ґратки.
Рис. 1.14. Точкові дислокації:
а –
вакансія; б
– заміщення;
в –
впровадження
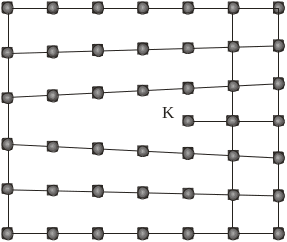
Рис. 1.15. Крайова (ліворуч) та гвинтова
(праворуч) дислокації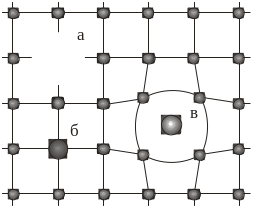

1) вакансія – це відсутність атома у вузлі ґратки;
2) заміщення – коли у вузлі ґратки міститься атом іншого сорту;
3) впровадження – коли атом іншого сорту міститься у міжвузлі кристалічної ґратки (рис. 1.14). Точкові дефекти порушують лише ближній порядок у кристалічній ґратці. На відміну від точкових, лінійні дефекти порушують дальній порядок у кристалі. Лінійні дефекти називають дислокаціями і поділяють на крайові та гвинтові. Крайову дислокацію можна уявити як додаткову півплощину, розміщену між атомними площинами кристала (див. рис. 1.14). Гвинтова дислокація утворюється внаслідок ковзання двох атомних півплощин на один період одна щодо одної (рис. 1.15).
Дислокації не можуть обриватися всередині кристала. Вони закінчуються на поверхні кристала, на межі зерна у полікристалічному зразку або ж мають вигляд замкненої петлі. Дислокації можуть суттєво впливати на механічні властивості твердих тіл.