
- •Молекулярна фізика. Лабораторний практикум
- •Перелік лабораторних робіт
- •Список рекомендованої літератури
- •Частина і. Молекулярна фізика. Розділ 1. Будова речовини
- •1.1. Модель речовини. Маси атомів і молекул
- •1.2. Сили міжмолекулярної взаємодії. Агрегатні стани речовини
- •1.3. Енергія міжмолекулярної взаємодії. Потенціал Ленарда–Джонса
- •1.4. Структура речовини
- •1.4.1. Газоподібний стан
- •1.4.2. Рідини
- •1.4.3. Тверді тіла
- •Розділ 2. Основи молекулярно-кінетичної теорії газів
- •2.1. Ідеальний газ. Ізопроцеси. Рівняння стану ідеального газу
- •2.2. Тиск і температура ідеального газу. Основне рівняння молекулярно-кінетичної теорії
- •2.3. Поняття про статистичний розподіл. Функції розподілу
- •2.3.1. Закони розподілу молекул ідеального газу за швидкостями й енергіями теплового руху (розподіл Максвелла)
- •2.3.2. Барометрична формула. Розподіл Больцмана
- •2.3.3. Розподіл Максвелла–Больцмана
- •2.3.4. Квантові аспекти розподілів. Розподіли Бозе–Айнштайна і Фермі–Дірака
- •2.4. Середня кількість зіткнень молекул. Середня довжина вільного пробігу
- •Розділ 3. Основи термодинаміки
- •3.1. Головні поняття й означення
- •3.2. Внутрішня енергія ідеального газу Молекули ідеального газу не взаємодіють на відстані, тому
- •Вище доведено, що середня кінетична енергія теплового руху молекули ідеального газу
- •3.3. Теплоємність ідеального газу
- •Для ізобарного процесу
- •3.4. Теплоємність рідин
- •3.5. Теплоємність твердих тіл
- •3.5.1. Класична теорія теплоємності твердих тіл
- •3.5.2. Квантові теорії теплоємності твердих тіл.
- •3.6. Адіабатний процес
- •3.7. Політропні процеси
- •3.8. Робота в термодинамічних процесах
- •3.9. Стисливість газів
- •3.10. Ентропія
- •3.11. Циклічні процеси. Теплові машини
- •Розділ 4. Реальні гази
- •4.1. Рівняння стану реального газу. Рівняння Ван-дер-Ваальса
- •4.2. Внутрішня енергія і теплоємність реального газу
- •Розділ 5. Поверхневий натяг. Капілярні явища
- •На підставі (5.3) рівняння (5.4) запишемо у вигляді
- •Розділ 6. Фазові переходи
- •6.1. Агрегатні стани і фази речовини
- •6.2. Фазові переходи першого і другого роду
- •Розділ 7. Явища перенесення
- •7.1. Самодифузія і взаємна дифузія
- •7.2. Теплопровідність
- •7.4. Розріджені гази. Вакуум
- •Частина іі. Молекулярна фізика. Лабораторний практикум. Лабораторна робота № 201. Визначення коефіцієнта в’язкості рідини методом стокса
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 202. Дослідження залежності коефіцієнта в’язкості рідини від температури
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 203. Визначення коефіцієнта в’язкості рідини за допомогою капілярного віскозиметра оствальда
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №205. Визначення коефіцієнта поверхневого натягу рідини методом відривання кільця
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 206. Дослідження залежності коефіцієнта поверхневого натягу рідини від температури методом максимального тиску в бульбашці
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №208. Дослідження теплового розширення металів
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №209. Визначення питомої теплоємності металів методом охолодження
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 210. Визначення сталої больцмана та універсальної газової сталої
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №211. Визначення середньої довжини вільного пробігу та ефективного діаметра молекул повітря
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 212 визначення співвідношення теплоємностей повітря сp/сv методом клемана–дезорма
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 213. Визначення співвідношення теплоємностей повітря ср / сv методом стоячої хвилі
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 214. Вимірювання вологості повітря психрометром
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 215. Дослідження критичного стану речовини
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №216. Дослідження процесу плавлення кристалічних речовин
- •Порядок виконання роботи
- •Контрольні запитання
- •Додатки Головні фізичні сталі
- •Густина твердих тіл . За температури 20ºС
- •Густина рідин за температури 20ºС
- •Густина газів
- •Додаток 4 Теплофізичні коефіцієнти твердих тіл
- •Додаток 5 Пружні властивості твердих тіл
- •Додаток 6 Коефіцієнти лінійного теплового розширення твердих тіл в інтервалі 0–100 ºС
- •Додаток 7 Швидкість поширення звуку в різних середовищах
- •Додаток 8 Деякі фізичні характеристики рідин
- •Додаток 11 Коефіцієнт об’ємного теплового розширення деяких рідин
Порядок виконання роботи
1. Записати вихідні дані: 0=(1,250+0,005)103 кг/м3; свинцю=(11,40±0,01)103 кг/м3; сталі=(7,80 + 0,01)103 кг/м3.
2. Тричі виміряти внутрішній діаметр циліндра і діаметр кульки. Обчислити середні значення R і r..
3. Мітками 2 позначити і тричі виміряти задану викладачем відстань l між ними. (Для забезпечення рівномірного руху кульки верхня мітка повинна бути на 3–5 см нижче від рівня рідини). Обчислити середнє значення l.
4. Опустити кульку в рідину вздовж осі циліндра і виміряти секундоміром час її руху між мітками. Виконати аналогічні експерименти з п’ятьма кульками.
5. Результати вимірювань і обчислень записати в таблицю.
Номер за пор. |
l, м |
l, м |
R, М |
R, м |
r, м |
r, м |
t, с |
t, с |
1 |
|
|
|
|
|
|
|
|
... |
|
|
|
|
|
|
|
|
C.з. |
|
|
|
|
|
|
|
|
Абсолютну похибку вимірювання обчислити за формулою
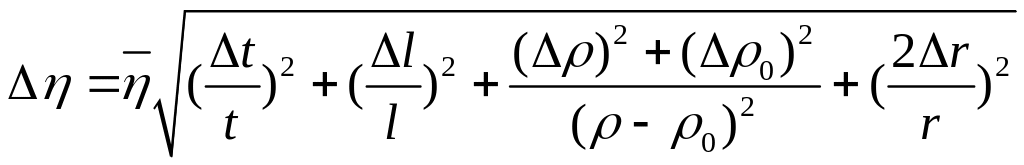 .
.
Значення i 0 взяти з п.1, t розрахувати як похибку приладу.
6. Кінцевий результат записати у вигляді
=( ), E=...%.
Контрольні запитання
1. Чому внутрішнє тертя належить до явищ перенесення?
2. Від чого залежить сила внутрішнього тертя в рідинах і газах?
3. У чому полягає фізичний зміст коефіцієнта в’язкості рідин?
4. Запишіть і поясніть формулу Стокса. За яких умов її можна застосовувати?
5. Які сили діють на кульку під час її руху в рідині?
6. Від чого залежить коефіцієнт в’язкості рідини?
7. Запишіть і поясніть формулу Пуазейля.
Лабораторна робота № 202. Дослідження залежності коефіцієнта в’язкості рідини від температури
Завдання: визначити коефіцієнт в’язкості гліцерину за різних температур в інтервалі 18–40° С, побудувати графік залежності = f(t°С) і розрахувати енергію активації молекули.
Приладдя: віскозиметр Хепплера з досліджуваною рідиною, скляною кулькою і термометром; лабораторний автотрансформатор (ЛАТР); секундомір.
Теоретичний матеріал, який необхідно засвоїти під час підготовки до роботи: Див. лабораторну роботу №201.
Рис. 2
Рис. 3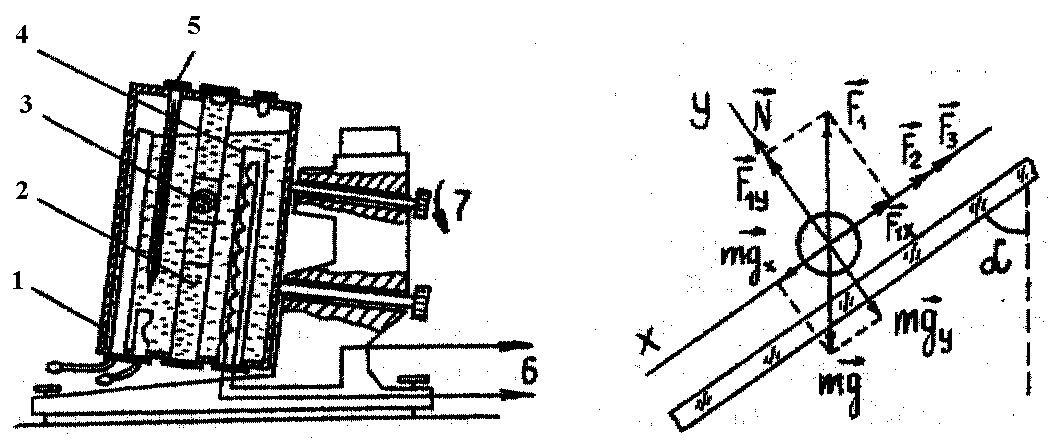
Опис установки. Віскозиметр Хепплера (рис. 2) складається зі скляного термостата 1, заповненого водою, всередині якого розміщена трубка 2 з досліджуваною рідиною і скляною кулькою 3. Трубка 2 нахилена під кутом 10° до вертикалі. В термостаті розміщений нагрівник 4 і термометр 5. Живлення нагрівника (не більше 80 В) забезпечують за допомогою ЛАТР 6. Скляний термостат 1 можна обертати навколо осі 00 і фіксувати гвинтом 7 у двох положеннях – прямому й оберненому. Це дає змогу виконувати багаторазові експерименти з досліджуваною рідиною, не виймаючи з неї скляної кульки.
Ідея роботи та виведення робочої формули. Визначення коефіцієнта в’язкості рідини за допомогою віскозиметра Хепплера ґрунтується на вимірюванні часу руху скляної кульки на заданому відрізку шляху у в’язкій рідині, температуру якої можна змінювати.
Під
час руху кульки на неї діють такі сили:
сила тяжіння
![]() ,
,
сила
Архімеда
![]() ,
сила тертя до стінки трубки F2=N,
сила
опору рідини рухові кульки F3,
яка за формулою Стокса дорівнює 6rv,
де r
– радіус кульки; 1
і 0
– густина матеріалу кульки і рідини;
– коефіцієнт тертя; N
– сила реакції;
– коефіцієнт в’язкості рідини; v
– швидкість руху кульки.
,
сила тертя до стінки трубки F2=N,
сила
опору рідини рухові кульки F3,
яка за формулою Стокса дорівнює 6rv,
де r
– радіус кульки; 1
і 0
– густина матеріалу кульки і рідини;
– коефіцієнт тертя; N
– сила реакції;
– коефіцієнт в’язкості рідини; v
– швидкість руху кульки.
Сили, які діють на кульку, показані на рис. 3. Якщо осі Х та У вибрати так, як показано на рис. 3, то, розклавши сили F1 і mg на складові, рівняння руху кульки (за умови, що її рух рівномірний) можна записати у виглядi
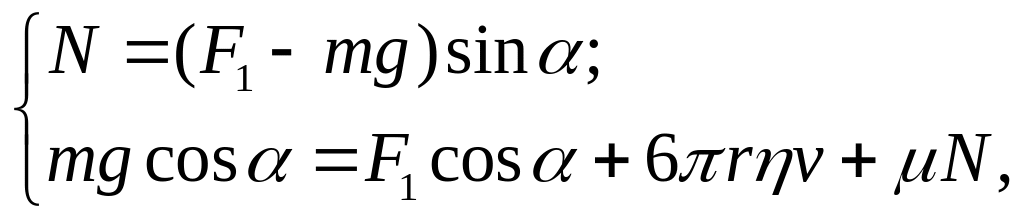 (1)
(1)
або
![]() .
(2)
.
(2)
Врахуємо, що швидкість кульки V можна виразити як
v=l/t, (3)
де l – відстань, яку проходить кулька; t – час руху. Із (2) і (3) отримаємо
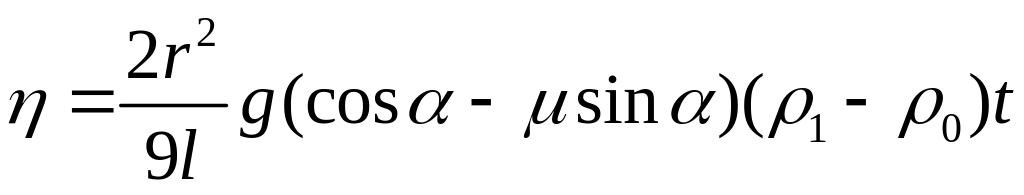 ,
,
або = (1 - 0)t, (4)
де є сталою приладу.
Вираз (4) – це робоча формула цієї лабораторної роботи.
Відомо, що коефіцієнт в’язкості залежить від температури. Для газів цю залежність визначає таке співвідношення:
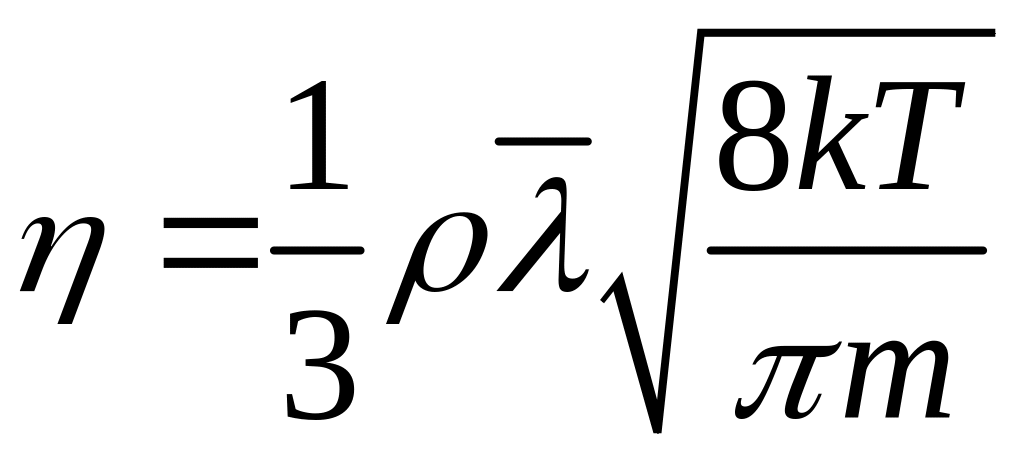 ,
(5)
,
(5)
де – густина; Т – абсолютна температура газу; m – маса молекули; – середня довжина вільного пробігу. Із (5) можна бачити, що для газів збільшується з підвищенням температури.
В’язкість рідин, на відміну від газів, зменшується з підвищенням температури. Це зумовлено різним характером руху молекул у рідинах і газах. Перехід молекули рідини від коливального до поступального руху (перехід в інше положення рівноваги) потребує певної енергії активації. Тому коефіцієнт в’язкості рідини залежить від температури так:
![]() ,
(6)
,
(6)
де Е – енергія активації молекули; k – стала Больцмана; Т – абсолютна температура; 0 – стала, що має розмірність коефіцієнта в’язкості.
Якщо експериментально визначити коефіцієнти в’язкості рідини 1 i 2
за різних температур Т1 і Т2, то на підставі (6) легко отримати співвідношення для визначення енергії активації молекул рідини:
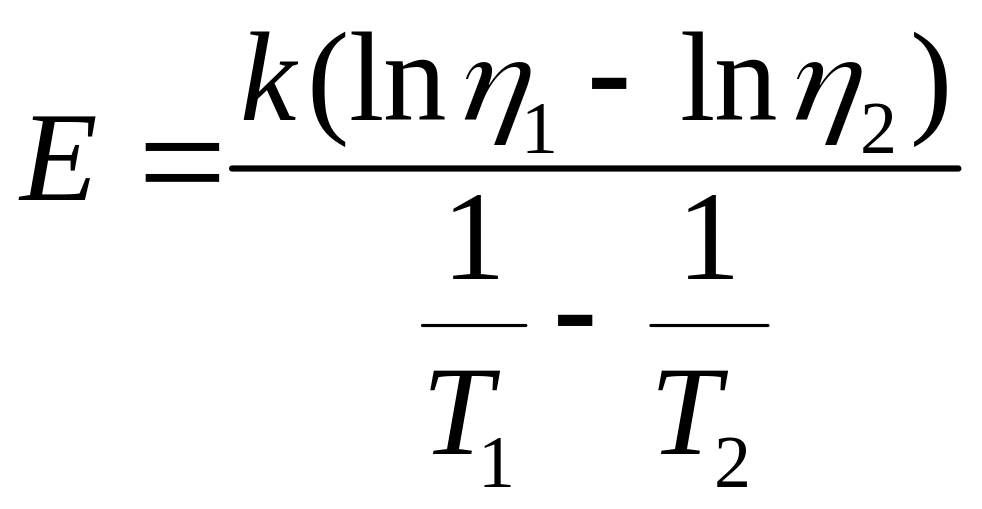 .
(7)
.
(7)
