
- •Молекулярна фізика. Лабораторний практикум
- •Перелік лабораторних робіт
- •Список рекомендованої літератури
- •Частина і. Молекулярна фізика. Розділ 1. Будова речовини
- •1.1. Модель речовини. Маси атомів і молекул
- •1.2. Сили міжмолекулярної взаємодії. Агрегатні стани речовини
- •1.3. Енергія міжмолекулярної взаємодії. Потенціал Ленарда–Джонса
- •1.4. Структура речовини
- •1.4.1. Газоподібний стан
- •1.4.2. Рідини
- •1.4.3. Тверді тіла
- •Розділ 2. Основи молекулярно-кінетичної теорії газів
- •2.1. Ідеальний газ. Ізопроцеси. Рівняння стану ідеального газу
- •2.2. Тиск і температура ідеального газу. Основне рівняння молекулярно-кінетичної теорії
- •2.3. Поняття про статистичний розподіл. Функції розподілу
- •2.3.1. Закони розподілу молекул ідеального газу за швидкостями й енергіями теплового руху (розподіл Максвелла)
- •2.3.2. Барометрична формула. Розподіл Больцмана
- •2.3.3. Розподіл Максвелла–Больцмана
- •2.3.4. Квантові аспекти розподілів. Розподіли Бозе–Айнштайна і Фермі–Дірака
- •2.4. Середня кількість зіткнень молекул. Середня довжина вільного пробігу
- •Розділ 3. Основи термодинаміки
- •3.1. Головні поняття й означення
- •3.2. Внутрішня енергія ідеального газу Молекули ідеального газу не взаємодіють на відстані, тому
- •Вище доведено, що середня кінетична енергія теплового руху молекули ідеального газу
- •3.3. Теплоємність ідеального газу
- •Для ізобарного процесу
- •3.4. Теплоємність рідин
- •3.5. Теплоємність твердих тіл
- •3.5.1. Класична теорія теплоємності твердих тіл
- •3.5.2. Квантові теорії теплоємності твердих тіл.
- •3.6. Адіабатний процес
- •3.7. Політропні процеси
- •3.8. Робота в термодинамічних процесах
- •3.9. Стисливість газів
- •3.10. Ентропія
- •3.11. Циклічні процеси. Теплові машини
- •Розділ 4. Реальні гази
- •4.1. Рівняння стану реального газу. Рівняння Ван-дер-Ваальса
- •4.2. Внутрішня енергія і теплоємність реального газу
- •Розділ 5. Поверхневий натяг. Капілярні явища
- •На підставі (5.3) рівняння (5.4) запишемо у вигляді
- •Розділ 6. Фазові переходи
- •6.1. Агрегатні стани і фази речовини
- •6.2. Фазові переходи першого і другого роду
- •Розділ 7. Явища перенесення
- •7.1. Самодифузія і взаємна дифузія
- •7.2. Теплопровідність
- •7.4. Розріджені гази. Вакуум
- •Частина іі. Молекулярна фізика. Лабораторний практикум. Лабораторна робота № 201. Визначення коефіцієнта в’язкості рідини методом стокса
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 202. Дослідження залежності коефіцієнта в’язкості рідини від температури
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 203. Визначення коефіцієнта в’язкості рідини за допомогою капілярного віскозиметра оствальда
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №205. Визначення коефіцієнта поверхневого натягу рідини методом відривання кільця
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 206. Дослідження залежності коефіцієнта поверхневого натягу рідини від температури методом максимального тиску в бульбашці
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №208. Дослідження теплового розширення металів
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №209. Визначення питомої теплоємності металів методом охолодження
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 210. Визначення сталої больцмана та універсальної газової сталої
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №211. Визначення середньої довжини вільного пробігу та ефективного діаметра молекул повітря
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 212 визначення співвідношення теплоємностей повітря сp/сv методом клемана–дезорма
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 213. Визначення співвідношення теплоємностей повітря ср / сv методом стоячої хвилі
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 214. Вимірювання вологості повітря психрометром
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 215. Дослідження критичного стану речовини
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №216. Дослідження процесу плавлення кристалічних речовин
- •Порядок виконання роботи
- •Контрольні запитання
- •Додатки Головні фізичні сталі
- •Густина твердих тіл . За температури 20ºС
- •Густина рідин за температури 20ºС
- •Густина газів
- •Додаток 4 Теплофізичні коефіцієнти твердих тіл
- •Додаток 5 Пружні властивості твердих тіл
- •Додаток 6 Коефіцієнти лінійного теплового розширення твердих тіл в інтервалі 0–100 ºС
- •Додаток 7 Швидкість поширення звуку в різних середовищах
- •Додаток 8 Деякі фізичні характеристики рідин
- •Додаток 11 Коефіцієнт об’ємного теплового розширення деяких рідин
3.6. Адіабатний процес
Адіабатним називають процес, під час якого термодинамічна система не обмінюється теплотою з навколишнім середовищем. На практиці до адіабатних можна зачислити всі швидкоплинні процеси. Рівняння адіабатного процесу для ідеального газу можна отримати з першого закону термодинаміки (3.1) і рівняння стану (2.6). Оскільки δQ=0, то
dU=
–δA,
або
![]() .
(3.30)
.
(3.30)
Продиференціюємо (3.30), отримаємо
![]() .
(3.31)
.
(3.31)
Тоді з (3.30) і (3.31)
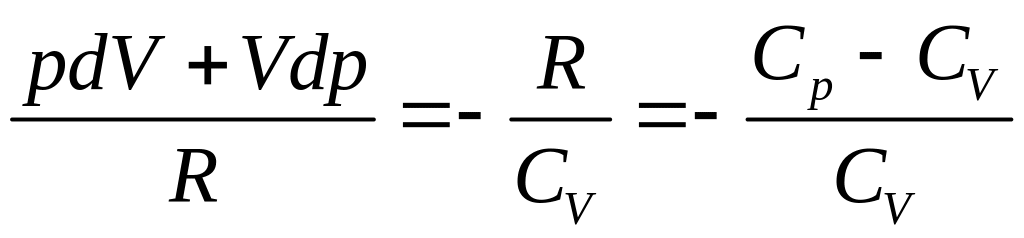 .
(3.32)
.
(3.32)
Після
розділення змінних і заміни
 (γ
– безрозмірна величина, яку називають
показником
адіабати)
маємо
(γ
– безрозмірна величина, яку називають
показником
адіабати)
маємо
 ,
(3.33)
,
(3.33)
звідки після інтегрування
![]() (3.34)
(3.34)
Це і є рівнянням адіабатного процесу, або рівнянням Пуассона. В інших змінних воно матиме вигляд
![]() ,
або
,
або
![]() .
(3.35)
.
(3.35)
Г
Рис. 3.5. Графіки
адіабатного та ізотермічного процесів
![]() і S=const.
і S=const.
3.7. Політропні процеси
Чотири класичні ізопроцеси, властиві ідеальному газу, мають спільну ознаку, а саме – сталу теплоємність:
ізобарний процес – C=Cр;
ізохорний процес – C=CV;
ізотермічний
процес – C=![]() ;
;
адіабатний процес – C=0.
Процеси, які відбуваються за сталої теплоємності (C=const), називають політропними. Рівняння політропного процесу
![]() (3.36)
(3.36)
де n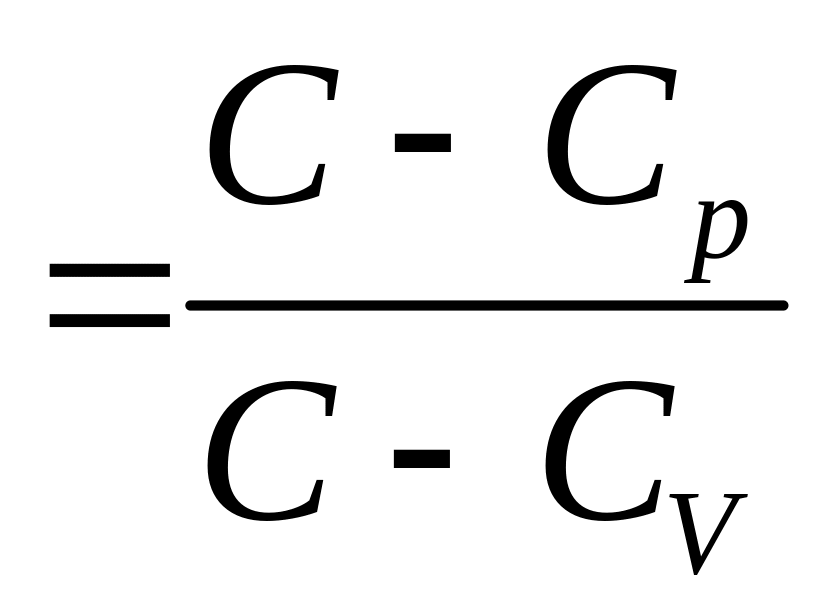 – показник політропи.
– показник політропи.
3.8. Робота в термодинамічних процесах
Роботу газу під час зміни його об’єму відображає інтеграл
А= .
(3.37)
.
(3.37)
Обчислимо роботу газу в кожному з політропних процесів.
1.
Ізотермічний процес (Т=const).
З рівняння стану ідеального газу
![]() ,
тоді з (3.37)
,
тоді з (3.37)
А=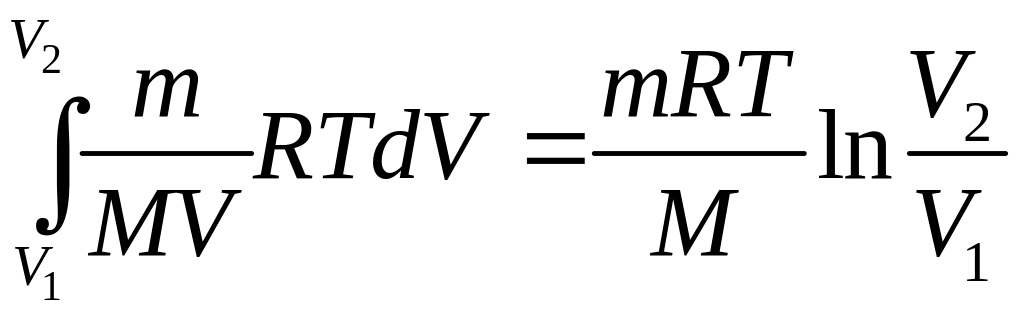 .
(3.38)
.
(3.38)
Оскільки
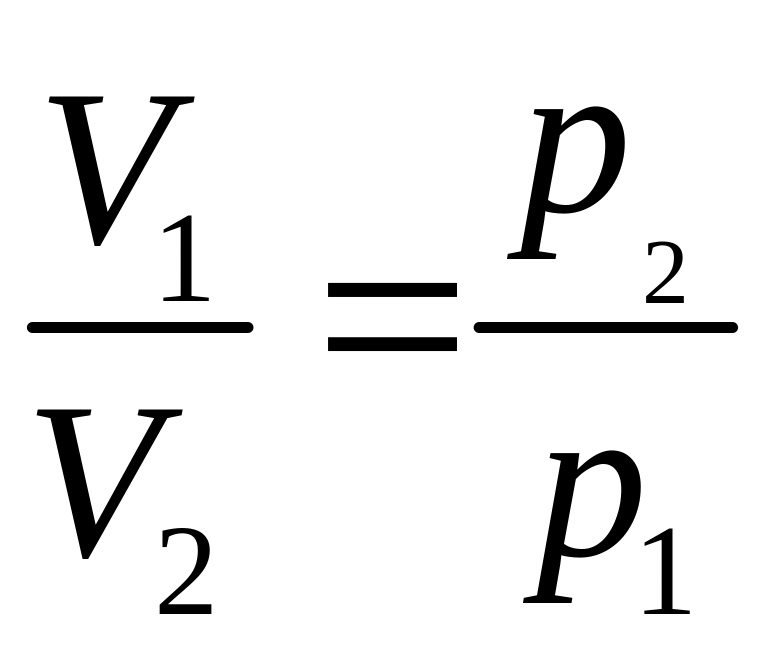 ,
то
,
то
А=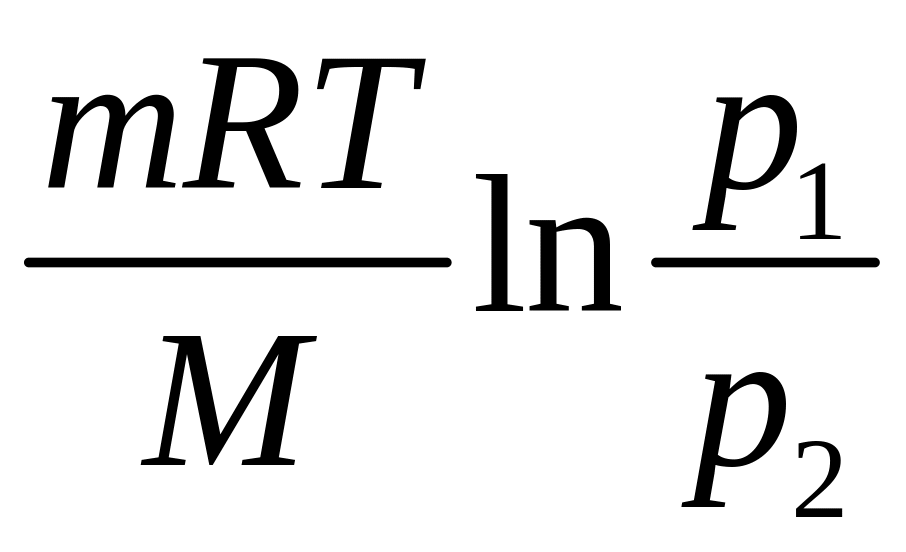 .
(3.39)
.
(3.39)
2. Ізохорний процес (V=const). За цих умов А=0, оскільки dV=0. Отже, під час ізохорного процесу виконання роботи не відбувається.
3. Ізобарний процес (р=const). За умови р=const з рівняння (3.37) маємо
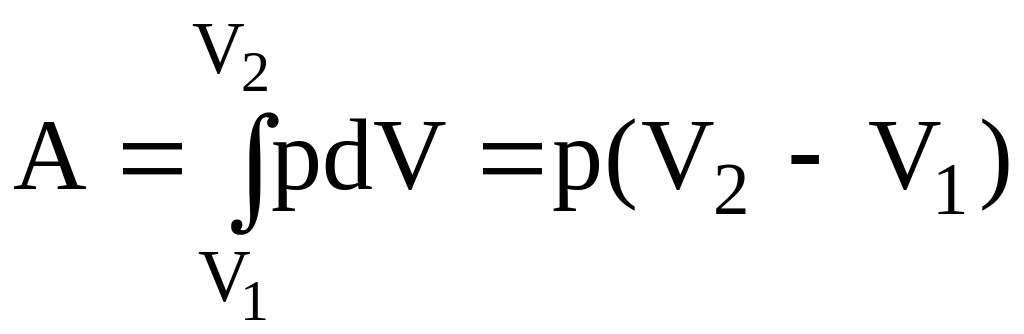 .
(3.40)
.
(3.40)
4. Адіабатичний процес (δQ=0). З першого закону термодинаміки
![]() .
(3.41)
.
(3.41)
Тоді
 .
(3.42)
.
(3.42)
З використанням рівнянь (3.27) та (3.28) вираз (3.42) можна звести до вигляду
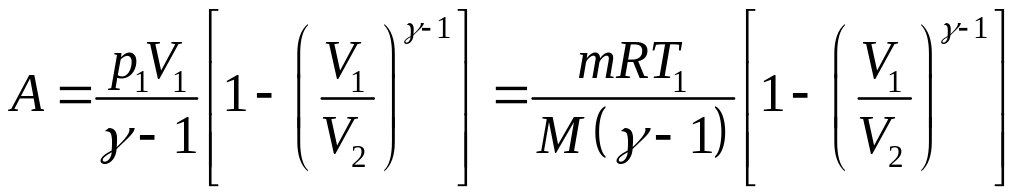 .
(3.43)
.
(3.43)
3.9. Стисливість газів
Зі зміною тиску газ змінює об’єм. Цю властивість газу називають стисливістю, яку характеризує коефіцієнт стисливості
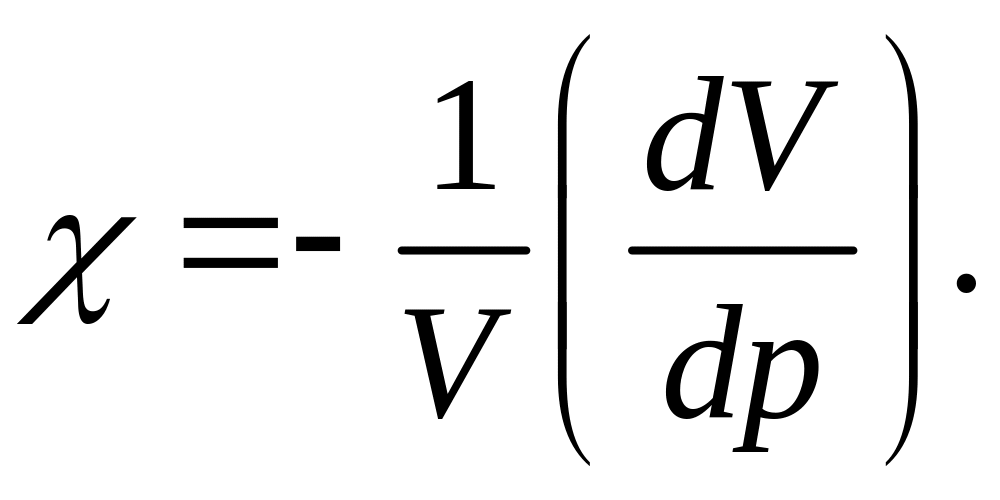 (3.44)
(3.44)
Тобто χ дорівнює відносній зміні об’єму газу, якщо його тиск змінюється на одиницю.
Розглядають ізотермічну χТ й адіабатичну χА стисливості газу. Скористаємось рівнянням стану газу і продиференціюємо його за умови Т=const:
![]() ,
(3.45)
,
(3.45)
звідки
 ,
отже, на підставі (3.45)
,
отже, на підставі (3.45)
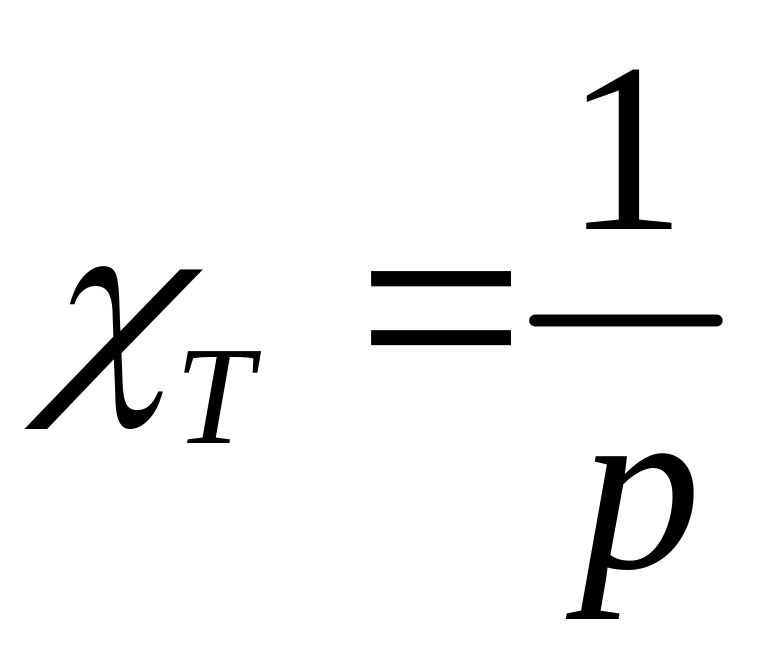 . (3.46)
. (3.46)
Коефіцієнт ізотермічної стисливості газу обернений до його тиску. Знак „мінус” означає, що зі збільшенням тиску об’єм газу зменшується.
В адіабатному процесі
![]() .
(3.47)
.
(3.47)
Продиференціюємо
(3.47), отримаємо
![]() dV=0,
звідки
dV=0,
звідки
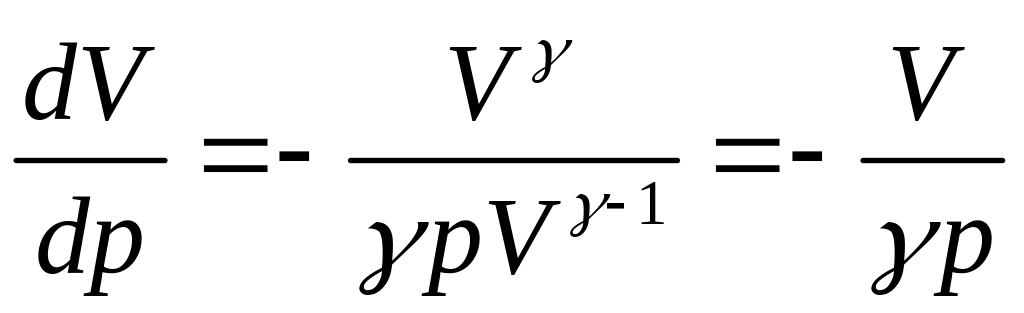 .
(3.48)
.
(3.48)
Отже, на підставі (3.46) і (3.48)
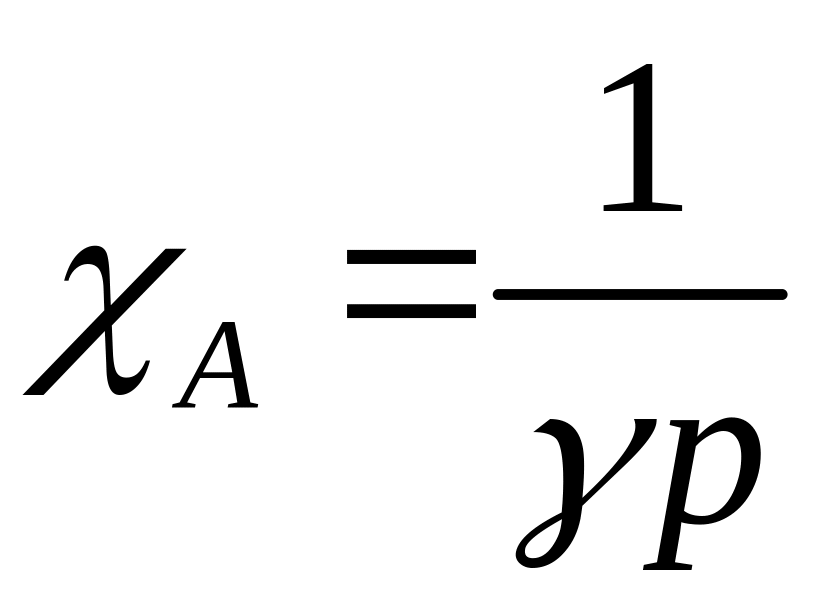 .
(3.49)
.
(3.49)
Як бачимо, адіабатична стисливість газу менша від ізотермічної:
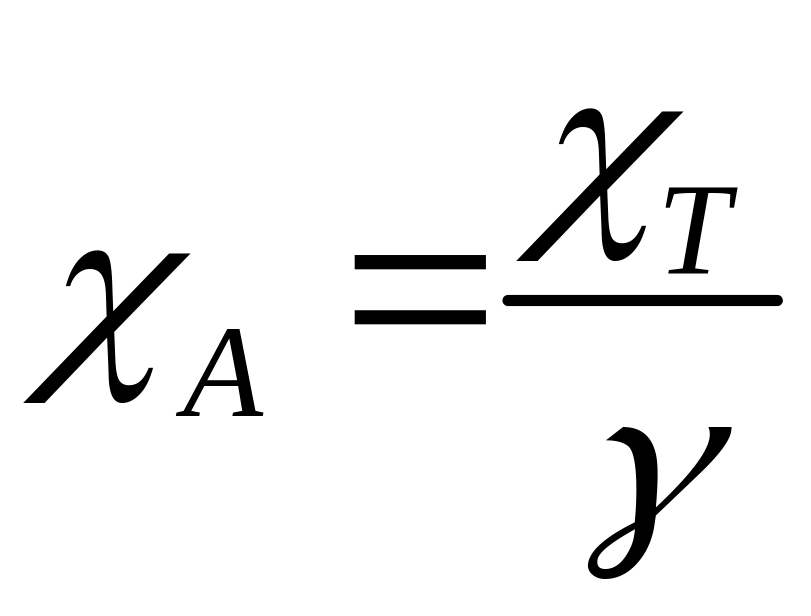 .
(3.50)
.
(3.50)
3.10. Ентропія
Під час розгляду першого закону термодинаміки (3.1) ми виявили, що лише зміна внутрішньої енергії dU є повним диференціалом. Це зумовлено тим, що внутрішня енергія – це функція стану термодинамічної системи, яка не залежить від способу переходу системи зі стану 1 у стан 2. Крім того, термодинаміка оперує іншими термодинамічними функціями, які є функціями стану системи. Одна з них – ентропія S.
Спробуємо, скориставшись (3.1) та (3.12), виділити один повний диференціал функції, що залежить від макропараметрів ідеального газу:
![]() .
(3.51)
.
(3.51)
Поділимо (3.51) на Т, отримаємо
![]() .
(3.52)
.
(3.52)
Як
бачимо, праворуч у рівнянні (3.52) маємо
повний диференціал, отже, і ліва частина
рівняння повинна бути повним диференціалом.
Функцію стану, повним диференціалом
якої є
![]() ,
називають ентропією
S,
отже,
,
називають ентропією
S,
отже,
![]() .
(3.53)
.
(3.53)
Фізичний зміст ентропії виражає формула Больцмана
S=к·lnW, (3.54)
де W – термодинамічна ймовірність.
Термодинамічна ймовірність W – це кількість мікростанів, які зумовлюють заданий макростан системи. На відміну від математичної ймовірності, яка не може бути більшою від одиниці, W може набувати будь-яких додатних значень.
Отже, ентропія S визначена логарифмом кількості мікростанів системи, за допомогою яких може бути реалізовано цей мікростан.
Ентропія має ще й статистичне тлумачення – вона є мірою розупорядкованості системи. Справді, зі збільшенням упорядкованості частинок системи кількість мікростанів зменшується, отже, зменшується й ентропія. Якщо система перебуває в стані термодинамічної рівноваги, то кількість мікростанів максимальна, отже, максимальною є ентропія системи.
З урахуванням ентропії рівняння (3.51) для оборотних процесів можна записати так:
![]() .
(3.55)
.
(3.55)
Це головна термодинамічна тотожність.
Для характеристики різноманітних термодинамічних процесів важли-вою є не ентропія системи, а її зміна. Щоб обчислити зміну ентропії у певному процесі, скористаємось (3.55):
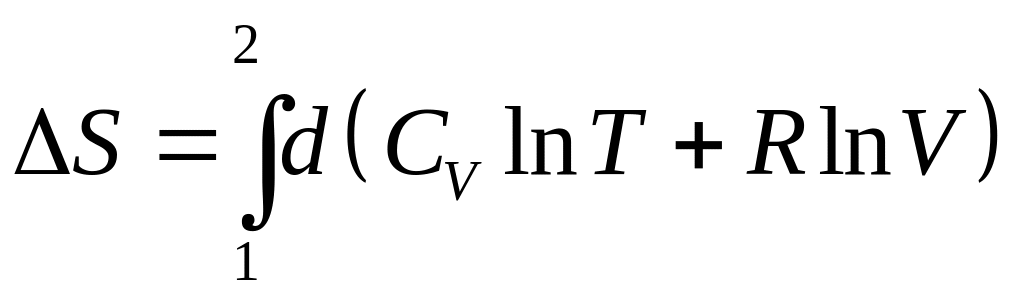 .
(3.56)
.
(3.56)
1. Ізотермічний процес:
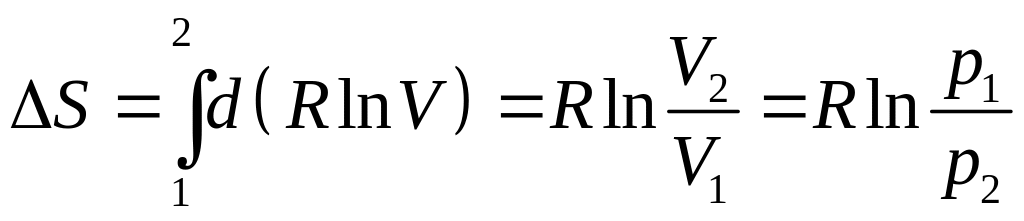 .
(3.57)
.
(3.57)
2. Ізохорний процес:
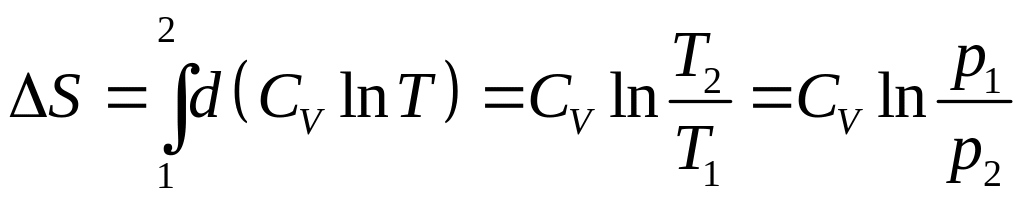 .
(3.58)
.
(3.58)
3. Ізобарний процес:
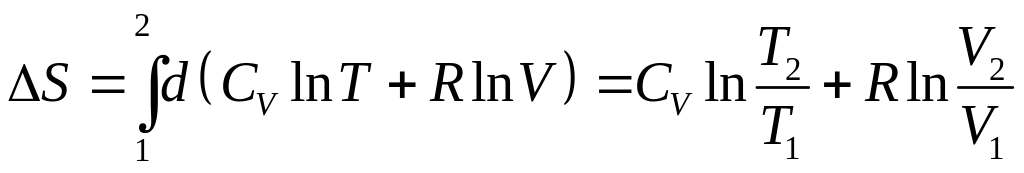 ,
(3.59)
,
(3.59)
однак
 ,
тоді
,
тоді
 .
(3.60)
.
(3.60)
4. Адіабатний процес:
ΔS=0, оскільки δQ=0.
Отже, адіабатний процес є ізоентропійним.
Зміна ентропії в необоротних процесах. Розглянемо зміну ентропії під час вирівнювання температури двох тіл, які перебувають у тепловому контакті. Нехай температура першого тіла Т1, а другого – Т2. Після контакту температура обох тіл Т3. Щоб визначити цю температуру скористаємось рівнянням теплового балансу
![]() ,
(3.61)
,
(3.61)
звідки
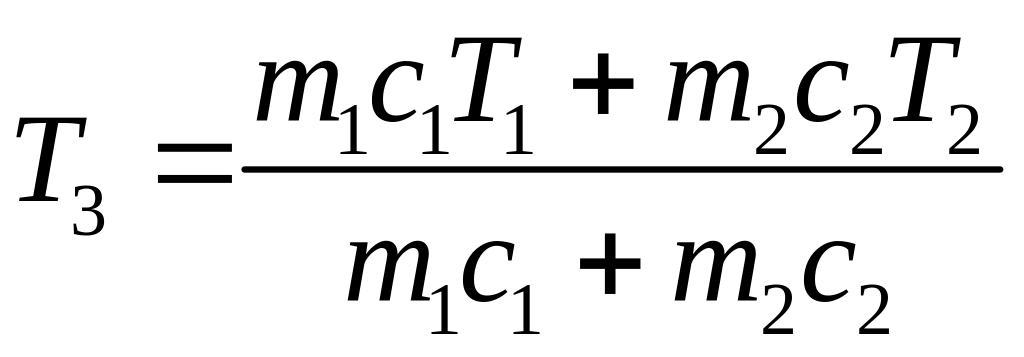 .
(3.62)
.
(3.62)
Тут m i c – маса і питома теплоємність кожного тіла.
Зміну ентропії в цьому нерівноважному процесі можна обчислити, звівши його до двох рівноважних процесів. Тоді
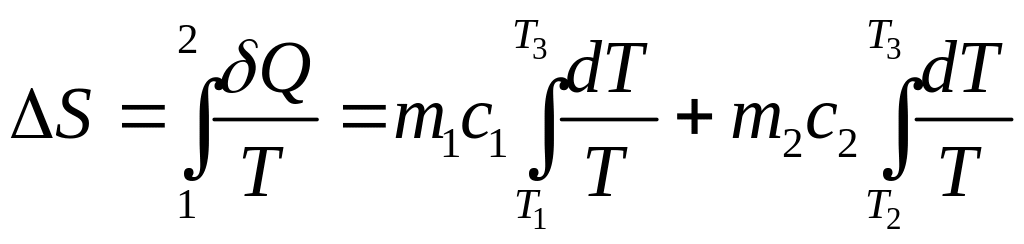 ,
,
звідки
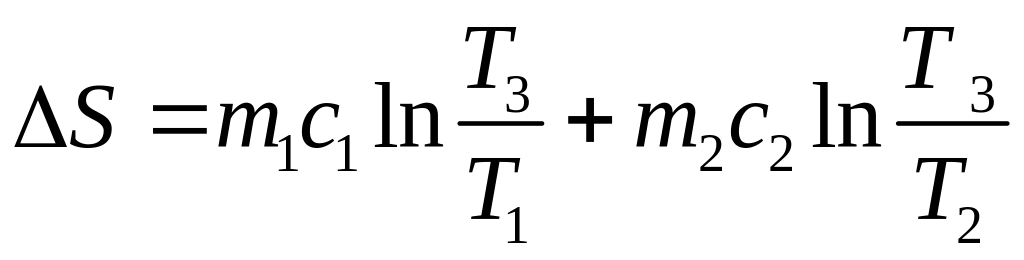 ,
(3.63)
,
(3.63)
Підставимо у (3.62) і (3.63), і переконаємось, що ΔS>0, тобто під час теплопередавання ентропія зростає.
Необоротними є також фазові переходи першого роду. Під час таких процесів зміну ентропії системи виражає формула
![]() ,
(3.64)
,
(3.64)
де q – питома теплота; Т – температура фазового переходу.
