
- •Молекулярна фізика. Лабораторний практикум
- •Перелік лабораторних робіт
- •Список рекомендованої літератури
- •Частина і. Молекулярна фізика. Розділ 1. Будова речовини
- •1.1. Модель речовини. Маси атомів і молекул
- •1.2. Сили міжмолекулярної взаємодії. Агрегатні стани речовини
- •1.3. Енергія міжмолекулярної взаємодії. Потенціал Ленарда–Джонса
- •1.4. Структура речовини
- •1.4.1. Газоподібний стан
- •1.4.2. Рідини
- •1.4.3. Тверді тіла
- •Розділ 2. Основи молекулярно-кінетичної теорії газів
- •2.1. Ідеальний газ. Ізопроцеси. Рівняння стану ідеального газу
- •2.2. Тиск і температура ідеального газу. Основне рівняння молекулярно-кінетичної теорії
- •2.3. Поняття про статистичний розподіл. Функції розподілу
- •2.3.1. Закони розподілу молекул ідеального газу за швидкостями й енергіями теплового руху (розподіл Максвелла)
- •2.3.2. Барометрична формула. Розподіл Больцмана
- •2.3.3. Розподіл Максвелла–Больцмана
- •2.3.4. Квантові аспекти розподілів. Розподіли Бозе–Айнштайна і Фермі–Дірака
- •2.4. Середня кількість зіткнень молекул. Середня довжина вільного пробігу
- •Розділ 3. Основи термодинаміки
- •3.1. Головні поняття й означення
- •3.2. Внутрішня енергія ідеального газу Молекули ідеального газу не взаємодіють на відстані, тому
- •Вище доведено, що середня кінетична енергія теплового руху молекули ідеального газу
- •3.3. Теплоємність ідеального газу
- •Для ізобарного процесу
- •3.4. Теплоємність рідин
- •3.5. Теплоємність твердих тіл
- •3.5.1. Класична теорія теплоємності твердих тіл
- •3.5.2. Квантові теорії теплоємності твердих тіл.
- •3.6. Адіабатний процес
- •3.7. Політропні процеси
- •3.8. Робота в термодинамічних процесах
- •3.9. Стисливість газів
- •3.10. Ентропія
- •3.11. Циклічні процеси. Теплові машини
- •Розділ 4. Реальні гази
- •4.1. Рівняння стану реального газу. Рівняння Ван-дер-Ваальса
- •4.2. Внутрішня енергія і теплоємність реального газу
- •Розділ 5. Поверхневий натяг. Капілярні явища
- •На підставі (5.3) рівняння (5.4) запишемо у вигляді
- •Розділ 6. Фазові переходи
- •6.1. Агрегатні стани і фази речовини
- •6.2. Фазові переходи першого і другого роду
- •Розділ 7. Явища перенесення
- •7.1. Самодифузія і взаємна дифузія
- •7.2. Теплопровідність
- •7.4. Розріджені гази. Вакуум
- •Частина іі. Молекулярна фізика. Лабораторний практикум. Лабораторна робота № 201. Визначення коефіцієнта в’язкості рідини методом стокса
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 202. Дослідження залежності коефіцієнта в’язкості рідини від температури
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 203. Визначення коефіцієнта в’язкості рідини за допомогою капілярного віскозиметра оствальда
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №205. Визначення коефіцієнта поверхневого натягу рідини методом відривання кільця
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 206. Дослідження залежності коефіцієнта поверхневого натягу рідини від температури методом максимального тиску в бульбашці
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №208. Дослідження теплового розширення металів
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №209. Визначення питомої теплоємності металів методом охолодження
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 210. Визначення сталої больцмана та універсальної газової сталої
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №211. Визначення середньої довжини вільного пробігу та ефективного діаметра молекул повітря
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 212 визначення співвідношення теплоємностей повітря сp/сv методом клемана–дезорма
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 213. Визначення співвідношення теплоємностей повітря ср / сv методом стоячої хвилі
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 214. Вимірювання вологості повітря психрометром
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 215. Дослідження критичного стану речовини
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №216. Дослідження процесу плавлення кристалічних речовин
- •Порядок виконання роботи
- •Контрольні запитання
- •Додатки Головні фізичні сталі
- •Густина твердих тіл . За температури 20ºС
- •Густина рідин за температури 20ºС
- •Густина газів
- •Додаток 4 Теплофізичні коефіцієнти твердих тіл
- •Додаток 5 Пружні властивості твердих тіл
- •Додаток 6 Коефіцієнти лінійного теплового розширення твердих тіл в інтервалі 0–100 ºС
- •Додаток 7 Швидкість поширення звуку в різних середовищах
- •Додаток 8 Деякі фізичні характеристики рідин
- •Додаток 11 Коефіцієнт об’ємного теплового розширення деяких рідин
Порядок виконання роботи
1. Записати вихідні дані експерименту: Т1= (... ± ...) К – кімнатна температура; P0= ( ... ± ... ) Н/м2 – атмосферний тиск.
2. Закрити кран 4, а кран 3 відкрити. За допомогою ручної помпи 2 нагнітати в балон 1 повітря, доки різниця рівнів води в манометрі 6 не досягне 15–18 см. Кран 3 одразу закрити.
3. Спостерігати 2–3 хв за рівнями води в колінах манометра. Коли рівні перестануть змінюватись, записати різницю рівнів h1 у таблицю.
4. За допомогою крана 4 з’єднати об’єм балона з атмосферою на 2–3 с, після чого кран 4 одразу закрити.
5. Спостерігати 2–3 хв за рівнями води в колінах манометра. Коли рівні перестануть змінюватись, записати різницю рівнів h2 у таблицю.
6. Повторити досліди згідно з пунктами 2–5 п’ять разів.
Номер за пор. |
h1, м |
h1, м |
h2, м |
h2, м |
1 |
|
|
|
|
…. |
|
|
|
|
С.з. |
|
|
|
|
7. За усередненими значеннями h1 і h2 розрахувати згідно з формулою (9).
8. Абсолютну похибку обчислити за формулою
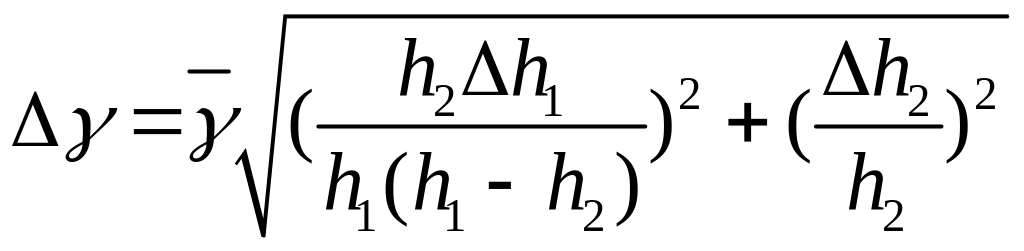 .
.
9. Записати кінцевий результат експерименту у вигляді
= ; E = …%.
Контрольні запитання
Сформулюйте і запишіть перший закон термодинаміки.
Поясніть причину зміни температури газу під час його адіабатичного розширення або стиснення.
Запишіть формулу для обчислення через ступені вільності молекул газу.
Дайте визначення молярної теплоємності газу за сталого об’єму і сталого тиску. Поясніть, чому СV < СР.
Виведіть і поясніть рівняння Майєра.
Запишіть і поясніть формулу, за якою обчислюють внутрішню енергію ідеального газу.
Чому повітря в нашому досліді можна наближено вважати двохатомним ідеальним газом?
Поясніть на графіку залежності р = f(V), у чому полягає відмінність між ізотермою й адіабатою.
Лабораторна робота № 213. Визначення співвідношення теплоємностей повітря ср / сv методом стоячої хвилі
Завдання: експериментально визначити співвідношення теплоєм-ностей повітря за сталого тиску і сталого об’єму методом стоячої хвилі.
Приладдя: установка для визначення довжини звукової хвилі в повітрі; генератор звукових коливань; телефон, мікрофон і осцилограф; барометр; термометр.
Теоретичний матеріал, який необхідно засвоїти під час підготовки до виконання роботи: ізопроцеси в ідеальному газі; адіабатичний процес; рівняння Пуассона; теплоємність, питома та молярна теплоємності; теплоємність за сталого тиску і сталого об’єму; звук та звукові хвилі; швидкість поширення звукових хвиль у різних середовищах, від чого вона залежить; утворення стоячої хвилі, вузли та пучності.
Література:
1. § 16.2–16.5, c. 285–304; § 12.1, c. 205–208;
2. § 18.6–18.8, c. 68–74;
3. § 45–46, с. 104–146; § 71–72, с. 223–232;
4. § 41, с.73–75; § 50–55, с. 88–96; § 157–158, с. 247–251.
Опис установки. Установка для визначення довжини звукової хвилі в по-вітрі показана на рис. 14. Вона складається зі скляної труби 2 та резервуара з водою 1, який через кран 9 приєднаний до ручної помпи 8. Уздовж труби
розташована
лінійка 5
з міліметровими поділками. Якщо нагнітати
воду в т
Рис. 14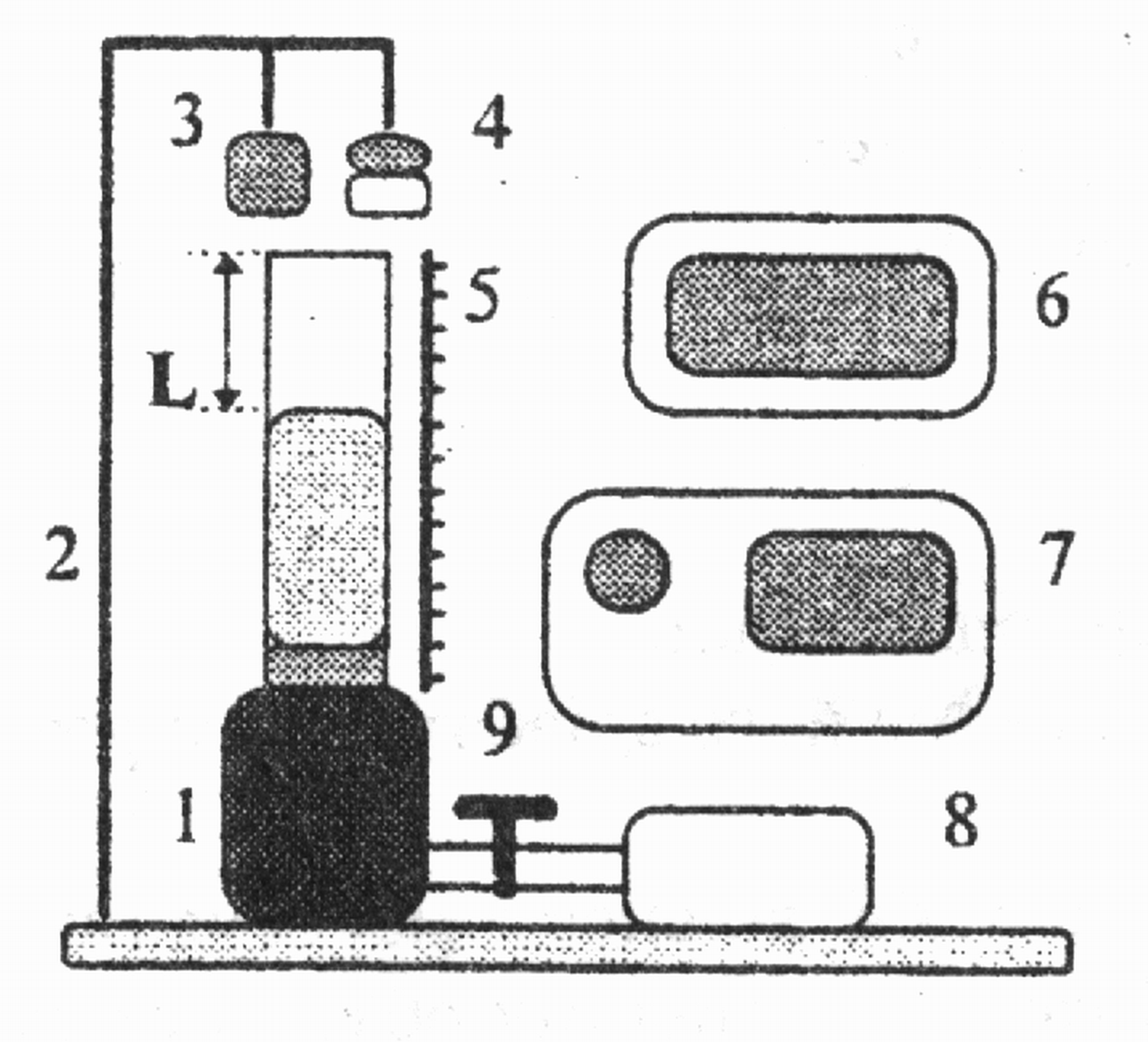
Ідея роботи та виведення робочої формули. Коливання мембрани телефону збуджують поздовжні коливання стовпа повітря у трубі, тобто звукова хвиля, яка поширюється в трубі, відбивається від поверхні води і йде у зворотному напрямі. У випадку накладання падаючої та відбитої хвиль утворюється стояча хвиля. Процес поширення поздовжньої хвилі в газі супроводжується утворенням зон стиску і розрідження, між якими за великих частот теплообміну практично нема. З огляду на це процес поширення звукових хвиль у повітрі можна розглядати як адіабатичний, який описує рівняння Пуассона
PV = const, (1)
де = Ср /СV – співвідношення питомих теплоємностей газу за сталого тиску й об’єму.
Швидкість поширення звукової хвилі в повітрі залежить від його фізичних властивостей:
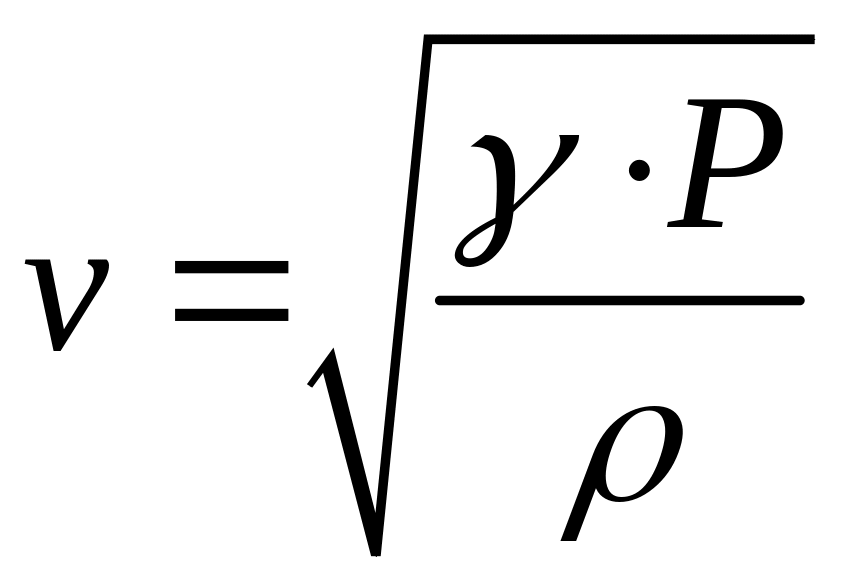 ,
(2)
,
(2)
де P – тиск; – густина повітря за заданої температури t°.
Зазначимо, що густина повітря залежить від температури
![]() ,
(3)
,
(3)
де 0 – густина повітря за 0°С; – температурний коефіцієнт об’ємного розширення повітря.
Підставимо (3) в (2) і розв’яжемо отримане рівняння щодо , матимемо
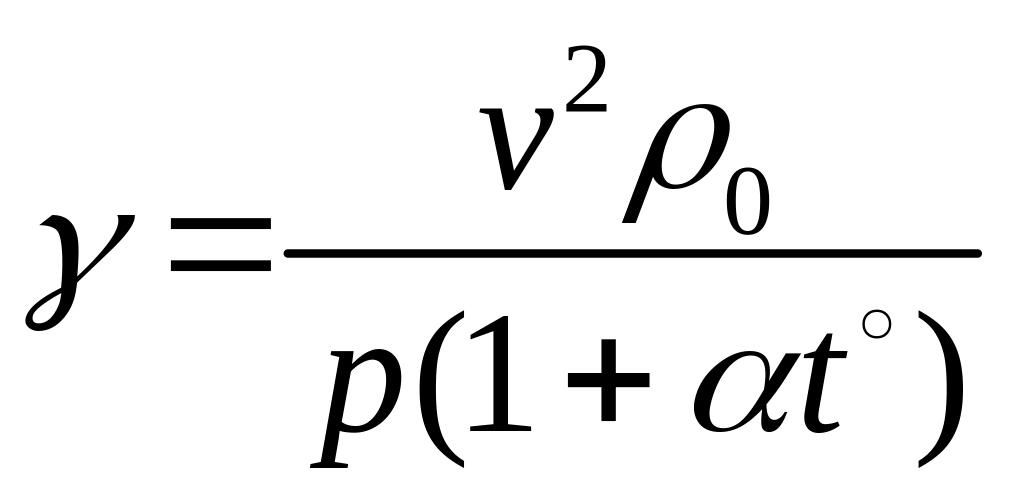 .
(4)
.
(4)
Д
Рис. 15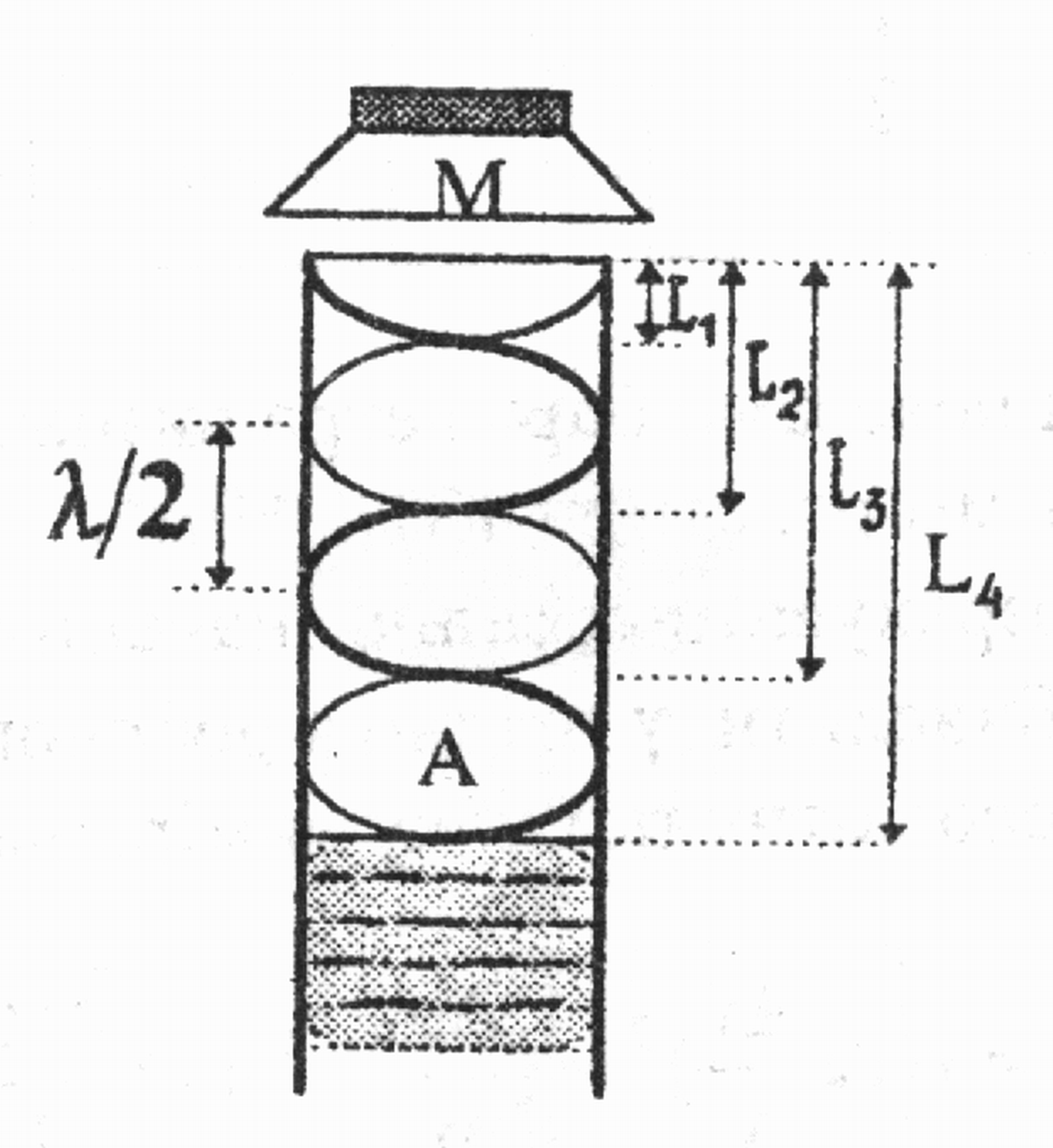
Ln = (2n–1) /4, (5)
де n – порядок підсилення (n = 1,2,3...). Очевидно, що наступне підсилення простежуватиметься тоді, коли
Ln+1 = [(2n+1) –1] /4. (6)
Відстань між двома наступними підсиленнями звуку
Ln+1 – Ln = /2. (7)
Поряд з цим відомо, що довжина хвилі пов’язана зі швидкістю її поширення v та частотою таким співвідношенням:
= v/ . (8)
Із (7) і (8) отримаємо
v = 2(Ln+1 – Ln) . (9)
Підставимо (9) у формулу (4), знайдемо
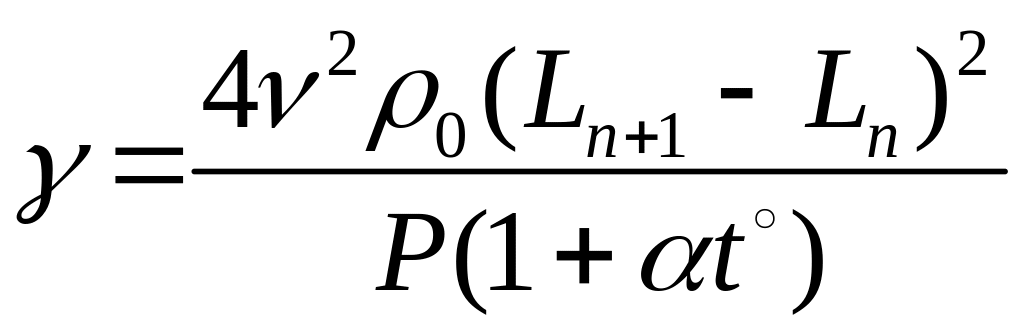 .
(10)
.
(10)
Це і є робоча формула лабораторної роботи.
