
- •Молекулярна фізика. Лабораторний практикум
- •Перелік лабораторних робіт
- •Список рекомендованої літератури
- •Частина і. Молекулярна фізика. Розділ 1. Будова речовини
- •1.1. Модель речовини. Маси атомів і молекул
- •1.2. Сили міжмолекулярної взаємодії. Агрегатні стани речовини
- •1.3. Енергія міжмолекулярної взаємодії. Потенціал Ленарда–Джонса
- •1.4. Структура речовини
- •1.4.1. Газоподібний стан
- •1.4.2. Рідини
- •1.4.3. Тверді тіла
- •Розділ 2. Основи молекулярно-кінетичної теорії газів
- •2.1. Ідеальний газ. Ізопроцеси. Рівняння стану ідеального газу
- •2.2. Тиск і температура ідеального газу. Основне рівняння молекулярно-кінетичної теорії
- •2.3. Поняття про статистичний розподіл. Функції розподілу
- •2.3.1. Закони розподілу молекул ідеального газу за швидкостями й енергіями теплового руху (розподіл Максвелла)
- •2.3.2. Барометрична формула. Розподіл Больцмана
- •2.3.3. Розподіл Максвелла–Больцмана
- •2.3.4. Квантові аспекти розподілів. Розподіли Бозе–Айнштайна і Фермі–Дірака
- •2.4. Середня кількість зіткнень молекул. Середня довжина вільного пробігу
- •Розділ 3. Основи термодинаміки
- •3.1. Головні поняття й означення
- •3.2. Внутрішня енергія ідеального газу Молекули ідеального газу не взаємодіють на відстані, тому
- •Вище доведено, що середня кінетична енергія теплового руху молекули ідеального газу
- •3.3. Теплоємність ідеального газу
- •Для ізобарного процесу
- •3.4. Теплоємність рідин
- •3.5. Теплоємність твердих тіл
- •3.5.1. Класична теорія теплоємності твердих тіл
- •3.5.2. Квантові теорії теплоємності твердих тіл.
- •3.6. Адіабатний процес
- •3.7. Політропні процеси
- •3.8. Робота в термодинамічних процесах
- •3.9. Стисливість газів
- •3.10. Ентропія
- •3.11. Циклічні процеси. Теплові машини
- •Розділ 4. Реальні гази
- •4.1. Рівняння стану реального газу. Рівняння Ван-дер-Ваальса
- •4.2. Внутрішня енергія і теплоємність реального газу
- •Розділ 5. Поверхневий натяг. Капілярні явища
- •На підставі (5.3) рівняння (5.4) запишемо у вигляді
- •Розділ 6. Фазові переходи
- •6.1. Агрегатні стани і фази речовини
- •6.2. Фазові переходи першого і другого роду
- •Розділ 7. Явища перенесення
- •7.1. Самодифузія і взаємна дифузія
- •7.2. Теплопровідність
- •7.4. Розріджені гази. Вакуум
- •Частина іі. Молекулярна фізика. Лабораторний практикум. Лабораторна робота № 201. Визначення коефіцієнта в’язкості рідини методом стокса
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 202. Дослідження залежності коефіцієнта в’язкості рідини від температури
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 203. Визначення коефіцієнта в’язкості рідини за допомогою капілярного віскозиметра оствальда
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №205. Визначення коефіцієнта поверхневого натягу рідини методом відривання кільця
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 206. Дослідження залежності коефіцієнта поверхневого натягу рідини від температури методом максимального тиску в бульбашці
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №208. Дослідження теплового розширення металів
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №209. Визначення питомої теплоємності металів методом охолодження
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 210. Визначення сталої больцмана та універсальної газової сталої
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №211. Визначення середньої довжини вільного пробігу та ефективного діаметра молекул повітря
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 212 визначення співвідношення теплоємностей повітря сp/сv методом клемана–дезорма
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 213. Визначення співвідношення теплоємностей повітря ср / сv методом стоячої хвилі
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 214. Вимірювання вологості повітря психрометром
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 215. Дослідження критичного стану речовини
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №216. Дослідження процесу плавлення кристалічних речовин
- •Порядок виконання роботи
- •Контрольні запитання
- •Додатки Головні фізичні сталі
- •Густина твердих тіл . За температури 20ºС
- •Густина рідин за температури 20ºС
- •Густина газів
- •Додаток 4 Теплофізичні коефіцієнти твердих тіл
- •Додаток 5 Пружні властивості твердих тіл
- •Додаток 6 Коефіцієнти лінійного теплового розширення твердих тіл в інтервалі 0–100 ºС
- •Додаток 7 Швидкість поширення звуку в різних середовищах
- •Додаток 8 Деякі фізичні характеристики рідин
- •Додаток 11 Коефіцієнт об’ємного теплового розширення деяких рідин
Порядок виконання роботи
Записати вихідні дані: початкову довжину стрижня l0 (зазначена в паспорті установки) і значення кімнатної температури t1°С.
Шток індикатора зміни довжини 6 сконтактувати з правим кінцем стрижня. Повертанням шкали індикатора встановити його стрілку на позначці «0».
Вимикачем 4 увімкнути живлення потенціометра 5, а вимикачем 2 – нагрівник. За умови підвищення температури стрижня до 30°С записати покази індикатора l.
Записати покази індикатора за кожного наступного підвищення температури на 10°С (за 40, 50 ... 120°С). Досягнувши температури 120°С, вимкнути нагрівник вимикачем 2.
Результати вимірювань записати в таблицю:
Номер За пор. |
t, °С |
l, мм |
105, (°С)-1 |
105, (°С)-1 |
1 |
|
|
|
|
.... |
|
|
|
|
Похибку вимірювань обчислити за формулою
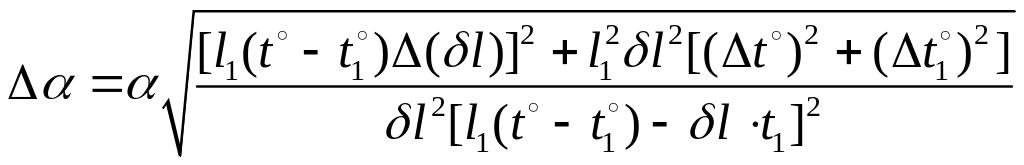 .
.
Похибки (l), t i t1 обчислити як похибки вимірювальних приладів.
Записати кінцевий результат для температурного коефіцієнта лінійного розширення у вигляді
= ( ), Е =...%.
8. На міліметровому папері побудувати графік залежності = f(t°С).
Контрольні запитання
У чому полягає подібність і відмінність теплового руху молекул газів, рідин і твердих кристалічних тіл?
Сформулюйте основні положення молекулярно-кінетичної теорії.
Зобразіть графічно залежність сили і потенціальної енергії взаємодії двох молекул від відстані між ними.
У чому полягає фізичний зміст температурного коефіцієнта лінійного розширення?
Що називають коефіцієнтом об’ємного розширення?
Зобразіть графічно залежність видовження твердого тіла від температури.
Чи змінюється густина тіла з температурою?
Тіла внаслідок нагрівання, як звичайно, розширюються. Чи є винятки з цього правила?
Наведіть приклади застосування явища теплового розширення твердих тіл.
Лабораторна робота №209. Визначення питомої теплоємності металів методом охолодження
Завдання: експериментально визначити питому теплоємність заліза й алюмінію за різних температур.
Приладдя: досліджувані зразки (циліндри з різних металів, Сu, Fе, Аl); електричний термометр (термопара з потенціометром, шкала якого програ-дуйована в градусах Цельсія); електрична піч; секундомір.
Теоретичний матеріал, який необхідно опрацювати під час підготовки до виконання роботи: перший закон термодинаміки; теплоємність; питома теплоємність; рівняння теплопровідності; теплоємність за сталого тиску і сталого об’єму; закон Дюлонга i Пті.
Література:
1) § 18.6, c. 361–364;
2) § 20.6, c. 114–118;
3) § 70, с. 164–166; § 97–99, с. 218–224;
4) § 70, с. 116; § 73, с. 122–123; § 103, с. 166.
О
Рис. 9
Ідея роботи та виведення робочої формули. Зміну внутрішньої енергії тіла в процесі, під час якого механічна робота не виконується, називають теплопередаванням. Якщо термодинамічна система складається з кількох тіл, які мають різну температуру, то вона намагатиметься перейти в стан термодинамічної рівноваги. В цьому процесі більш нагріті тіла будуть охолоджуватись, а менш нагріті – нагріватись, причому швидкість охолод-ження (нагрівання) тіла залежатиме від його теплоємності.
Розглянемо процес охолодження невеликого металевого зразка, нагрітого до температури Т. Нехай dq – кількість теплоти, яку віддає метал з масою m під час охолодження на dT. Тоді dq=cmdT, або
dq=cVdT, (1)
де с – теплоємність металу; – його густина; V – об’єм зразка.
Якщо охолодження відбувається протягом часу dt, то (1) можна записати у вигляді
![]() ,
(2)
,
(2)
де dT/dt – швидкість охолодження зразка.
Величину dq можна також визначити за формулою Ньютона, яка описує процес охолодження тіла:
dq=(T–T0)Sdt, (3)
де – коефіцієнт теплопередавання; S – площа поверхні тіла; Т0 – температура навколишнього середовища.
Прирівняємо (2) і (3), отримаємо
![]() .
(4)
.
(4)
Рівняння (4) є вихідним для виведення робочої формули.
В експерименті використовують три металеві зразки (мідний, залізний і алюмінієвий), однакові за розмірами. В цьому випадку їхні площі поверхонь, об’єми і коефіцієнти теплопередавання будуть однакові, тобто
S1=S2=S3, V1=V2=V3, 1=2=3.
Нехай теплоємність міді c1 відома. Тоді, записавши рівняння (4) для кожного з досліджуваних зразків і розв’язавши одержану систему рівнянь, отримаємо робочу формулу для визначення невідомої теплоємності металу cx через теплоємність міді:
 .
(5)
.
(5)
У формулі (5) швидкість охолодження зразка dT/dt за температури Т визначають графічно. Вираз (5) є робочою формулою лабораторної роботи.
