
- •Молекулярна фізика. Лабораторний практикум
- •Перелік лабораторних робіт
- •Список рекомендованої літератури
- •Частина і. Молекулярна фізика. Розділ 1. Будова речовини
- •1.1. Модель речовини. Маси атомів і молекул
- •1.2. Сили міжмолекулярної взаємодії. Агрегатні стани речовини
- •1.3. Енергія міжмолекулярної взаємодії. Потенціал Ленарда–Джонса
- •1.4. Структура речовини
- •1.4.1. Газоподібний стан
- •1.4.2. Рідини
- •1.4.3. Тверді тіла
- •Розділ 2. Основи молекулярно-кінетичної теорії газів
- •2.1. Ідеальний газ. Ізопроцеси. Рівняння стану ідеального газу
- •2.2. Тиск і температура ідеального газу. Основне рівняння молекулярно-кінетичної теорії
- •2.3. Поняття про статистичний розподіл. Функції розподілу
- •2.3.1. Закони розподілу молекул ідеального газу за швидкостями й енергіями теплового руху (розподіл Максвелла)
- •2.3.2. Барометрична формула. Розподіл Больцмана
- •2.3.3. Розподіл Максвелла–Больцмана
- •2.3.4. Квантові аспекти розподілів. Розподіли Бозе–Айнштайна і Фермі–Дірака
- •2.4. Середня кількість зіткнень молекул. Середня довжина вільного пробігу
- •Розділ 3. Основи термодинаміки
- •3.1. Головні поняття й означення
- •3.2. Внутрішня енергія ідеального газу Молекули ідеального газу не взаємодіють на відстані, тому
- •Вище доведено, що середня кінетична енергія теплового руху молекули ідеального газу
- •3.3. Теплоємність ідеального газу
- •Для ізобарного процесу
- •3.4. Теплоємність рідин
- •3.5. Теплоємність твердих тіл
- •3.5.1. Класична теорія теплоємності твердих тіл
- •3.5.2. Квантові теорії теплоємності твердих тіл.
- •3.6. Адіабатний процес
- •3.7. Політропні процеси
- •3.8. Робота в термодинамічних процесах
- •3.9. Стисливість газів
- •3.10. Ентропія
- •3.11. Циклічні процеси. Теплові машини
- •Розділ 4. Реальні гази
- •4.1. Рівняння стану реального газу. Рівняння Ван-дер-Ваальса
- •4.2. Внутрішня енергія і теплоємність реального газу
- •Розділ 5. Поверхневий натяг. Капілярні явища
- •На підставі (5.3) рівняння (5.4) запишемо у вигляді
- •Розділ 6. Фазові переходи
- •6.1. Агрегатні стани і фази речовини
- •6.2. Фазові переходи першого і другого роду
- •Розділ 7. Явища перенесення
- •7.1. Самодифузія і взаємна дифузія
- •7.2. Теплопровідність
- •7.4. Розріджені гази. Вакуум
- •Частина іі. Молекулярна фізика. Лабораторний практикум. Лабораторна робота № 201. Визначення коефіцієнта в’язкості рідини методом стокса
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 202. Дослідження залежності коефіцієнта в’язкості рідини від температури
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 203. Визначення коефіцієнта в’язкості рідини за допомогою капілярного віскозиметра оствальда
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №205. Визначення коефіцієнта поверхневого натягу рідини методом відривання кільця
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 206. Дослідження залежності коефіцієнта поверхневого натягу рідини від температури методом максимального тиску в бульбашці
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №208. Дослідження теплового розширення металів
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №209. Визначення питомої теплоємності металів методом охолодження
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 210. Визначення сталої больцмана та універсальної газової сталої
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №211. Визначення середньої довжини вільного пробігу та ефективного діаметра молекул повітря
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 212 визначення співвідношення теплоємностей повітря сp/сv методом клемана–дезорма
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 213. Визначення співвідношення теплоємностей повітря ср / сv методом стоячої хвилі
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 214. Вимірювання вологості повітря психрометром
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 215. Дослідження критичного стану речовини
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №216. Дослідження процесу плавлення кристалічних речовин
- •Порядок виконання роботи
- •Контрольні запитання
- •Додатки Головні фізичні сталі
- •Густина твердих тіл . За температури 20ºС
- •Густина рідин за температури 20ºС
- •Густина газів
- •Додаток 4 Теплофізичні коефіцієнти твердих тіл
- •Додаток 5 Пружні властивості твердих тіл
- •Додаток 6 Коефіцієнти лінійного теплового розширення твердих тіл в інтервалі 0–100 ºС
- •Додаток 7 Швидкість поширення звуку в різних середовищах
- •Додаток 8 Деякі фізичні характеристики рідин
- •Додаток 11 Коефіцієнт об’ємного теплового розширення деяких рідин
1.3. Енергія міжмолекулярної взаємодії. Потенціал Ленарда–Джонса
Точну характеристику залежності Еп(r) можна дати лише для конкретних молекул. У загальному
![]() .
(1.5)
.
(1.5)
Дослідження доводять, що для молекул рідин і газів достатньо добре наближення отримують за умови n=12, m=6. Тоді, записавши (1.5) через потенціал парної взаємодії φ(r), отримаємо
![]() ,
(1.6)
,
(1.6)
де перший доданок відповідає відштовхуванню, а другий – притяганню молекул, σ – найменша відстань зближення молекул, коли φ(σ)=0.
Вираз (1.6) називають потенціалом Леонарда–Джонса. Зазначимо, що формула (1.6) враховує взаємодію лише двох молекул, що можливо тільки для газів. У рідинах треба враховувати вплив сусідніх молекул, що суттєво ускладнює задачу. Водночас потенціал Ленарда–Джонса повністю придатний для наближеної оцінки сил і потенціалу взаємодії.
Спробуємо скористатись виразом (1.6), щоб оцінити залежність ван-дер-ваальсівських сил від відстані між молекулами.
На підставі рис. 1.3 запишемо напруженість електричного поля, створеного першим диполем на відстані r:
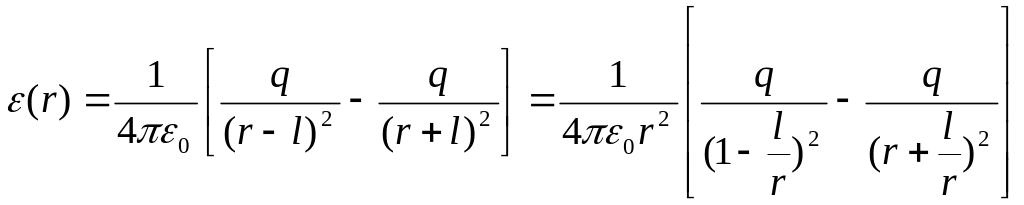 .
(1.7)
.
(1.7)
Оскільки
 і
і
![]() ,
то
,
то
![]() .
(1.8)
.
(1.8)
Обчислимо тепер силу, з якою це поле діє на другу поляризовану молекулу:
![]()
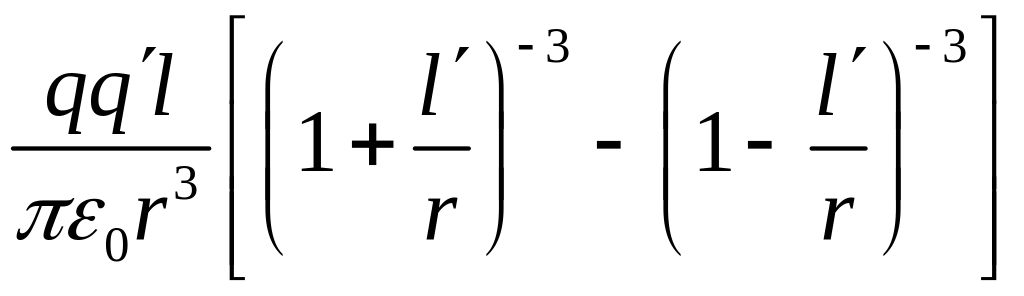 . (1.9)
. (1.9)
Оскільки
![]() і
і
![]() ,
то
,
то
![]() .
(1.10)
.
(1.10)
З
урахуванням того, що поляризованість
молекули прямо пропорційна до напруженості
поля ε,
тобто
![]() ~
ε
~
~
ε
~![]() ,
отримаємо
,
отримаємо
![]() ~
~![]() .
(1.11)
.
(1.11)
Отже ван-дер-ваальсівська сила притягування двох молекул дуже швидко зменшується зі збільшенням відстані між ними.
1.4. Структура речовини
Будь-яка речовина залежно від температури і тиску може перебувати в одному із трьох агрегатних станів: твердому, рідкому або газоподібному. Властивості речовини та її внутрішня молекулярна структура є різними у кожному з агрегатних станів і визначені, головно характером міжмолекулярної взаємодії.
1.4.1. Газоподібний стан
Рис. 1.4. Хаотично-поступальний рух
молекули газу
![]() ~kT).
Зокрема, у газоподібному стані
значно більша від потенціальної енергії
міжмолекулярної взаємодії (
>>
~kT).
Зокрема, у газоподібному стані
значно більша від потенціальної енергії
міжмолекулярної взаємодії (
>>![]() ),
тому молекули газу рухаються поступально,
взаємодіючи лише під час зіткнень.
Зіткнення молекул зумовлюють зміни
їхньої
кінетичної енергії
та імпульсу, тому характер руху молекул
газу хаотично-поступальний (рис. 1.4). Від
зіткнення до зіткнення молекули рухаються
незалежно одна від одної рівномірно і
прямолінійно. Такий характер руху і
взаємодії молекул газу спричинює те,
що речовина в газоподібному стані не
зберігає своєї форми й об’єму і не має
власної структури. Газоподібний стан
– це безструктурний стан речовини.
),
тому молекули газу рухаються поступально,
взаємодіючи лише під час зіткнень.
Зіткнення молекул зумовлюють зміни
їхньої
кінетичної енергії
та імпульсу, тому характер руху молекул
газу хаотично-поступальний (рис. 1.4). Від
зіткнення до зіткнення молекули рухаються
незалежно одна від одної рівномірно і
прямолінійно. Такий характер руху і
взаємодії молекул газу спричинює те,
що речовина в газоподібному стані не
зберігає своєї форми й об’єму і не має
власної структури. Газоподібний стан
– це безструктурний стан речовини.
1.4.2. Рідини
У рідинах
середня відстань між молекулами суттєво
менша, ніж у газах, тому сили і потенціальна
енергія міжмолекулярної взаємодії
достатньо великі. Для молекул рідини
середня кінетична енергія теплового
руху kT
сумірна з потенціальною енергією парної
взаємодії (
![]() ).
За таких умов сума кінетичної та
потенціальної енергії конкретної пари
молекул може стати від’ємною. Система
таких молекул уже не може самовільно
розсіюватись в об’ємі та перебуває у
зв’язаному стані. Молекули рідини,
маючи від’ємну енергію, виконують
коливальні рухи навколо тимчасових
положень рівноваги. Та оскільки
).
За таких умов сума кінетичної та
потенціальної енергії конкретної пари
молекул може стати від’ємною. Система
таких молекул уже не може самовільно
розсіюватись в об’ємі та перебуває у
зв’язаному стані. Молекули рідини,
маючи від’ємну енергію, виконують
коливальні рухи навколо тимчасових
положень рівноваги. Та оскільки
![]() ,
то молекули, які мають надлишок кінетичної
енергії (
>
),
можуть „перестрибувати” у нове
рівноважне положення, виконуючи навколо
нього подальші коливальні рухи. Такий
стрибкоподібний рух молекул однаково
ймовірний
у всіх напрямах. Отже, для молекул рідини
характерний коливально-поступальний
рух (рис. 1.5). Згідно з трактуваннями Я.
Френкеля, час „осілого життя” τ,
тобто час, протягом якого молекула
рідини коливається навколо положення
рівноваги,
,
то молекули, які мають надлишок кінетичної
енергії (
>
),
можуть „перестрибувати” у нове
рівноважне положення, виконуючи навколо
нього подальші коливальні рухи. Такий
стрибкоподібний рух молекул однаково
ймовірний
у всіх напрямах. Отже, для молекул рідини
характерний коливально-поступальний
рух (рис. 1.5). Згідно з трактуваннями Я.
Френкеля, час „осілого життя” τ,
тобто час, протягом якого молекула
рідини коливається навколо положення
рівноваги,
![]() , (1.12)
, (1.12)
д
Рис. 1.5. Коливально-поступальний
рух молекули рідини
![]() – період коливань молекули; U
– висота потенціального бар’єра; T
– абсолютна
темпера-тура.
– період коливань молекули; U
– висота потенціального бар’єра; T
– абсолютна
темпера-тура.
За висоту
потенціального бар’єра U
приймають мінімальну енергію, яку
потрібно надати молекулі для
„перестрибування” з одного положення
рівноваги в інше. Зокрема, за кімнатної
температури для молекул води
![]() ,
а
,
а
![]() .
Від часу „осілого життя” залежать такі
властивості рідин, як в’язкість та
дифузія.
.
Від часу „осілого життя” залежать такі
властивості рідин, як в’язкість та
дифузія.
Н
Рис. 1.6. Функція радіального розподілу
середньої густини молекул в рідині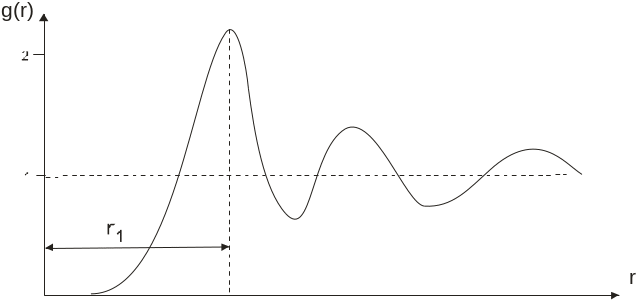
![]() , (1.13)
, (1.13)
д
Рис. 1.7. Визначення ближчої
міжатомної відстані

![]() і координатного числа r
і координатного числа r![]() – середня густина молекул у сферичному
шарі радіуса r
товщини dr;
– середня густина молекул у сферичному
шарі радіуса r
товщини dr;
![]() – середня густина молекул за умови
рівно-мірного розподілу по об’єму V.
На рис. 1.6 показана експериментальна
залежність g(r),
характерна для рідин. Як бачимо, функція
g(r)
має кілька максимумів, осцилюючи відносно
одиниці. Максимуми на графіку відповідають
найімовірні-шим відстаням між молекулами
рідини. На практиці в рентгенографії
рідин частіше використовують функцію
– середня густина молекул за умови
рівно-мірного розподілу по об’єму V.
На рис. 1.6 показана експериментальна
залежність g(r),
характерна для рідин. Як бачимо, функція
g(r)
має кілька максимумів, осцилюючи відносно
одиниці. Максимуми на графіку відповідають
найімовірні-шим відстаням між молекулами
рідини. На практиці в рентгенографії
рідин частіше використовують функцію
![]() ,
графік якої зображено на рис. 1.7. За цим
графіком визначають кількісні параметри
ближнього порядку рідини, зокрема,
найближчу міжатомну відстань r1
і координаційне число Z1.
Координаційному числу Z1
(кількості атомів у першій координаційній
сфері) відповідає площа під першим
максимумом, а найближчій міжатомній
відстані r1
– відстань від початку координат до
першого максимуму.
,
графік якої зображено на рис. 1.7. За цим
графіком визначають кількісні параметри
ближнього порядку рідини, зокрема,
найближчу міжатомну відстань r1
і координаційне число Z1.
Координаційному числу Z1
(кількості атомів у першій координаційній
сфері) відповідає площа під першим
максимумом, а найближчій міжатомній
відстані r1
– відстань від початку координат до
першого максимуму.
Сучасна наука розглядає рідину як систему, що має структуру ближнього порядку і складається з багатьох молекул, що рухаються коливально-поступально і взаємодіють між собою. Фізичні властивості і структура рідин суттєво залежать від характеру міжмолекулярних зв’язків та хімічного складу рідини.
