
- •Молекулярна фізика. Лабораторний практикум
- •Перелік лабораторних робіт
- •Список рекомендованої літератури
- •Частина і. Молекулярна фізика. Розділ 1. Будова речовини
- •1.1. Модель речовини. Маси атомів і молекул
- •1.2. Сили міжмолекулярної взаємодії. Агрегатні стани речовини
- •1.3. Енергія міжмолекулярної взаємодії. Потенціал Ленарда–Джонса
- •1.4. Структура речовини
- •1.4.1. Газоподібний стан
- •1.4.2. Рідини
- •1.4.3. Тверді тіла
- •Розділ 2. Основи молекулярно-кінетичної теорії газів
- •2.1. Ідеальний газ. Ізопроцеси. Рівняння стану ідеального газу
- •2.2. Тиск і температура ідеального газу. Основне рівняння молекулярно-кінетичної теорії
- •2.3. Поняття про статистичний розподіл. Функції розподілу
- •2.3.1. Закони розподілу молекул ідеального газу за швидкостями й енергіями теплового руху (розподіл Максвелла)
- •2.3.2. Барометрична формула. Розподіл Больцмана
- •2.3.3. Розподіл Максвелла–Больцмана
- •2.3.4. Квантові аспекти розподілів. Розподіли Бозе–Айнштайна і Фермі–Дірака
- •2.4. Середня кількість зіткнень молекул. Середня довжина вільного пробігу
- •Розділ 3. Основи термодинаміки
- •3.1. Головні поняття й означення
- •3.2. Внутрішня енергія ідеального газу Молекули ідеального газу не взаємодіють на відстані, тому
- •Вище доведено, що середня кінетична енергія теплового руху молекули ідеального газу
- •3.3. Теплоємність ідеального газу
- •Для ізобарного процесу
- •3.4. Теплоємність рідин
- •3.5. Теплоємність твердих тіл
- •3.5.1. Класична теорія теплоємності твердих тіл
- •3.5.2. Квантові теорії теплоємності твердих тіл.
- •3.6. Адіабатний процес
- •3.7. Політропні процеси
- •3.8. Робота в термодинамічних процесах
- •3.9. Стисливість газів
- •3.10. Ентропія
- •3.11. Циклічні процеси. Теплові машини
- •Розділ 4. Реальні гази
- •4.1. Рівняння стану реального газу. Рівняння Ван-дер-Ваальса
- •4.2. Внутрішня енергія і теплоємність реального газу
- •Розділ 5. Поверхневий натяг. Капілярні явища
- •На підставі (5.3) рівняння (5.4) запишемо у вигляді
- •Розділ 6. Фазові переходи
- •6.1. Агрегатні стани і фази речовини
- •6.2. Фазові переходи першого і другого роду
- •Розділ 7. Явища перенесення
- •7.1. Самодифузія і взаємна дифузія
- •7.2. Теплопровідність
- •7.4. Розріджені гази. Вакуум
- •Частина іі. Молекулярна фізика. Лабораторний практикум. Лабораторна робота № 201. Визначення коефіцієнта в’язкості рідини методом стокса
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 202. Дослідження залежності коефіцієнта в’язкості рідини від температури
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 203. Визначення коефіцієнта в’язкості рідини за допомогою капілярного віскозиметра оствальда
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №205. Визначення коефіцієнта поверхневого натягу рідини методом відривання кільця
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 206. Дослідження залежності коефіцієнта поверхневого натягу рідини від температури методом максимального тиску в бульбашці
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №208. Дослідження теплового розширення металів
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №209. Визначення питомої теплоємності металів методом охолодження
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 210. Визначення сталої больцмана та універсальної газової сталої
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №211. Визначення середньої довжини вільного пробігу та ефективного діаметра молекул повітря
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 212 визначення співвідношення теплоємностей повітря сp/сv методом клемана–дезорма
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 213. Визначення співвідношення теплоємностей повітря ср / сv методом стоячої хвилі
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 214. Вимірювання вологості повітря психрометром
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 215. Дослідження критичного стану речовини
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №216. Дослідження процесу плавлення кристалічних речовин
- •Порядок виконання роботи
- •Контрольні запитання
- •Додатки Головні фізичні сталі
- •Густина твердих тіл . За температури 20ºС
- •Густина рідин за температури 20ºС
- •Густина газів
- •Додаток 4 Теплофізичні коефіцієнти твердих тіл
- •Додаток 5 Пружні властивості твердих тіл
- •Додаток 6 Коефіцієнти лінійного теплового розширення твердих тіл в інтервалі 0–100 ºС
- •Додаток 7 Швидкість поширення звуку в різних середовищах
- •Додаток 8 Деякі фізичні характеристики рідин
- •Додаток 11 Коефіцієнт об’ємного теплового розширення деяких рідин
Порядок виконання роботи
1. Записати вихідні дані: сталу приладу = (2,40± 0,05) 10-6 м 2/с2, густину рідини 0 = (1,25±0,05) 103 кг/м3, густину кульки = (2,25 ±0,05) 103 кг/м3, температуру рідини t°С.
2. Відтягнути фіксатор 7 і обернути термостат 1 на 180°. Фіксатор 7 відпустити. Скляна кулька у внутрішньому циліндрі почне опускатися. Під час проходження кулькою середньої мітки на циліндрі увімкнути секундомір. Тричі виміряти секундоміром час t проходження кулькою відстані l між двома мітками на скляній трубці за початкової температури t1°С.
3. Увімкнути ЛАТР у мережу і подати напругу живлення (U = 80В) на нагрівник. У разі підвищення температури рідини у термостаті на 3–5°С живлення вимкнути і знову тричі виміряти час руху кульки на відстані l за цієї температури.
4. Виконати аналогічні досліди ще за трьох–п’яти різних температур.
5. Розрахувати середні значення t для кожної температури. Результати вимірювань та обчислень записати в таблицю:
Номер за пор. |
t°, °С |
t°, °С |
t, c |
t, С |
0, кг/м3 |
, кг/м3 |
, Па с |
, Па с |
ln |
1/Т °С-1 |
1 |
|
|
|
|
|
|
|
|
|
|
... |
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
C.з. |
|
|
|
|
|
|
|
|
|
|
6. За формулою (4) обчислити значення коефіцієнта в’язкості рідини для кожної температури.
7. Абсолютну похибку обчислити за формулою
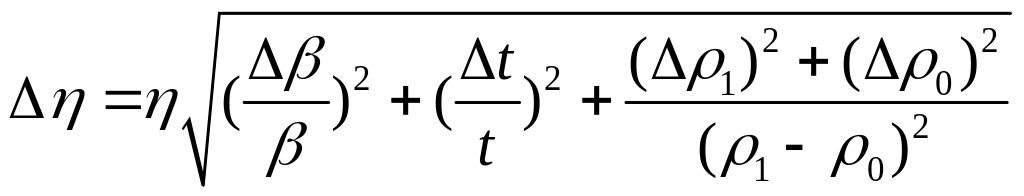 .
.
8. Побудувати графіки залежностей = f (t°С), ln = f (1/T).
9. Обчислити згідно з (7) енергію активації Е для трьох різних пар значень і Т. Виконати усереднення і розрахувати Е.
10. Записати кінцевий результат у вигляді
Е = (E ± E ), Дж/кмоль, ЕE=...%.
Контрольні запитання
Від чого залежить сила внутрішнього тертя в рідинах і газах?
У чому полягає фізичний зміст коефіцієнта в’язкості рідин?
Запишіть і поясніть формулу Стокса. За яких умов її можна застосовувати?
На яких принципах ґрунтується метод визначення коефіцієнта в’язкості рідини за допомогою віскозиметра Хепплера?
Які сили діють на кульку під час її руху в рідині?
Від чого залежить коефіцієнт в’язкості рідини?
Що таке енергія активації молекули рідини?
Лабораторна робота № 203. Визначення коефіцієнта в’язкості рідини за допомогою капілярного віскозиметра оствальда
Завдання: визначити коефіцієнт в’язкості рідини за допомогою капілярного віскозиметра Оствальда.
Приладдя: капілярні віскозиметри, ручна помпа, термометр, секун-домір, дистильована вода, досліджувана рідина.
Теоретичний матеріал, який необхідно засвоїти під час підготовки до виконання роботи: головні поняття гідродинаміки, закон Пуазейля, ламі нар-ний і турбулентний потік рідини, гідростатичний тиск (див. також перелік матеріалу до роботи № 201).
Література:
1) § 7.6–7.9, с. 114–124;
2) § 14.2.3, с. 36–38;
3) § 60, с. 186–190;
4) § 28, 31–33, с. 51–52, 55–59.
Опис установки. Експериментальна установка для вимірювання в’язкості рідин (рис. 4) складається з двох однакових віскозиметрів 1 і 2, розміщених у термостаті 3. Нижні резервуари віскозиметрів заповнені дистильованою водою і досліджуваною рідиною. Пампа 4 призначена для піднімання рівня рідини у віскозиметрі. Час протікання рідини через капіляр вимірюють секундоміром 5.
І
Рис. 4
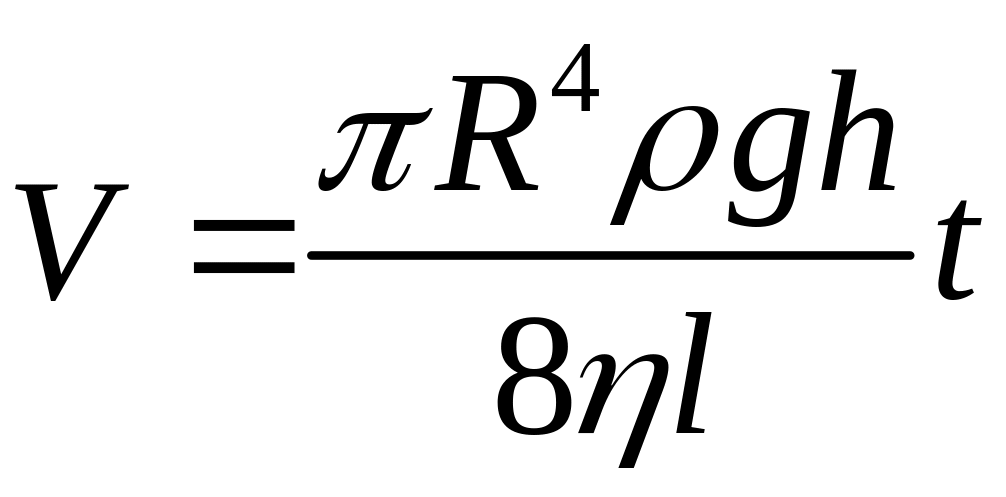 ,
(1)
,
(1)
де l – довжина капіляра; – густина рідини; h – висота капіляра; – коефіцієнт в’язкості рідини.
Якщо відомі конструктивні розміри віскозиметра і виміряно значення потрібних величин експеримент-тально, то з (1) можна визначити . У цій роботі використовують порівняльний метод визначення коефіцієнта в’язкості рідини, забезпечуючи в експерименті сталість величин V, R, h і l. Цього досягають використанням одного віскозиметра або двох ідентичних віскозиметрів з досліджуваною рідиною і рідиною з відомою в’язкістю. Тоді з (1) матимемо
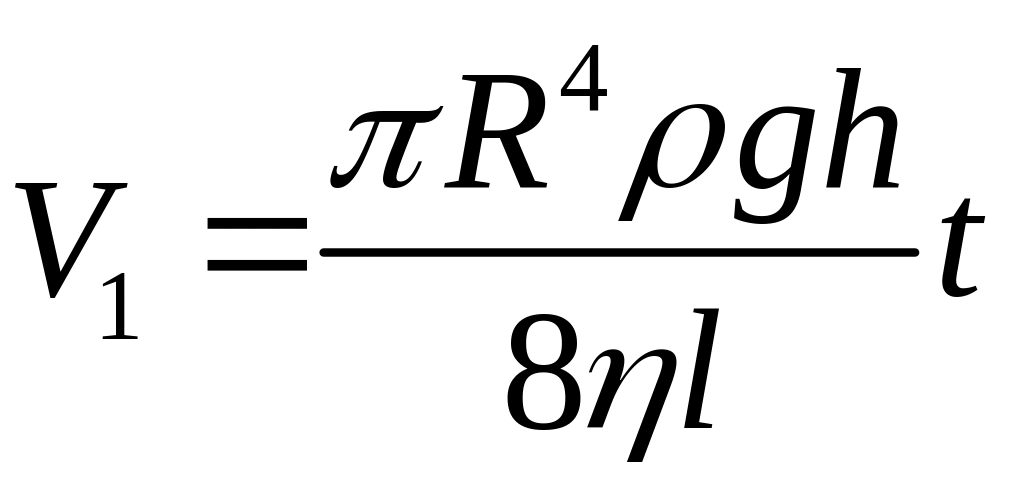 i
i
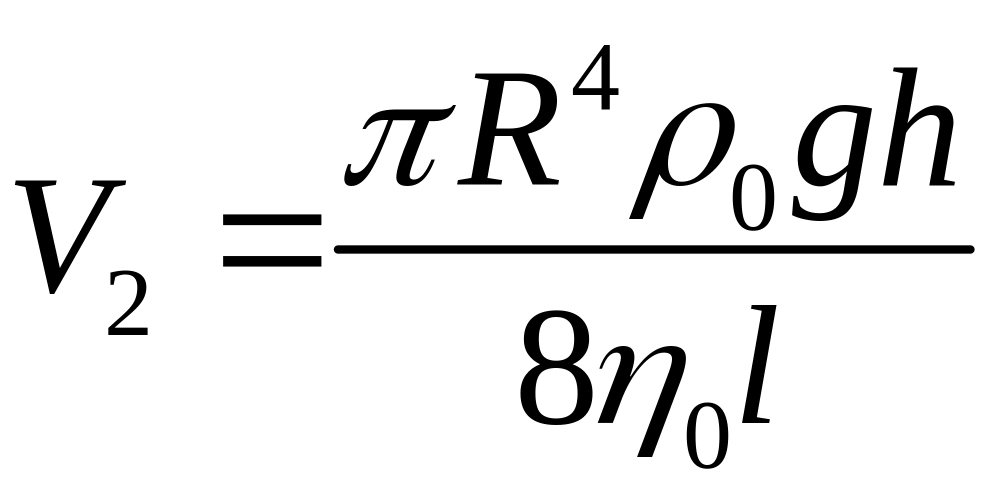 .
.
Однак V1=V2, тоді, прирівнявши праві частини рівнянь, легко отримати формулу для :
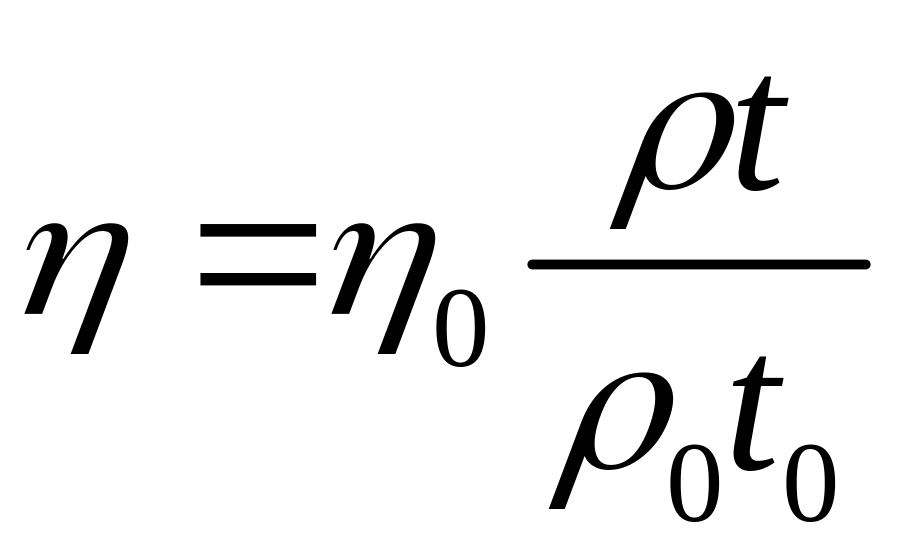 ,
(2)
,
(2)
де і – коефіцієнт в’язкості та густина досліджуваної рідини; 0 і 0 – коефіцієнт в’язкості та густина дистильованої води.
Вираз (2) є робочою формулою лабораторної роботи.
Формулу Пуазейля (1) можна вивести з таких міркувань. Нехай по трубі радіусом R і довжиною l (рис. 5) тече в’язка рідина зі швидкістю v. Протікання забезпечує різниця сил тиску на торцях циліндра F1 та F2. Водночас між шарами рідини виникає сила внутрішнього тертя
![]() ,
(3)
,
(3)
д
Рис. 5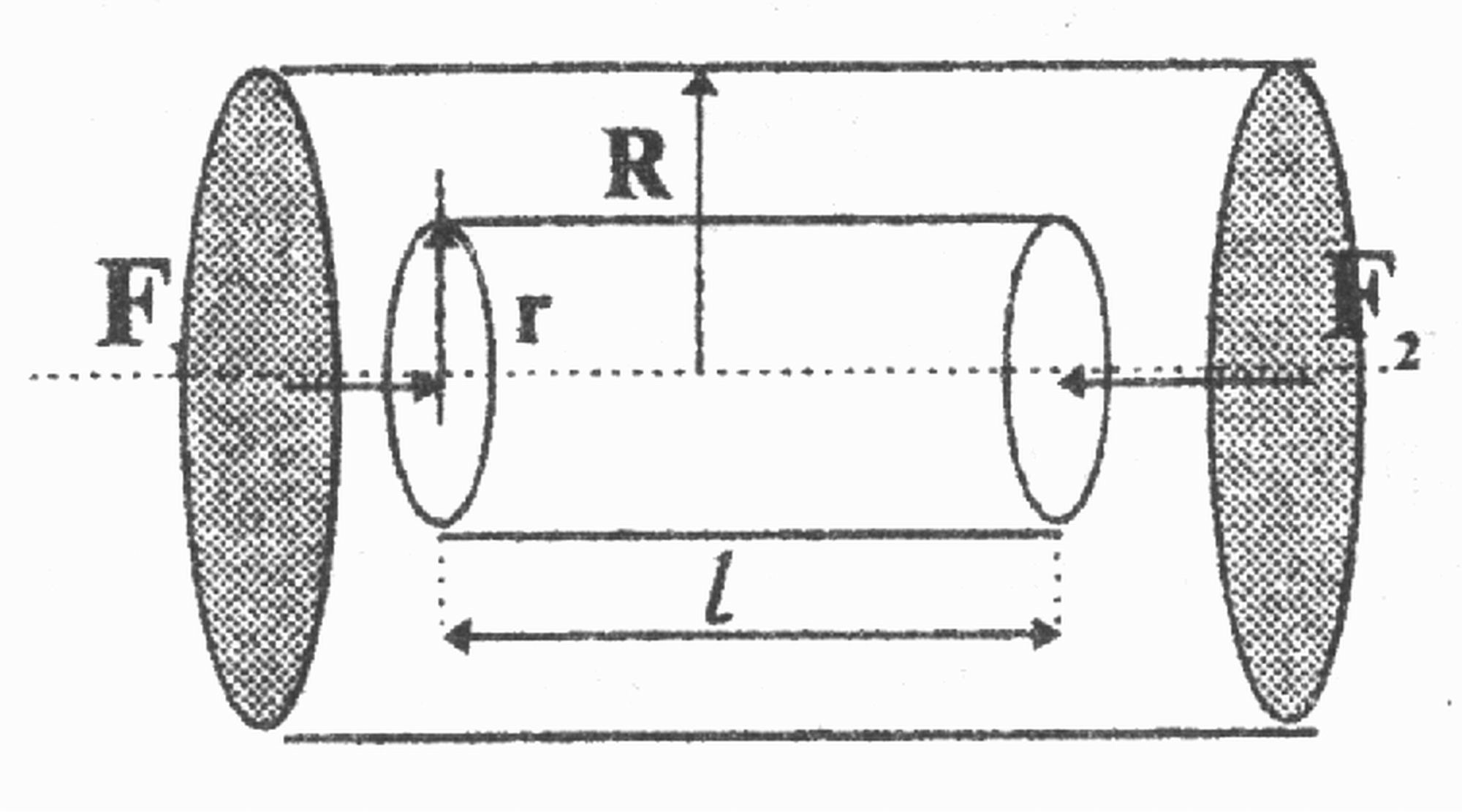
![]() .
(4)
.
(4)
Проінтегруємо цю рівність, отримаємо
 .
(5)
.
(5)
Сталу інтегрування С визначаємо з умови, що біля стінок труби v = 0. Тоді
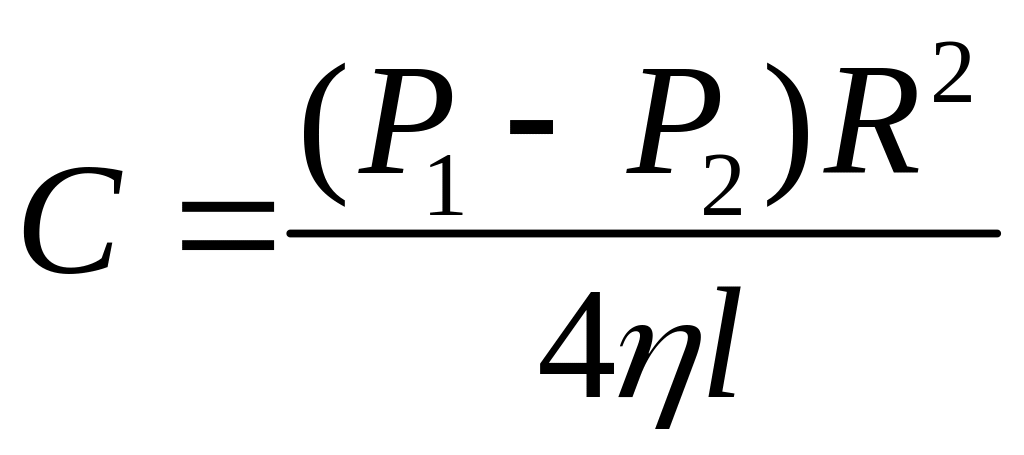 ,
а
,
а
 . (6)
. (6)
Формула (6) свідчить, що швидкість рідини розподілена в напрямі, перпендикулярному до осі труби, за квадратичним законом і є максимальною на осі труби.
Визначимо тепер об’єм рідини, яка протікає через трубу за одиницю часу. Для цього розіб’ємо поперечний переріз труби на кільця товщиною dr з радіусом r. Тоді dV=2vrdr. Після інтегрування
 ,
,
a
за час t
–
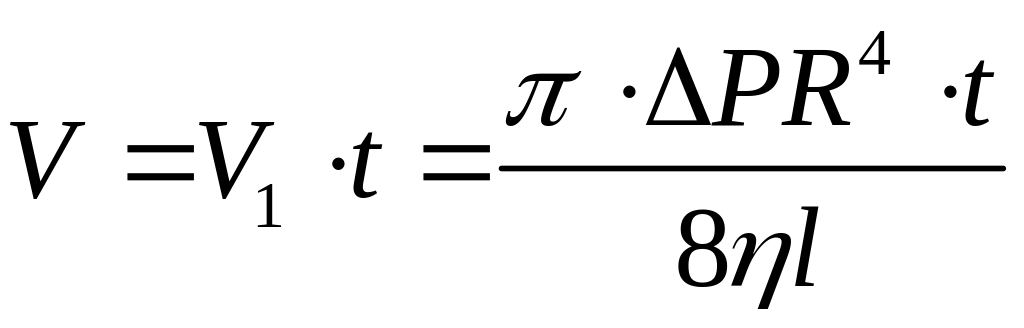 .
(7)
.
(7)
Це формула Пуазейля для ламінарної течії рідини в капілярній трубці.
