
- •Молекулярна фізика. Лабораторний практикум
- •Перелік лабораторних робіт
- •Список рекомендованої літератури
- •Частина і. Молекулярна фізика. Розділ 1. Будова речовини
- •1.1. Модель речовини. Маси атомів і молекул
- •1.2. Сили міжмолекулярної взаємодії. Агрегатні стани речовини
- •1.3. Енергія міжмолекулярної взаємодії. Потенціал Ленарда–Джонса
- •1.4. Структура речовини
- •1.4.1. Газоподібний стан
- •1.4.2. Рідини
- •1.4.3. Тверді тіла
- •Розділ 2. Основи молекулярно-кінетичної теорії газів
- •2.1. Ідеальний газ. Ізопроцеси. Рівняння стану ідеального газу
- •2.2. Тиск і температура ідеального газу. Основне рівняння молекулярно-кінетичної теорії
- •2.3. Поняття про статистичний розподіл. Функції розподілу
- •2.3.1. Закони розподілу молекул ідеального газу за швидкостями й енергіями теплового руху (розподіл Максвелла)
- •2.3.2. Барометрична формула. Розподіл Больцмана
- •2.3.3. Розподіл Максвелла–Больцмана
- •2.3.4. Квантові аспекти розподілів. Розподіли Бозе–Айнштайна і Фермі–Дірака
- •2.4. Середня кількість зіткнень молекул. Середня довжина вільного пробігу
- •Розділ 3. Основи термодинаміки
- •3.1. Головні поняття й означення
- •3.2. Внутрішня енергія ідеального газу Молекули ідеального газу не взаємодіють на відстані, тому
- •Вище доведено, що середня кінетична енергія теплового руху молекули ідеального газу
- •3.3. Теплоємність ідеального газу
- •Для ізобарного процесу
- •3.4. Теплоємність рідин
- •3.5. Теплоємність твердих тіл
- •3.5.1. Класична теорія теплоємності твердих тіл
- •3.5.2. Квантові теорії теплоємності твердих тіл.
- •3.6. Адіабатний процес
- •3.7. Політропні процеси
- •3.8. Робота в термодинамічних процесах
- •3.9. Стисливість газів
- •3.10. Ентропія
- •3.11. Циклічні процеси. Теплові машини
- •Розділ 4. Реальні гази
- •4.1. Рівняння стану реального газу. Рівняння Ван-дер-Ваальса
- •4.2. Внутрішня енергія і теплоємність реального газу
- •Розділ 5. Поверхневий натяг. Капілярні явища
- •На підставі (5.3) рівняння (5.4) запишемо у вигляді
- •Розділ 6. Фазові переходи
- •6.1. Агрегатні стани і фази речовини
- •6.2. Фазові переходи першого і другого роду
- •Розділ 7. Явища перенесення
- •7.1. Самодифузія і взаємна дифузія
- •7.2. Теплопровідність
- •7.4. Розріджені гази. Вакуум
- •Частина іі. Молекулярна фізика. Лабораторний практикум. Лабораторна робота № 201. Визначення коефіцієнта в’язкості рідини методом стокса
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 202. Дослідження залежності коефіцієнта в’язкості рідини від температури
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 203. Визначення коефіцієнта в’язкості рідини за допомогою капілярного віскозиметра оствальда
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №205. Визначення коефіцієнта поверхневого натягу рідини методом відривання кільця
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 206. Дослідження залежності коефіцієнта поверхневого натягу рідини від температури методом максимального тиску в бульбашці
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №208. Дослідження теплового розширення металів
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №209. Визначення питомої теплоємності металів методом охолодження
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 210. Визначення сталої больцмана та універсальної газової сталої
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №211. Визначення середньої довжини вільного пробігу та ефективного діаметра молекул повітря
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 212 визначення співвідношення теплоємностей повітря сp/сv методом клемана–дезорма
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 213. Визначення співвідношення теплоємностей повітря ср / сv методом стоячої хвилі
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 214. Вимірювання вологості повітря психрометром
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 215. Дослідження критичного стану речовини
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №216. Дослідження процесу плавлення кристалічних речовин
- •Порядок виконання роботи
- •Контрольні запитання
- •Додатки Головні фізичні сталі
- •Густина твердих тіл . За температури 20ºС
- •Густина рідин за температури 20ºС
- •Густина газів
- •Додаток 4 Теплофізичні коефіцієнти твердих тіл
- •Додаток 5 Пружні властивості твердих тіл
- •Додаток 6 Коефіцієнти лінійного теплового розширення твердих тіл в інтервалі 0–100 ºС
- •Додаток 7 Швидкість поширення звуку в різних середовищах
- •Додаток 8 Деякі фізичні характеристики рідин
- •Додаток 11 Коефіцієнт об’ємного теплового розширення деяких рідин
Частина і. Молекулярна фізика. Розділ 1. Будова речовини
1.1. Модель речовини. Маси атомів і молекул
Відомо, що всі матеріальні тіла складаються з атомів та молекул, які перебувають у стані безперервного руху і взаємодіють між собою. Атоми і молекули, як структурні елементи речовини, можна описати різними моделями залежно від обставин і характеру явищ, що відбуваються в речовині. В одних випадках їх уявляють матеріальними точками, в інших – абсолютно твердими тілами, а ще в інших беруть до уваги їхню внутрішню структуру. Будову атомів і молекул вивчає квантова механіка, тому закономірності структури і взаємодії молекул можна вважати відомими.
У молекулярній фізиці моделлю речовини є сукупність атомів і молекул, закономірності руху і взаємодії яких відомі.
Масу атомів і молекул у молекулярній фізиці описують не абсолютними значеннями, а відносною безрозмірною величиною, яку називають відносною атомною Аr, або відносною молекулярною масою Мr. За одиницю атомної маси приймають 1/12 маси ізотопу вуглецю 12С:
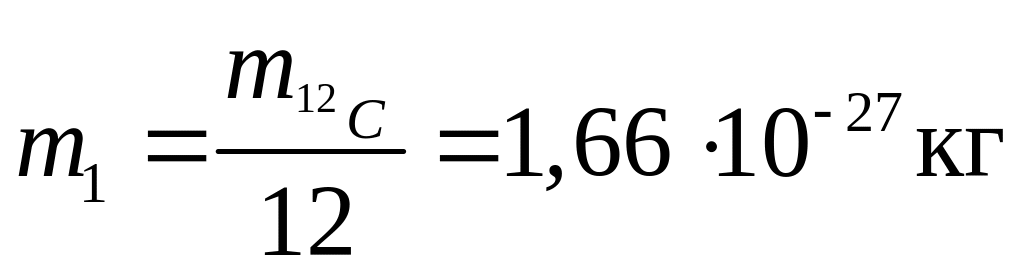 (1.1)
(1.1)
Відносну молекулярну (атомну) масу визначають за формулою
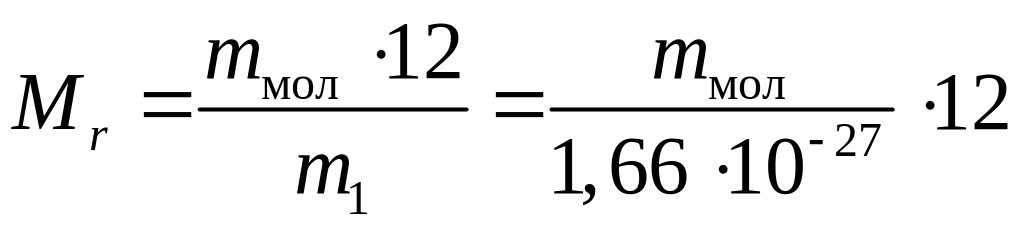 ,
(1.2)
,
(1.2)
де mмол – абсолютна маса молекули (атома), кг.
Кількість речовини в системі одиниць СІ виражають у молях. Один моль – це така кількість речовини, яка містить у собі стільки ж структурних елементів, скільки їх міститься в 0,012 кг ізотопу вуглецю 12С. Один моль будь-якої речовини завжди містить однакову кількість структурних елементів (закон Авогадро). Цю кількість виражає число Авогадро
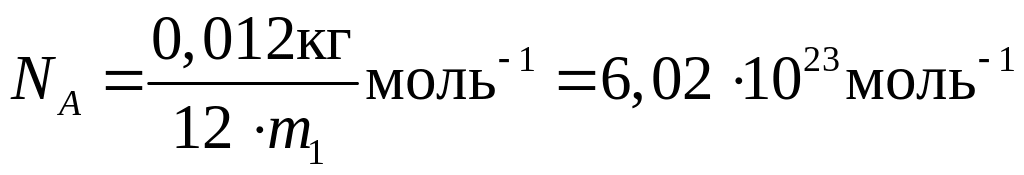 .
.
У молекулярній фізиці користуються також поняттям молярної маси, тобто маси одного моля речовини:
![]() , (1.3)
, (1.3)
де mмол – маса молекули, Mr – відносна молекулярна маса.
Кількість
молів речовини
![]() пов’язане з кількістю її молекул N
або ж з її масою m
таким співвідношенням:
пов’язане з кількістю її молекул N
або ж з її масою m
таким співвідношенням:
 ,
(1.4)
,
(1.4)
де М – молярна маса.
1.2. Сили міжмолекулярної взаємодії. Агрегатні стани речовини
А
Рис. 1.1. Потенціальна крива взаємодії
двох частинок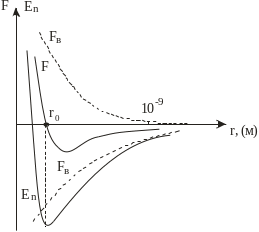
Загалом, молекули
речовини мають кінетичну енергію та
потенціальну енер-гію
взаємодії. Співвідношення між кіне-тичною
та потенціальною енергією моле-кул
визначають, у якому агрегатному стані
перебуває речовина. Якщо сумарна
кінетична енергія поступального руху
молекул є більшою від потенціальної
енергії їхньої взаємодії (![]()
![]() ),
то речовина перебуває в газоподібному
стані, якщо (
),
– то це твердий стан. Умовою рідкого
стану речовини є те, що ці енергії
приблизно дорівнюють одна одній. На
рис. 1.1 показано залежності сили взаємодії
та потенціальної енергії взаємодії
двох молекул від відстані між ними.
Відстані r0 відповідає мінімум
Еп(r), отже, на відстані r
=
= r0 молекули перебувають
у рівноважному стані. Оскільки сила
взаємодії
),
то речовина перебуває в газоподібному
стані, якщо (
),
– то це твердий стан. Умовою рідкого
стану речовини є те, що ці енергії
приблизно дорівнюють одна одній. На
рис. 1.1 показано залежності сили взаємодії
та потенціальної енергії взаємодії
двох молекул від відстані між ними.
Відстані r0 відповідає мінімум
Еп(r), отже, на відстані r
=
= r0 молекули перебувають
у рівноважному стані. Оскільки сила
взаємодії
![]() ,
то очевидно, що F(r0)=0. Якщо
r>r0, то між молекулами
переважають сили притягання, якщо r<r0
– то сили відштовхування.
,
то очевидно, що F(r0)=0. Якщо
r>r0, то між молекулами
переважають сили притягання, якщо r<r0
– то сили відштовхування.
У газоподібному стані відстані між молекулами речовини достатньо великі (r>>r0), тому взаємодія між ними доволі слабка. Це зумовлює відсутність форми і власного об’єму газів.
У рідині відстані між атомами і молекулами є близько r0, тому рідина має власний об’єм, однак власної форми не має. Для рідин характерний ближній порядок у розміщенні атомів. Тобто атом оточений певною кількістю впорядковано розміщених найближчих сусідів. Положення кожного атома чи молекули у рідині не є чітко визначеним, і вони можуть постійно переміщуватись в об’ємі рідини.
У твердому стані речовина має власний об’єм і сталу форму. Атоми і молекули можуть виконувати лише коливні рухи відносно своїх положень рівноваги, а переміщення атомів по об’єму ускладнене. Є два типи твердих тіл – аморфні й кристалічні. В аморфних тілах порядок розміщення атомів подібний до рідини, однак сили взаємодії між ними значно більші. У кристалічних тілах існує дальній порядок розміщення. Атоми перебувають у чітко фіксованих положеннях, які утворюють так звані елементарні комірки.
Розглянемо детальніше сили міжатомної та між молекулярної взаємо-дії. Відомо, що атом у цілому електронейтральний. Водночас сили, які утримують атоми в молекулі, є електромагнітними. Загалом існує два типи зв’язків атомів у молекулі – це іонний зв’язок і ковалентний зв’язок.
Іонний зв’язок виникає тоді, коли під час утворення молекули атоми речовини можуть легко втрачати (або приєднувати) один або ж декілька електронів, перетворюючись у додатні та від’ємні іони. Між такими іонами виникають кулонівські сили взаємного притягання, які й забезпечують утворення молекули. Прикладами молекул з іонним зв’язком є NaCl, NaJ, KBr та ін. За умови іонного зв’язку між іонами відбувається повний обмін зарядом, кратний до заряду електрона.
К
Рис. 1.2. Утворення ковалентного зв’язку
в молекулі
Іонний та ковалентний зв’язки не тільки відповідальні за утримування атомів у молекулі, а й відіграють важливу роль у створенні сил міжмолекулярної взаємодії у речовині. Іонний та ковалентний зв’язки виявляються лише тоді, коли відстані між молекулами стають достатньо малими. Саме тому вони характерні, головно для кристалічних твердих тіл, формуючи їхню кристалічну структуру. З огляду на це кристали поділяють на іонні та ковалентні. Сили іонного та ковалентного зв’язків достатньо великі, що зумовлює міцність та низку інших властивостей кристалічних тіл.
Різновидом ковалентного зв’язку в кристалах є металевий зв’язок, за якого валентні електрони всіх атомів кристала стають вільними і колективізованими, утворюючи електронний газ, який заповнює кристалічну ґратку. У вузлах кристалічної ґратки містяться позитивно заряджені іони, які, взаємодіючи з колективізованими електронами, утворюють стійку структуру кристала. Металевий зв’язок характерний, здебільшого, для кристалів, що містять атоми одного сорту (мідь, золото, срібло тощо). Енергія металевого зв’язку значно менша від енергії ковалентного та іонного зв’язків. Свідченням цього є, зокрема, нижча температура плавлення металів порівняно з іонними та ковалентними кристалами.
В
Рис. 1.3. Ван-дер-ваальсівська
міжмолекулярна взаємодія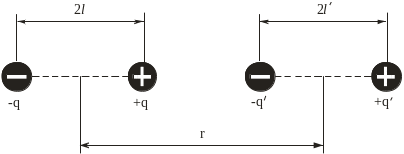
Неважко довести, що сила електростатичної взаємодії двох диполів є силою притягання. Отже, сили Ван-дер-Ваальса також мають електро-магнітну природу і зумовлені взаємодією поляризованих молекул.
Зазначимо, що молекули низки речовин мають власний дипольний момент. Такі молекули називають полярними, а ван-дер-ваальсівські сили взаємодії між ними – дипольно орієнтаційними.
Якщо ж внутрішня будова молекул така, що вони не мають власного дипольного моменту, то їх називають неполярними. Водночас у разі зближення неполярних молекул їхні електричні поля не повністю взаємно компенсуються і вони поляризують одна одну. Подальша їхня взаємодія відбувається так, як і для полярних молекул. Сили ван-дер-ваальсівської взаємодії неполярних молекул називають дисперсійними.
Отже, сили міжмолекулярної взаємодії в речовині поділяють на сили іонного зв’язку, сили ковалентного зв’язку та сили Ван-дер-Ваальса. Ван-дер-ваальсівські сили, на відміну від двох інших, виникають за повної відсутності обміну зарядами між молекулами. Зазначимо, що всередині молекули ван-дер-ваальсівські сили не виявляються.
