
- •Предисловие
- •Модуль курса общей химии «Учение о растворах. Протолитические и гетерогенные равновесия»
- •Темы занятий модуля Для студентов лечебного и педиатрического факультетов
- •Для студентов стоматологического факультета
- •Для студентов медико-профилактического факультета
- •Для студентов фармацевтического факультета
- •Литература
- •Введение
- •Тема: Вода как универсальный биорастворитель. Коллигативные свойства растворов электролитов и неэлектролитов
- • Учебно-целевые вопросы
- •Краткая теоретическая часть
- •Свойства и функции воды
- •1) Растворение веществ с ионным типом связи
- •Гидратация ионов
- •Коллигативные свойства растворов
- •К коллигативным свойствам относятся:
- •Диффузия;
- •Диффузия
- •Осмос. Осмотическое давление
- •Изотонический раствор
- •Гипертонический раствор
- •Гипотонический раствор
- •При снижении осмотического давления крови до 400-350 кПа н аступает гибель организма.
- •Давление насыщенного пара растворителя над раствором
- •Повышение температуры кипения и понижение температуры кристаллизации раствора по сравнению с растворителем
- •Для растворов электролитов в математическое выражение II закона Рауля вводится изотонический коэффициент I:
- •Типовые упражнения и задачи с решениями
- •Переход от массовой доли к молярной концентрации осуществляется по формуле:
- •Обучающие тесты
- •Задачи и упражнения для самостоятельного решения
- •Учебно-исследовательская лабораторная работа Тема: Осмос Опыт №1: Наблюдение явлений плазмолиза и гемолиза
- •Тема: Протолитические процессы и равновесия. Водородный показатель. Колориметрическое определение рН
- •Учебно-целевые вопросы
- •Краткая теоретическая часть
- •Э лектролиты
- •Вывод закона разведения Оствальда:
- •Петер-Йозеф-Вильгельм Дебай (24.03.1884-2.11.1966).
- •Биологическая роль электролитов в организме
- •Средние ежедневные поступления и потери жидкости у взрослых
- •Причины нарушения водного обмена
- •Баланс электролитов в организме
- •Водно-электролитный баланс биологических жидкостей в организме человека
- •Ионное произведение воды. Водородный и гидроксильный показатели
- •Характеристика среды раствора
- •Диапазон изменения рН биологических жидкостей
- •Интервал рН перехода окраски индикаторов
- •Типовые упражнения и задачи с решениями
- •Ответ: степень ионизации гликолевой кислоты 5,44×10–2.
- •Ответ: общая кислотность уксусной кислоты 1,75×10–5 моль/л.
- •Обучающие тесты
- •У чебно-исследовательская лабораторная работа Тема: Определение рН растворов
- •Опыт № 1. Определение рН биологической жидкости с помощью универсального индикатора
- •Опыт № 2. Одноцветные и двуцветные индикаторы
- •Опыт № 3. Смещение равновесия диссоциации уксусной кислоты и гидроксида аммония
- •Тема: Протолитические процессы и равновесия. Теории кислот и оснований. Гидролиз
- • Учебно-целевые вопросы
- •Краткая теоретическая часть
- •Типы протолитических реакций
- •Электронная теория Льюиса
- •Жесткие, мягкие кислоты и основания (жмко)
- •Типовые упражнения и задачи с решениями
- •Задачи и упражнения для самостоятельного решения
- •У чебно-исследовательская лабораторная работа Тема: Гидролиз солей
- •Тема: Протолитические процессы и равновесия. Буферные растворы
- •Учебно-целевые вопросы
- •Краткая теоретическая часть
- •Типовые упражнения и задачи с решениями
- •Учебно-исследовательская лабораторная работа Тема: Буферные системы. Буферные системы организма
- •Опыт 2.1. Определение способности буферных растворов сохранять рН при добавлении щелочей
- •Опыт 2.2. Определение способности буферных растворов сохранять рН при добавлении кислот
- •Опыт 2.3. Определение способности буферных растворов сохранять рН при разбавлении
- •Тема: Протолитические процессы и равновесия. Буферные системы организма
- •Учебно-целевые вопросы
- •Краткая теоретическая часть
- •Гидрокарбонатная буферная система
- •Гидрофосфатная буферная система
- •Белковая буферная система
- •Гемоглобиновая буферная система
- •Бикарбонатной буферных систем
- •Диапазон изменения значений рН при различных типах нарушения кислотно-основного баланса в организме
- •Причины и классификация ацидоза и алкалоза
- •Основные показатели крови при нарушении кислотно-основного баланса
- •Типовые упражнения и задачи с решениями
- •Обучающие тесты
- •Учебно-исследовательская лабораторная работа Тема: Определение буферной емкости сыворотки крови
- •Тема: Гетерогенные процессы и равновесия
- •Учебно-целевые вопросы
- •Краткая теоретическая часть
- •Взаимосвязь Ks и растворимости s:
- •Конкурирующие гетерогенные процессы: конкуренция за катион или анион
- •Формирование костной ткани
- •Патологические гетерогенные процессы в организме
- •Т иповые упражнения и задачи с решениями
- •Обучающие тесты
- •Задачи и упражнения для самостоятельного решения
- •У чебно-исследовательская лабораторная работа Тема: Гетерогенные равновесия
- •Опыт № 1. Условия образования осадка
- •Опыт № 2. Влияние одноименного иона на образование осадка
- •Опыт № 3. Влияние константы растворимости электролитов на их способность к переосаждению
- •Опыт № 4. Условия растворения осадка
- •Теоретические вопросы к контрольной работе по модулю для студентов лечебного и педиатрического факультетов
- •Для студентов стоматологического и медико-профилактического факультетов
- •Экзаменационные теоретические вопросы для студентов лечебного и педиатрического факультетов
- •Для студентов стоматологического факультета
- •Для студентов медико-профилактического факультета
- •Приложение
- •1. Константы некоторых жидкостей, применяемых в качестве растворителей
- •2. Коэффициенты активности f ионов в водных растворах
- •3. Средние значения водородного показателя (рН) биологических жидкостей
- •4. Ионное произведение воды kw при различных температурах
- •5. Силовые показатели и константы ионизации кислот по реакции
- •6. Константы растворимости некоторых малорастворимых солей и гидроксидов (25оС)
- •7. Константы нестойкости комплексных ионов в водных растворах (25оС)
- •8. Измененения содержания воды в организме в зависимости от возраста
- •9. Распределение воды в организме в зависимости от пола
- •10. Основные элементы жидкостных компартментов организма
- •11. Вещества определяющие осмоляльность плазмы
- •12. Наиболее часто используемые кристаллоидные растворы
- •Оглавление
Для студентов медико-профилактического факультета
Особенности строения воды, ее уникальные физико-химические свойства, роль в жизнедеятельности. Вода как универсальный растворитель.
Диссоциация воды. Ионное произведение воды. Kw при 37оС равна 10–13,62. Чему равен рН дистиллированной воды при этой температуре?
Водородный показатель (рН) как характеристика кислотности биологических сред и водных растворов. рН основных биологических жидкостей (плазмы, желудочного, кишечного соков, слюны). Шкала кислотности. Каков диапазон изменений концентраций Н+ в крови совместим с жизнью, если допустимые значения рН=7-7,8?
Сильные и слабые электролиты. Степень и константа диссоциации. Закон разведения Оствальда. Примеры электролитов в организме.
Основные положения протолитической теории кислот и оснований. Типы протолитических реакций. Чем являются следующие молекулы и ионы в водных растворах: СН3СООН, СН3СОО-, НСО3-, H3-СН2-СОО-. Ответ подтвердите соответствующими уравнениями реакций.
Гидролиз как протолитическая реакция. Константа гидролиза (Kг). Степень гидролиза (h). Факторы, влияющие на Kг и h. Роль гидролиза в санитарно-гигиенической практике.
Теория кислот и оснований Льюиса. Суть теории Пирсона (ЖМКО). Пользуясь теорией ЖМКО объясните, почему ионы Na+ и K+ находятся в организме в виде аква- и гидроксокомплексов; СО более прочно связывается с гемоглобином, чем кислород; ионы тяжелых металлов являются тиоловыми ядами?
Коллигативные свойства растворов электролитов и неэлектролитов. Диффузия, осмос.
Клетка как осмотическая ячейка. Роль осмоса в жизнедеятельности человека (эндоосмос, экзоосмос, осмотическое давление, осмолярная концентрация, «осмотический конфликт», «осмотический шок»). Применение гипо-, гипер- и изотонических растворов.
Буферные растворы, механизм буферного действия, рН буферных растворов.
Буферные системы организма. Бикарбонатный буфер, механизм действия, биологическая роль.
Буферные системы организма. Фосфатная буферная система, механизм действия, биологическая роль.
Белковые буферные системы крови, тканей, механизм действия, биологическая роль.
Гемоглобиновые буферные системы крови, особенности механизма действия, связь с процессом оксигенации, биологическая роль.
Буферная емкость, факторы, влияющие на ее величину. Буферная емкость крови.
Гетерогенные равновесия (изолированные). Условия существования гетерогенных равновесий. Константа гетерогенного равновесия. Взаимосвязь между растворимостью и константой растворимости.
Изолированные и конкурирующие гетерогенные процессы. Примеры конкуренции за общий анион и общий катион. Биологическое значение.
Гетерогенные процессы и равновесия в организме. Формирование костной и зубной ткани. Изоморфизм. Реакции, лежащие в основе образования конкрементов: оксалатов, карбонатов, фосфатов.
Рассчитайте ионную силу и активность ионов магния в 0,01М растворе K2SO4.
Установите, каким будет раствор по отношению к плазме крови (изо-, гипо- или гипертоническим) при 37оС хлорида калия с(КСl)=0,01 моль/л, i=1,96.
Рассчитайте осмотическое давление при 310 К 20%-го раствора глюкозы (пл. 1,08 г/см3), используемого для внутривенных вливаний и сравните с осмотическим давлением крови.
Осмотическое давление крови равно в норме 740-780 кПа. Вычислите осмолярность крови.
Вычислите изотонический коэффициент 0,2М раствора нитрата калия, имеющего при t = 37оС осмотическое давление равное 917 кПа.
При исследовании активности трансфераз динитрофенилгидразиновым методом применяют фосфатный буфер. Для его приготовления смешивают 840 мл гидрофосфата натрия (с = 0,1 М) и 160 мл раствора дигидрофосфата натрия (с = 0,1 М). Вычислите рН такого буферного раствора (рK(Н2РО
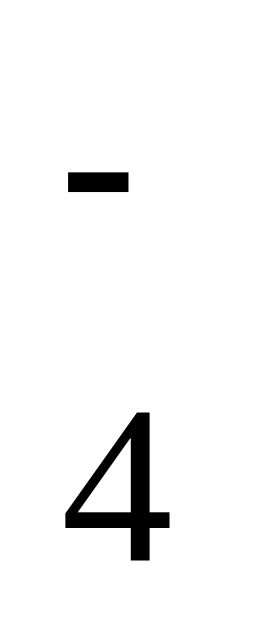 )
= 7,2)
)
= 7,2)К 1 л крови для изменения рН от 7,36 до 7,00 необходимо добавить 3,610-3 моль соляной кислоты. Какова буферная емкость крови по кислоте? Что такое буферная емкость, от каких факторов зависит ее величина?
Смешали равные объемы 0,001М растворов хлорида кальция и карбоната натрия. Образуется ли осадок? Почему? Ks(СаСО3) = 3,810–9. Что называется константой растворимости?
В какой последовательности должны выпадать осадки, если к раствору, содержащему ионы Са2+, Ва2+ и Sr2+ постепенно приливать раствор Na2SO4? (Ks(СаSО4)=2,510–5; Ks(ВаSО4)=1,110–10; Ks(SrSО4) = 3,210–7). Ответ поясните. Как называется данный процесс?
Рассчитайте рН ацетатного буферного раствора, содержащего в 1 л 0,2 моль уксусной кислоты и 0,05 моль ацетата натрия.
Определите рН, константу и степень гидролиза хлорида аммония, если с(NH4Cl) = 0,1 моль/л, Kв(NH4OH) = 1,7410–5.
УИРС: Тематика рефератов:
Биологическая роль растворов, применение растворов в медицине.
Роль электролитов в жизнедеятельности организма.
Изотонические, гипертонические, гипотонические растворы, их применение в медицине.
Исследование рН биологических жидкостей в целях диагностики, лечения и профилактики различных заболеваний.
Биохимическая роль гидролиза.
Буферные системы крови. Кислотно-основное равновесие организма.
Кислотно-щелочное равновесие крови, основные причины его нарушения.
Гетерогенные равновесия и их роль для живого организма.
