- •Специальные разделы оптического материаловедения
- •Термодинамика фазовых равновесий
- •1.1 Общие сведения о термодинамике
- •1 Предмет термодинамики1
- •1.1.2 Термодинамическая система, виды систем
- •Изолированные системы – те, которые не имеют возможности обмениваться веществом и энергией с окружением и имеющие постоянный объем.
- •1.1.3 Параметры состояния, параметры процессов
- •1.1.4 Функции состояния
- •1.1.5 Виды процессов
- •1.1.6 Внутренняя энергия, теплота и работа
- •1.1.7 Максимальная работа при изобарических, изотермических, адиабатических и изохорных процессах
- •1.2 Законы термодинамики
- •1.2.2 II закон термодинамики и энтропия как термодинамическая функция
- •1.2.3 Энтропия и термодинамическая вероятность. III закон термодинамики
- •Следствия Законов
- •1.2.5 Термодинамические функции, важные для материаловедения.
- •1.2.6 Применение термодинамических понятий в других областях науки
- •1.3 Производные термодинамических потенциалов и фазовые переходы
- •1.3.1 Первые производные термодинамических потенциалов, их физический
- •1.3.2 Вторые производные термодинамических потенциалов (соотношения
- •1.3.3 Фазовые переходы I и II рода.
- •1.3.4 Фазовые переходы I рода. Барическая зависимость фазовых переходов I рода:
- •1.4 Теория фазовых равновесий
- •1.4.1 Понятия «фазовые равновесия», «компонент», «диаграмма состояний»,
- •1.4.2 Понятие химического потенциала. Условия равновесия фаз. Правило фаз
- •1.4.3 Диаграмма состояний однокомпонентной системы
- •1.4.5 Эвтектики (двухкомпонентные системы). Линии ликвидуса и солидуса.
- •1.4.6 Твердые растворы (двухкомпонентные системы). Значение твердых
- •1.4.7 Ограниченные твердые растворы
- •1.4.8 Упорядочение твердых растворов
- •1.4.9 Полная несмешиваемость в жидком и в твердом состояниях
- •1.4.10 Системы с расслаиванием в жидком состоянии. Стабильное и
- •1.4.11 Системы с образованием химических соединений (двухкомпонентные
- •1.4.12 Системы с образованием химических соединений (двухкомпонентные
- •1.4.13 Трёхкомпонентные системы (принципы изображения,
- •1.4.14 Комбинация элементов диаграмм состояний. Физико-химический анализ.
- •2. Фазовые переходы и кинетическая теория стеклования
- •2.1 Стеклование
- •2.1.1 Принципиальная особенность фазовых переходов I и II рода в общей
- •2.1.2 Природа взаимодействия в конденсированных системах (общие
- •Ионное взаимодействие
- •Взаимодействие в металлах
- •Ковалентное взаимодействие
- •Водородные связи
- •Взаимодействие Ван-дер-Ваальса
- •Энергия химических связей
- •2.1.3 Основные особенности строения жидкостей и принцип их обобщенного
- •2.1.4 Общие сведения о релаксационных процессах как о процессах перехода от
- •2.1.5 Равновесные и мгновенные свойства жидкостей
- •2.1.6 Переохлажденные жидкости как частный случай метастабильного
- •2.1.7 Проявление стеклования на свойствах жидкостей
- •2.1.8 Определение стеклообразного состояния как лабильного (абсолютно
- •2.1.9 Математическое описание стеклования в кинетической теории. Твердо- и
- •2.1.10 Время релаксации структуры и его зависимость от температуры.
- •2.1.11 Соотношение температур стеклования и плавления (правило «2/3»
- •2.2 Кристаллизация расплавов стекол
- •2.2.1 Термодинамические особенности метастабильной жидкости
- •2.2.2 Работа образования зародыша кристаллизации20
- •2.2.3 Кривые Таммана а) скорость зарождения и кривая зарождения.
- •Б) скорость роста и кривая роста.
- •2.2.4 Методы изучения кристаллизационной способности и её
- •А) политермический метод и диаграммы кристаллизационной способности
- •Б) фазовый состав и морфология кристаллов.
- •В) дифференциальный термический анализ.
- •Г) скорость кристаллизации
- •2.2.5 Типы кристаллизации
- •2.2.6 Катализированная кристаллизация; ситаллы
- •2.2.7 Связь кристаллизационной способности с диаграммой состояния
- •3.Термодинамика стеклообразного состояния
- •3.1.1 Термодинамические переменные, используемые при математическом
- •3.1.2 Математическое описание избыточной свободной энергии лабильной
- •3.1.3 Математическое условие стеклования, налагаемое на изменения
- •3.1.4 Соотношение Пригожина-Дефея и его экспериментальная проверка
- •3.1.5 Термодинамический инвариант стеклообразного состояния
- •3.1.6 Следствия, вытекающие из соотношений термодинамики
- •5. Релаксационные процессы в стеклообразном состоянии. Ионная проводимость и ионный обмен
- •5.1.1 Зависимость температуры стеклования от скорости охлаждения
- •5.1.2 Процессы и законы релаксационных изменений свойств, структурная
- •5.1.3 Оценка времени достижения равновесного состояния в процессе отжига
- •5.1.4 Физическое старение стекла при комнатной температуре52
- •5.1.5 Релаксационные явления при переходе через температуру стеклования
- •5.1.6 «Кроссовер эффект»
- •5.1.7 Расчёт изменения свойств при отжиге стекол на основании
- •5.2 Природа ионной проводимости и диффузии в стеклах.
- •5.2.1 Структура стекла и основы механизма
- •5.2.2 Законы диффузии и соотношение Нернста – Эйнштейна
- •5.2.3 Основное статистическое уравнение проводимости. Энергия активации.
- •5.2.4 Общие корреляции, ряд подвижностей
- •5.2.5 Основные закономерности электропроводности, определяемые составом
- •5.2.6 Ионообменные процессы и проблемы современной оптической технологии
- •5.2.7 Ионообменные процессы с растворами. Стеклянный электрод.
- •6. Взаимосвязь между основными видами релаксационных процессов в стеклах
- •6.4.1 Соотношение Максвелла для проводимости диэлектриков
- •6.4.2 Соотношение Максвелла для проводимости диэлектриков как основа связи
- •6.4.3 Экспериментальная проверка возможности расчёта температуры «ионного» максимума внутреннего трения по данным проводимости
- •7. Основные принципы химической устойчивости стекол
- •7.1.1 Практическая значимость свойства и его физико-химическое
- •7.1.2 Методы испытания и классификация стекол по группам
- •Группы химической устойчивости бесцветного оптического стекла к действию кислоты и дистиллированной воды
- •Группы химической устойчивости бесцветного оптического стекла к действию влажной атмосферы
- •7.1.3 Влияние компонентов состава стекла на химическую устойчивость
- •7.1.4 Способы защиты оптических деталей от химического разрушения
- •8. Специфика некоторых структурных явлений в регистрирующих средах
- •8.1. Фотоструктурные изменения в халькогенидных стеклах, их существо и
- •8.2 Структурно-фазовые изменения в жидких кристаллах и физико-химическая
- •8.2.1 Общие представления о жидких кристаллах
- •8.2.2 Специфика изменения электрических и магнитных свойств при
8.2 Структурно-фазовые изменения в жидких кристаллах и физико-химическая
сторона этих процессов
8.2.1 Общие представления о жидких кристаллах
Жидкие кристаллы были открыты ботаником Рейнитцером (Австрия) в 1888 г. Было обнаружено, что некоторые вещества органической природы проявляют множественность изменений структуры при плавлении. При этом проявляются одновременно и свойства, типичные для жидкости, и свойства, типичные для кристаллов в довольно широком диапазоне температур. Такое состояние вещества было названо мезоморфным, то есть промежуточным между состояниями, а сам класс был назван жидкими кристаллами. Интерпретация этого явления вызвала много споров и не была сразу признана всеми. Долгое время даже такие авторитетные ученые как Тамманн отрицали их самостоятельное
|
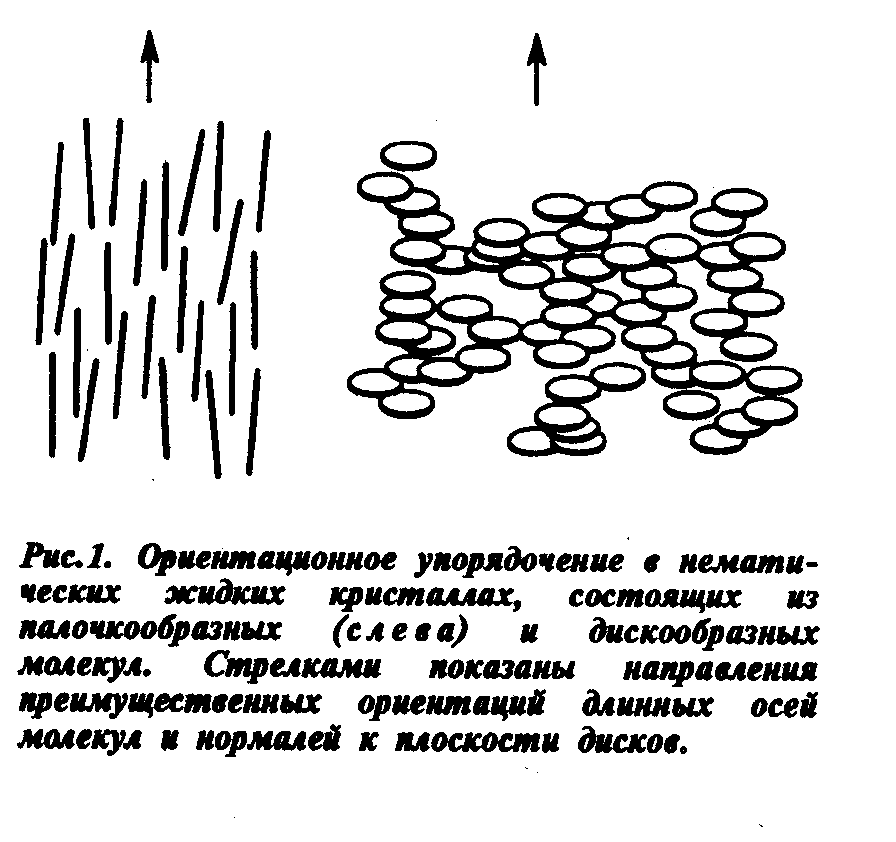
Рис. 91. Ориентационное упорядочение в нематических жидких кристаллах, состоящих из палочкообразных (слева) и дискообразных молекул. Стрелками показаны направления преимущественных ориентаций длинных осей осей молекул и нормалей к плоскости дисков. Б.И.Островский, Разнообразие жидких кристаллов. Природа, 1997, № 7, с. 60. |
существование, особенности свойств приписывались примесями и отсутствию чистоты эксперимента.
Обычное вещество в жидком состоянии обладает текучестью и принимает форму сосуда, в котором находится. В жидкости существует только ближний порядок в ориентации молекул. В твердотельном кристалле молекулы строго ориентированы и существует дальний порядок.
В жидкости, образованной плавлением жидких кристаллов (ЖК), существует оптическая анизотропия, свидетельствующая об ориентации молекул.
За истекшие более 100 лет после их открытия исследования жидких кристаллов развились чрезвычайно широко во всех странах. Ими занимались и физики, и химики и биологи. Сейчас это направление трудно даже охарактеризовать в одной лекции, настолько своеобразна специфика их свойств, настолько сложна их интерпретация и чрезвычайно широки области их применения.
а) классификация по признакам молекулярной ориентации
ЖК образуют вещества с сильно развитой анизотропией строения молекул. Молекулы могут быть вытянутыми (палочкообразными), могут быть плоскими (дискообразными). Если молекулы вытянутые, то в кристаллическом состоянии вещества все они ориентированы одинаково и существует строгая периодичность расположений во всех направлениях.
При плавлении может происходить частичное или полное исчезновение периодичности в одном из направлений, в других направлениях ориентация может сохраняться. Эти ЖК называются нематическими – рис. 91. В нематиках сохраняется только преимущественная ориентация.
|
Рис.92. Смектические и дискотические жидкие кристаллы. В смектиках (А) (а) и С (б) молекулы располагаются слоями, сохраняя преимущественную ориентацию; d – прериод смектических слоёв, z – направление трансляции В смектиках С длинные оси молекул наклонены относительно нормали к плоскости слоёв. Дискотики образуют вместо слоёв колонки, содержащие стопки дискообразных молекул (в). В направлении вдоль осей колонок система обладает свойствами жидкости, в то время как в плоскости дисков наблюдается дальний трансляционный порядок, отвечающий плоской гексагональной или ромбической сетке. Источник тот же. |
В смектических ЖК сохраняется полностью один из элементов симметрии (например, период слоёв или гексагональная форма упаковки в колонке) рис. 92.
смектиках длинные оси могут быть наклонены относительно нормали к плоскости слоёв. В дискотиках образуются вместо слоёв колонки, содержащие стопки дискообразных молекул. В направлении вдоль осей колонок система обладает свойствами жидкости, в плоскости дисков наблюдается дальний трансляционный порядок.
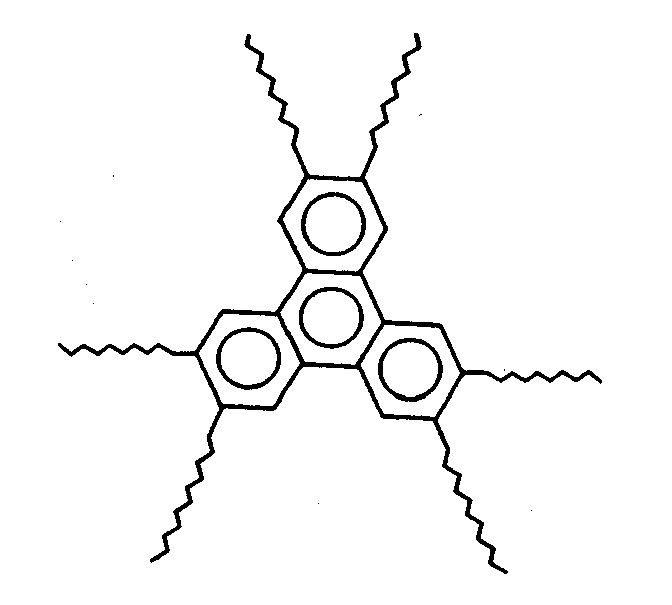
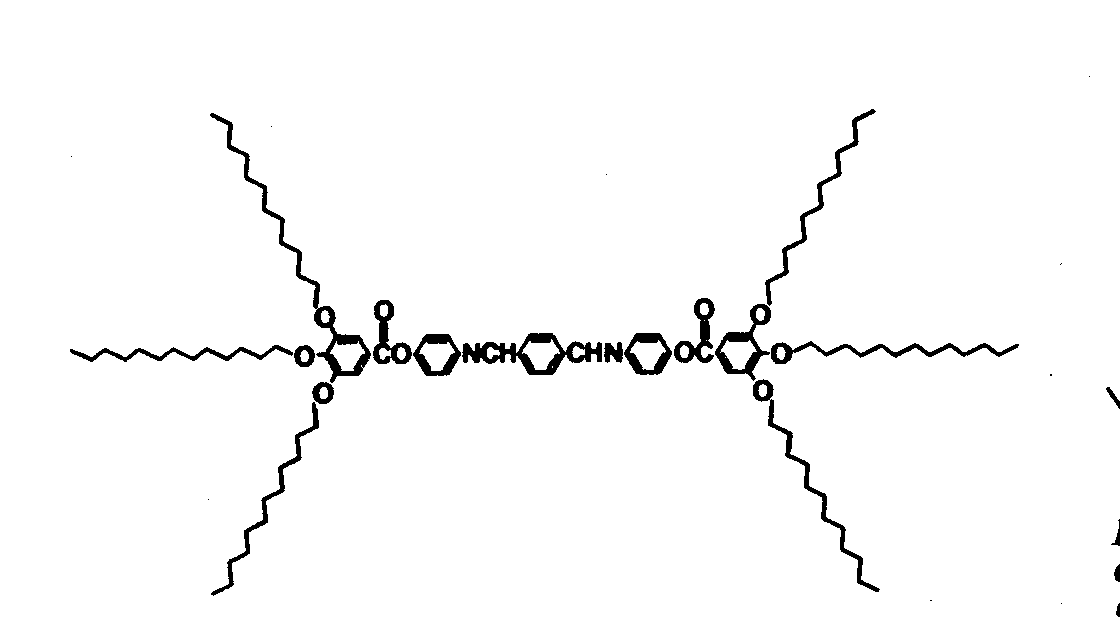
Примеры дискообразных молекул показаны на рис. 93, палочкообразных – на рис. 94.
|
Рис. 93. Пример дискообразных молекул. Источник- тот же. |
|
Рис. 94. Пример палочкообразных молекул. Источник тот же. |
Холестерические жидкие кристалла нами не рассматриваются, так как они являются производными от молекулы холестерина и эта область весьма специфична. Именно к этому классу относились ЖК, открытые Рейнитцером.
б) получение ЖК
ЖК могут быть получены плавлением кристаллов (термотропные ЖК) или растворением веществ в растворителях (лиотропные). Растворы обладают свойствами ЖК.
в) общие характеристики фазовых переходов
Термические свойства ЖК характерны прежде всего наличием первой температуры плавления Т0, и последующих температур Т1, Т2… при которых свойства расплавившегося ЖК изменяются вследствие последовательной потери элементов симметрии. Наконец, вся жидкость просветляется при Тпр . Схема таких переходов показана на рис. 94. Переходы могут быть только при нагревании (монотропные переходы) и также при охлаждении (энантиотропные). При нагревании и при охлаждении температуры переходов могут различаться. Это связано с возникновением переохлаждения или перегрева состояний.
В области температур от Т0 до Тпр свойства ЖК (для нас интересны оптические свойства)
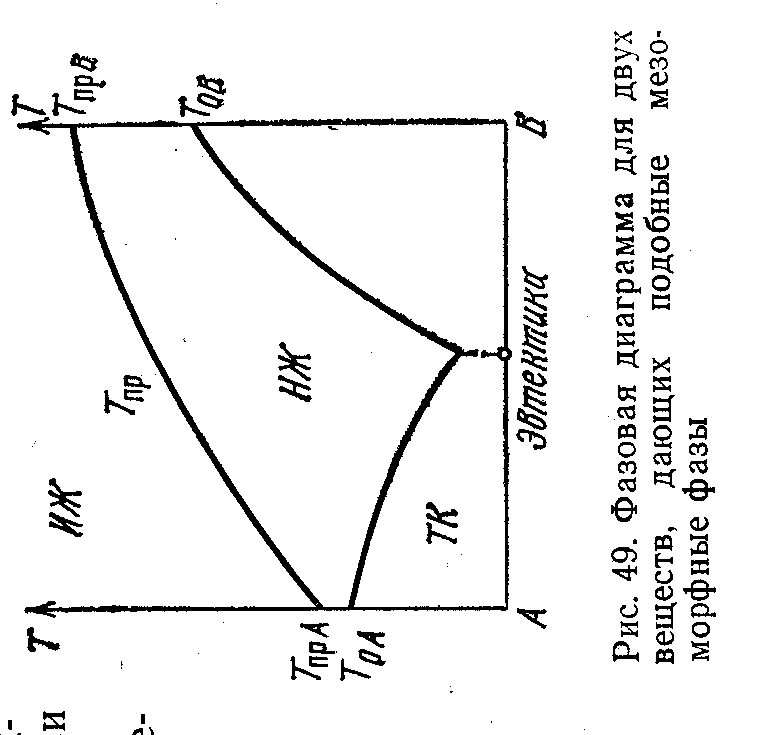
сильно меняются. Расширение этой области достигается подбором веществ, образующих эвтектики (рис. 95):
|
Рис. 94. Схема распределения температур фазовых переходов при охлаждении и при нагревании образца.
|
|
Рис. 95. Фазовая диаграмма для двух веществ, дающих подобные мезоморфные фазы. |
При этом достигается и расширение диапазона полей (в том числе электрического), в котором изменяются свойства ЖК.
Характер взаимодействия в молекулярных системах подробно рассматривался нами в курсе «Физическая химия стекла». Поскольку это всё - молекулярные вещества, характер взаимодействия между молекулами Ван-дер-Ваальсовский. Силы взаимодействия между молекулами слабы, изменения ориентации молекул (вращение и пр.) достигаются за счёт преодоления небольших барьеров. Разные состояния разделены небольшими величинами свободной энергии.
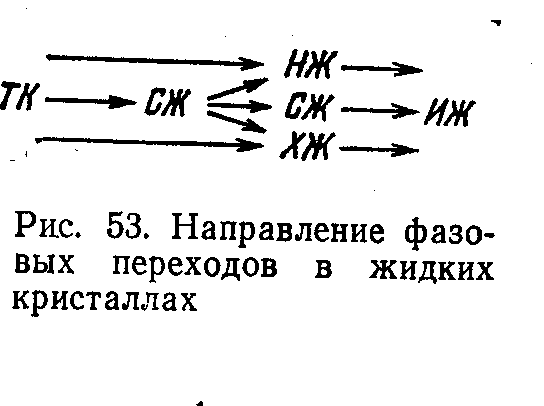
Фазовые переходы из кристаллического состояния в мезофазное или переходы твердый кристалл- нематик (ТК-НЖ), твердый кристалл - смектик (ТК-СЖ), твердый кристалл- холестерик (ТК-ХЖ)67 являются для всех известных веществ переходами I рода. Энтропия превращения порядка 10R, что обычно для энтропий плавления. Переходы I рода соответствуют переходу к изотропной жидкости, или переходы НЖ-ИЖ, СЖ-ИЖ, ХЖ-ИЖ. Изменения энтропии при этом на один-два порядка меньше, чем в предыдущем случае. Но полимезофазные переходы могут относиться как к истинным переходам II рода, так и квазифазовым переходам II рода. Фазовые переходы в смектических ЖК представлены схемой (рис. 96):
|
Рис. 96. Направление фазовых переходов нематиков. |
г) влияние электрического поля на фазовые переходов нематиков
Для нас важна причина того, почему при малой напряженности электрического поля мезофазы способны переходить одна в другую. Этот переход, как понятно из предыдущего, принципиально меняет характер распространения света из- за оптической анизотропии каждой фазы и специфического характера этой анизотропии. Наиболее просто описывается влияние напряженности поля на температуру перехода.
Если в точке фазового перехода изменяется диэлектрическая постоянная вещества, то приложенное электрическое поле сдвигает температуру фазового перехода из нематического состояния в изотропное на величину
∆T = (T0/q)[(ε2−ε1)/8πρ]E2,
где ε1 и ε2 − диэлектрические постоянные соответственно для низшей и высшей точек фазового перехода; T0 – температура фазового перехода при напряженностях электрического поля E = 0; ρ – плотность вещества; q – теплота фазового перехода на единицу массы.