- •Специальные разделы оптического материаловедения
- •Термодинамика фазовых равновесий
- •1.1 Общие сведения о термодинамике
- •1 Предмет термодинамики1
- •1.1.2 Термодинамическая система, виды систем
- •Изолированные системы – те, которые не имеют возможности обмениваться веществом и энергией с окружением и имеющие постоянный объем.
- •1.1.3 Параметры состояния, параметры процессов
- •1.1.4 Функции состояния
- •1.1.5 Виды процессов
- •1.1.6 Внутренняя энергия, теплота и работа
- •1.1.7 Максимальная работа при изобарических, изотермических, адиабатических и изохорных процессах
- •1.2 Законы термодинамики
- •1.2.2 II закон термодинамики и энтропия как термодинамическая функция
- •1.2.3 Энтропия и термодинамическая вероятность. III закон термодинамики
- •Следствия Законов
- •1.2.5 Термодинамические функции, важные для материаловедения.
- •1.2.6 Применение термодинамических понятий в других областях науки
- •1.3 Производные термодинамических потенциалов и фазовые переходы
- •1.3.1 Первые производные термодинамических потенциалов, их физический
- •1.3.2 Вторые производные термодинамических потенциалов (соотношения
- •1.3.3 Фазовые переходы I и II рода.
- •1.3.4 Фазовые переходы I рода. Барическая зависимость фазовых переходов I рода:
- •1.4 Теория фазовых равновесий
- •1.4.1 Понятия «фазовые равновесия», «компонент», «диаграмма состояний»,
- •1.4.2 Понятие химического потенциала. Условия равновесия фаз. Правило фаз
- •1.4.3 Диаграмма состояний однокомпонентной системы
- •1.4.5 Эвтектики (двухкомпонентные системы). Линии ликвидуса и солидуса.
- •1.4.6 Твердые растворы (двухкомпонентные системы). Значение твердых
- •1.4.7 Ограниченные твердые растворы
- •1.4.8 Упорядочение твердых растворов
- •1.4.9 Полная несмешиваемость в жидком и в твердом состояниях
- •1.4.10 Системы с расслаиванием в жидком состоянии. Стабильное и
- •1.4.11 Системы с образованием химических соединений (двухкомпонентные
- •1.4.12 Системы с образованием химических соединений (двухкомпонентные
- •1.4.13 Трёхкомпонентные системы (принципы изображения,
- •1.4.14 Комбинация элементов диаграмм состояний. Физико-химический анализ.
- •2. Фазовые переходы и кинетическая теория стеклования
- •2.1 Стеклование
- •2.1.1 Принципиальная особенность фазовых переходов I и II рода в общей
- •2.1.2 Природа взаимодействия в конденсированных системах (общие
- •Ионное взаимодействие
- •Взаимодействие в металлах
- •Ковалентное взаимодействие
- •Водородные связи
- •Взаимодействие Ван-дер-Ваальса
- •Энергия химических связей
- •2.1.3 Основные особенности строения жидкостей и принцип их обобщенного
- •2.1.4 Общие сведения о релаксационных процессах как о процессах перехода от
- •2.1.5 Равновесные и мгновенные свойства жидкостей
- •2.1.6 Переохлажденные жидкости как частный случай метастабильного
- •2.1.7 Проявление стеклования на свойствах жидкостей
- •2.1.8 Определение стеклообразного состояния как лабильного (абсолютно
- •2.1.9 Математическое описание стеклования в кинетической теории. Твердо- и
- •2.1.10 Время релаксации структуры и его зависимость от температуры.
- •2.1.11 Соотношение температур стеклования и плавления (правило «2/3»
- •2.2 Кристаллизация расплавов стекол
- •2.2.1 Термодинамические особенности метастабильной жидкости
- •2.2.2 Работа образования зародыша кристаллизации20
- •2.2.3 Кривые Таммана а) скорость зарождения и кривая зарождения.
- •Б) скорость роста и кривая роста.
- •2.2.4 Методы изучения кристаллизационной способности и её
- •А) политермический метод и диаграммы кристаллизационной способности
- •Б) фазовый состав и морфология кристаллов.
- •В) дифференциальный термический анализ.
- •Г) скорость кристаллизации
- •2.2.5 Типы кристаллизации
- •2.2.6 Катализированная кристаллизация; ситаллы
- •2.2.7 Связь кристаллизационной способности с диаграммой состояния
- •3.Термодинамика стеклообразного состояния
- •3.1.1 Термодинамические переменные, используемые при математическом
- •3.1.2 Математическое описание избыточной свободной энергии лабильной
- •3.1.3 Математическое условие стеклования, налагаемое на изменения
- •3.1.4 Соотношение Пригожина-Дефея и его экспериментальная проверка
- •3.1.5 Термодинамический инвариант стеклообразного состояния
- •3.1.6 Следствия, вытекающие из соотношений термодинамики
- •5. Релаксационные процессы в стеклообразном состоянии. Ионная проводимость и ионный обмен
- •5.1.1 Зависимость температуры стеклования от скорости охлаждения
- •5.1.2 Процессы и законы релаксационных изменений свойств, структурная
- •5.1.3 Оценка времени достижения равновесного состояния в процессе отжига
- •5.1.4 Физическое старение стекла при комнатной температуре52
- •5.1.5 Релаксационные явления при переходе через температуру стеклования
- •5.1.6 «Кроссовер эффект»
- •5.1.7 Расчёт изменения свойств при отжиге стекол на основании
- •5.2 Природа ионной проводимости и диффузии в стеклах.
- •5.2.1 Структура стекла и основы механизма
- •5.2.2 Законы диффузии и соотношение Нернста – Эйнштейна
- •5.2.3 Основное статистическое уравнение проводимости. Энергия активации.
- •5.2.4 Общие корреляции, ряд подвижностей
- •5.2.5 Основные закономерности электропроводности, определяемые составом
- •5.2.6 Ионообменные процессы и проблемы современной оптической технологии
- •5.2.7 Ионообменные процессы с растворами. Стеклянный электрод.
- •6. Взаимосвязь между основными видами релаксационных процессов в стеклах
- •6.4.1 Соотношение Максвелла для проводимости диэлектриков
- •6.4.2 Соотношение Максвелла для проводимости диэлектриков как основа связи
- •6.4.3 Экспериментальная проверка возможности расчёта температуры «ионного» максимума внутреннего трения по данным проводимости
- •7. Основные принципы химической устойчивости стекол
- •7.1.1 Практическая значимость свойства и его физико-химическое
- •7.1.2 Методы испытания и классификация стекол по группам
- •Группы химической устойчивости бесцветного оптического стекла к действию кислоты и дистиллированной воды
- •Группы химической устойчивости бесцветного оптического стекла к действию влажной атмосферы
- •7.1.3 Влияние компонентов состава стекла на химическую устойчивость
- •7.1.4 Способы защиты оптических деталей от химического разрушения
- •8. Специфика некоторых структурных явлений в регистрирующих средах
- •8.1. Фотоструктурные изменения в халькогенидных стеклах, их существо и
- •8.2 Структурно-фазовые изменения в жидких кристаллах и физико-химическая
- •8.2.1 Общие представления о жидких кристаллах
- •8.2.2 Специфика изменения электрических и магнитных свойств при
7.1.3 Влияние компонентов состава стекла на химическую устойчивость
Химически устойчивые оптические стекла не должны содержать более 10 – 13 мол.% оксидов щелочных металлов. Введение двух щелочных оксидов вместо одного желательно. Al2O3 и B2O3 (последний – не более 16%) способствуют повышению химической устойчивости.
Однако в каждом конкретном случае могут существовать и другие пути повышения устойчивости. К сожалению, это свойство относится к разряду наименее предсказуемых, поскольку процессы химического разрушения чрезвычайно сложны, до сих пор недостаточно изучены и потому во многом непонятны.
7.1.4 Способы защиты оптических деталей от химического разрушения
я и биологических образований
Обычно просветление оптических деталей одновременно является и защитой от химического разрушения. Особого внимания заслуживает защита стекол от разрушения в тропических условиях, когда на поверхности возникают обрастания биологической природы. Деятельность бактерий и грибов приводит к выделению особо неблагоприятных для поверхности стекла веществ. Существует ряд методов защиты поверхности фунгицидами – веществами, препятствующих биологическому разрушению, в их состав входят соединения ртути.
О старинном методе «восковой» защиты упоминалось выше.
Если оптическая деталь «работает» внутри герметически закрытой системы (например, объектива), то требования к химической устойчивости снижаются.
8. Специфика некоторых структурных явлений в регистрирующих средах
8.1. Фотоструктурные изменения в халькогенидных стеклах, их существо и
практическое использование
При действии света на халькогенидные стекла наблюдается совокупность изменений свойств, которые называют фотоструктурными изменениями. Изменяются электропроводность, пропускание и др. свойства. Проявление этих изменений зависит от длины волны, температуры, состава стекла и, в особенности, от величины ширины запрещенной зоны. Эти изменения в выбранных условиях эксперимента могут быть как обратимыми, так и необратимыми.
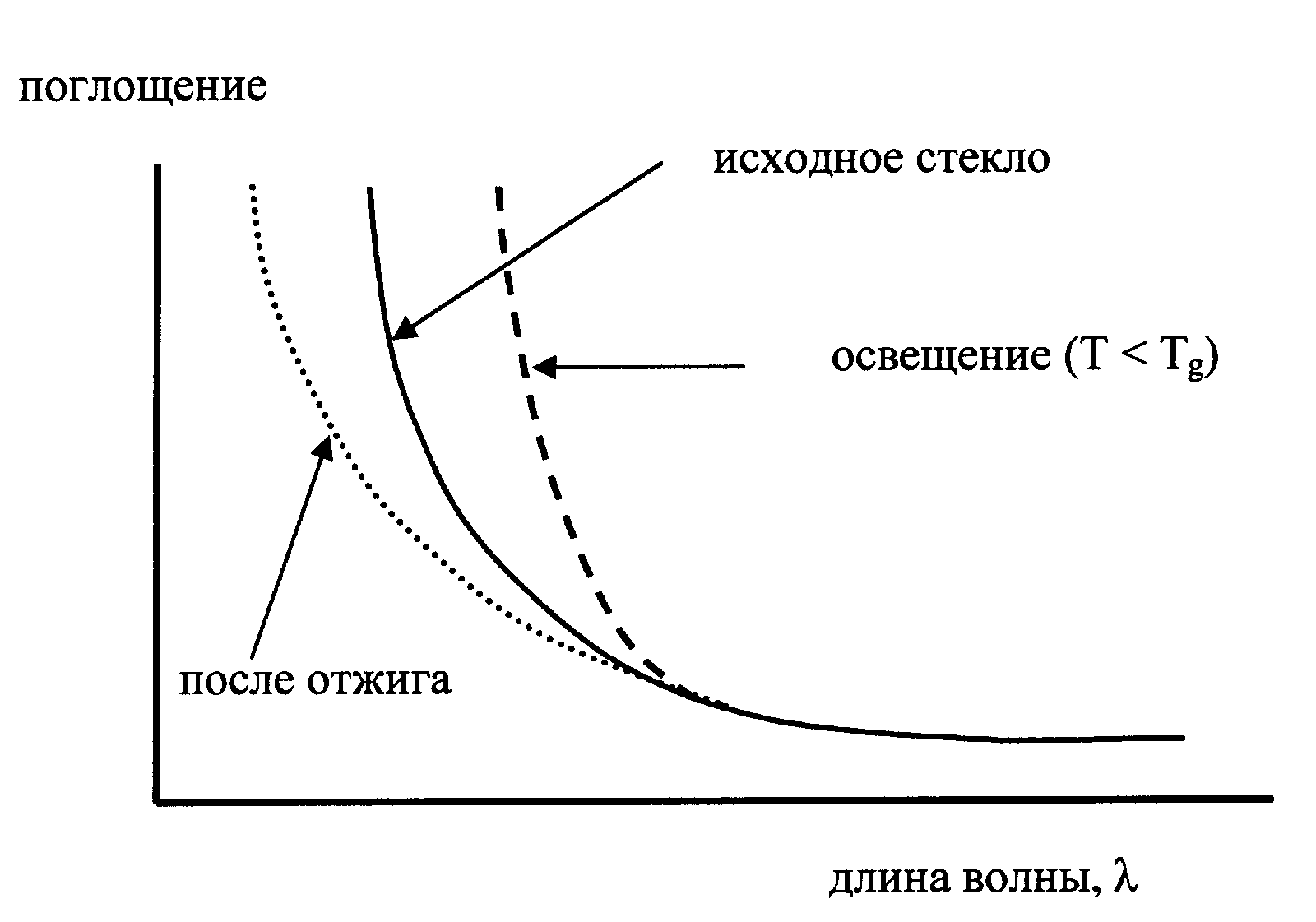
Фотоструктурные превращения проявляются прежде всего на оптических свойствах как явление потемнения образца в сильном световом потоке. Это потемнение может быть сохранено после выключения света. После прогрева до температуры, близкой к Тg, охлажденные стекла просветляются и граница пропускания может оказаться даже сдвинутой в сторону коротких длин волн (рис. 89).
|
Рис. 89. Принципиальный характер изменения границы коротковолнового поглощения халькогенидного стекла при освещении и последующем глубоком отжиге. |
Это явление впервые наблюдали и изучали в 70-х – 80 годах Б.Т.Коломиец, В.М. Любин (ФТИ РАН), Танака (Япония) и затем многие другие. В настоящее время интерпретация явления состоит в том, что свет вызывает в локальных областях поверхностного слоя стекла разложение структурных единиц. Например,
As2S3 → As + S.
Такая схема была подтверждена прямыми рентгеновскими данными.
Поскольку продукты разложения локализованы, они будут сохраняться и поглощать свет (мышьяк – это металл) до тех пор, пока температура не повысится и не стимулирует обратный процесс. В стекле даже после отжига могут быть примеси продуктов термической диссоциации. Поэтому пропускание тщательно отожженного стела может оказаться даже выше, чем оно было вначале (о роли термических дефектов в пропускании кварцевого стекла уже говорилось ранее). В модели зонной структуры эти состояния соответствуют состояниям, локализованным внутри запрещенной зоны, отжиг или свет меняют плотность таких состояний.
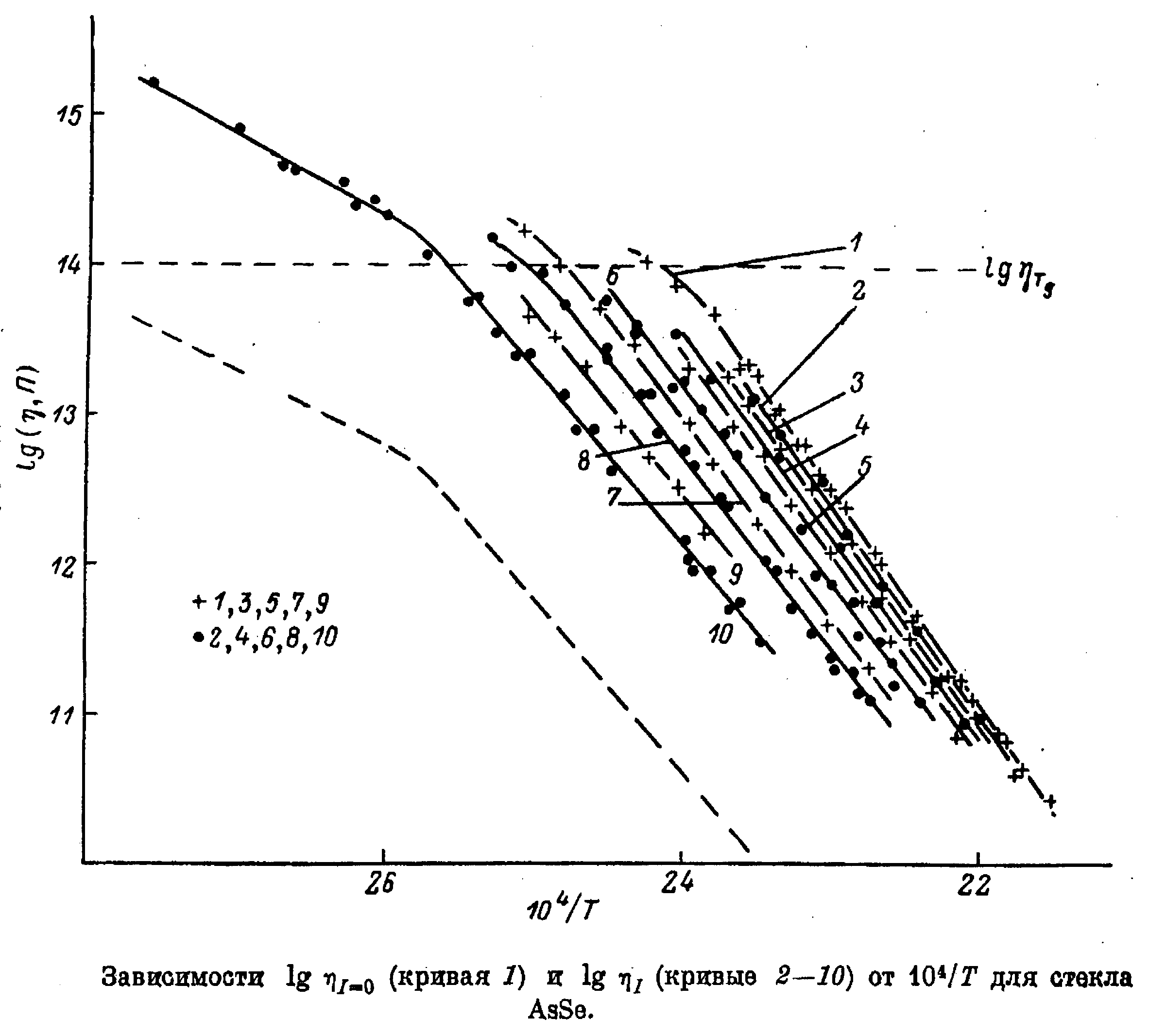
Особенно интересным оказалось обнаружение фотоэффекта при температурах выше температуры стеклования, состоящего в стационарном (существующем пока действует свет) уменьшении вязкости (Д.К.Таганцев и С.В. Немилов, 1981 – 1989гг.). В зависимости от длины волны света и его интенсивности изменение вязкости может достигать нескольких порядков величины – рис. 90.
Зависимость от интенсивности подчиняется закону
ηI=0/ηI = exp (α∙I).
Здесь ηI=0 и ηI – вязкости в темноте и при световом потоке I, а α – коэффициент, определяющий эффективность взаимодействия света с веществом. Коэффициент α зависит от температуры и длины волны. Для области прозрачности (глубокая ИК область) эффект отсутствует, для области полного поглощения эффект также отсутствует. Он максимален, когда энергия кванта света соизмерима с шириной запрещенной зоны (актиничный свет). Существенно, что в экспериментах был исключен эффект снижения вязкости из-за термического нагрева, вызванного превращением света в тепло.
|
Рис. 90. Зависимости lgηI=0 (кривая 1) и lgηI (кривые 2-10) от 104/Т для стекла AsSe.Относительные интенсивности: 0,065 (2), 0,11 (3), 0,19 (4), 0,24 (5), 0,37 (6), 0,52 (7), 0,61 (8), 0,79 (9), 1,00 (10). Штриховая кривая – экспериментальная зависимость lg ηI от 104/Т при относительной интенсивности, равной 1,00, для которой не учтен температурный вклад. Источник света – ксеноновя лампа (1200 – 300 нм). ηI=0 – вязкость в темноте, ηI – вязкость на свету. Д.К. Таганцев, С.В.Немилов Физика и химия стекла, т. 15, № 6, 397-409 (1989).
|
Теория этого явления полагает, что свет производит локальное разрыхление структуры из-за перевода электронов химических связей в возбужденное состояние, эти возбужденные состояния быстро диффундируют внутрь образца, вызывая снижение коэффициента вязкого течения в объеме вещества. Высокая скорость диффузии последних была позднее подтверждена независимыми экспериментами. В терминах зонной теории фотовязкостной эффект связан с изменением заселенности состояний, локализованных внутри запрещенной зоны.