- •Специальные разделы оптического материаловедения
- •Термодинамика фазовых равновесий
- •1.1 Общие сведения о термодинамике
- •1 Предмет термодинамики1
- •1.1.2 Термодинамическая система, виды систем
- •Изолированные системы – те, которые не имеют возможности обмениваться веществом и энергией с окружением и имеющие постоянный объем.
- •1.1.3 Параметры состояния, параметры процессов
- •1.1.4 Функции состояния
- •1.1.5 Виды процессов
- •1.1.6 Внутренняя энергия, теплота и работа
- •1.1.7 Максимальная работа при изобарических, изотермических, адиабатических и изохорных процессах
- •1.2 Законы термодинамики
- •1.2.2 II закон термодинамики и энтропия как термодинамическая функция
- •1.2.3 Энтропия и термодинамическая вероятность. III закон термодинамики
- •Следствия Законов
- •1.2.5 Термодинамические функции, важные для материаловедения.
- •1.2.6 Применение термодинамических понятий в других областях науки
- •1.3 Производные термодинамических потенциалов и фазовые переходы
- •1.3.1 Первые производные термодинамических потенциалов, их физический
- •1.3.2 Вторые производные термодинамических потенциалов (соотношения
- •1.3.3 Фазовые переходы I и II рода.
- •1.3.4 Фазовые переходы I рода. Барическая зависимость фазовых переходов I рода:
- •1.4 Теория фазовых равновесий
- •1.4.1 Понятия «фазовые равновесия», «компонент», «диаграмма состояний»,
- •1.4.2 Понятие химического потенциала. Условия равновесия фаз. Правило фаз
- •1.4.3 Диаграмма состояний однокомпонентной системы
- •1.4.5 Эвтектики (двухкомпонентные системы). Линии ликвидуса и солидуса.
- •1.4.6 Твердые растворы (двухкомпонентные системы). Значение твердых
- •1.4.7 Ограниченные твердые растворы
- •1.4.8 Упорядочение твердых растворов
- •1.4.9 Полная несмешиваемость в жидком и в твердом состояниях
- •1.4.10 Системы с расслаиванием в жидком состоянии. Стабильное и
- •1.4.11 Системы с образованием химических соединений (двухкомпонентные
- •1.4.12 Системы с образованием химических соединений (двухкомпонентные
- •1.4.13 Трёхкомпонентные системы (принципы изображения,
- •1.4.14 Комбинация элементов диаграмм состояний. Физико-химический анализ.
- •2. Фазовые переходы и кинетическая теория стеклования
- •2.1 Стеклование
- •2.1.1 Принципиальная особенность фазовых переходов I и II рода в общей
- •2.1.2 Природа взаимодействия в конденсированных системах (общие
- •Ионное взаимодействие
- •Взаимодействие в металлах
- •Ковалентное взаимодействие
- •Водородные связи
- •Взаимодействие Ван-дер-Ваальса
- •Энергия химических связей
- •2.1.3 Основные особенности строения жидкостей и принцип их обобщенного
- •2.1.4 Общие сведения о релаксационных процессах как о процессах перехода от
- •2.1.5 Равновесные и мгновенные свойства жидкостей
- •2.1.6 Переохлажденные жидкости как частный случай метастабильного
- •2.1.7 Проявление стеклования на свойствах жидкостей
- •2.1.8 Определение стеклообразного состояния как лабильного (абсолютно
- •2.1.9 Математическое описание стеклования в кинетической теории. Твердо- и
- •2.1.10 Время релаксации структуры и его зависимость от температуры.
- •2.1.11 Соотношение температур стеклования и плавления (правило «2/3»
- •2.2 Кристаллизация расплавов стекол
- •2.2.1 Термодинамические особенности метастабильной жидкости
- •2.2.2 Работа образования зародыша кристаллизации20
- •2.2.3 Кривые Таммана а) скорость зарождения и кривая зарождения.
- •Б) скорость роста и кривая роста.
- •2.2.4 Методы изучения кристаллизационной способности и её
- •А) политермический метод и диаграммы кристаллизационной способности
- •Б) фазовый состав и морфология кристаллов.
- •В) дифференциальный термический анализ.
- •Г) скорость кристаллизации
- •2.2.5 Типы кристаллизации
- •2.2.6 Катализированная кристаллизация; ситаллы
- •2.2.7 Связь кристаллизационной способности с диаграммой состояния
- •3.Термодинамика стеклообразного состояния
- •3.1.1 Термодинамические переменные, используемые при математическом
- •3.1.2 Математическое описание избыточной свободной энергии лабильной
- •3.1.3 Математическое условие стеклования, налагаемое на изменения
- •3.1.4 Соотношение Пригожина-Дефея и его экспериментальная проверка
- •3.1.5 Термодинамический инвариант стеклообразного состояния
- •3.1.6 Следствия, вытекающие из соотношений термодинамики
- •5. Релаксационные процессы в стеклообразном состоянии. Ионная проводимость и ионный обмен
- •5.1.1 Зависимость температуры стеклования от скорости охлаждения
- •5.1.2 Процессы и законы релаксационных изменений свойств, структурная
- •5.1.3 Оценка времени достижения равновесного состояния в процессе отжига
- •5.1.4 Физическое старение стекла при комнатной температуре52
- •5.1.5 Релаксационные явления при переходе через температуру стеклования
- •5.1.6 «Кроссовер эффект»
- •5.1.7 Расчёт изменения свойств при отжиге стекол на основании
- •5.2 Природа ионной проводимости и диффузии в стеклах.
- •5.2.1 Структура стекла и основы механизма
- •5.2.2 Законы диффузии и соотношение Нернста – Эйнштейна
- •5.2.3 Основное статистическое уравнение проводимости. Энергия активации.
- •5.2.4 Общие корреляции, ряд подвижностей
- •5.2.5 Основные закономерности электропроводности, определяемые составом
- •5.2.6 Ионообменные процессы и проблемы современной оптической технологии
- •5.2.7 Ионообменные процессы с растворами. Стеклянный электрод.
- •6. Взаимосвязь между основными видами релаксационных процессов в стеклах
- •6.4.1 Соотношение Максвелла для проводимости диэлектриков
- •6.4.2 Соотношение Максвелла для проводимости диэлектриков как основа связи
- •6.4.3 Экспериментальная проверка возможности расчёта температуры «ионного» максимума внутреннего трения по данным проводимости
- •7. Основные принципы химической устойчивости стекол
- •7.1.1 Практическая значимость свойства и его физико-химическое
- •7.1.2 Методы испытания и классификация стекол по группам
- •Группы химической устойчивости бесцветного оптического стекла к действию кислоты и дистиллированной воды
- •Группы химической устойчивости бесцветного оптического стекла к действию влажной атмосферы
- •7.1.3 Влияние компонентов состава стекла на химическую устойчивость
- •7.1.4 Способы защиты оптических деталей от химического разрушения
- •8. Специфика некоторых структурных явлений в регистрирующих средах
- •8.1. Фотоструктурные изменения в халькогенидных стеклах, их существо и
- •8.2 Структурно-фазовые изменения в жидких кристаллах и физико-химическая
- •8.2.1 Общие представления о жидких кристаллах
- •8.2.2 Специфика изменения электрических и магнитных свойств при
2.1.11 Соотношение температур стеклования и плавления (правило «2/3»
Кауцмана)
В.Кауцман (США) в 1948 г. эмпирически показал, что между Tg и значением нормальной температуры плавления Тпл. существует приближенное соотношение: Tg/Тпл. ≈ 2/3. Это правило чрезвычайно полезно для практики18. В таблице 1 приведены примеры величин отношения Tg/Тпл. За значение Tg принято значение температуры, соответствующей вязкости 1013 П. Среднее значение Tg/Тпл здесь составляет 0.655.
Таблица 1. Правило "2/3" Кауцмана на примере простых соединений.
Соединение |
Т пл., К |
η, П, при Тпл. |
Тg, K |
Tg/Tпл. |
SiO2 |
1998 |
~ 107 |
1500 |
0.75 |
GeO2 |
1390 |
7∙105 |
853 |
0.61 |
B2O3 |
723 |
1∙105 |
550 |
0.76 |
P2O5 |
853 |
5∙106 |
573 |
0.63 |
As2O3 |
585 |
1∙106 |
420 |
0.72 |
BeF2 |
823 |
>106 |
523 |
0.64 |
Na2B4O7 |
1015 |
101.70 |
720 |
0.71 |
глицерин |
291 |
101.20 |
183 |
0.63 |
селен |
494 |
101.3 |
300 |
0.61 |
о-терфенил |
329 |
0.296 |
244 |
0.74 |
Этиловый спирт C2H5OH |
159 |
1.34 |
90 |
0.57 |
Вода H2O |
273 |
~0.01 |
~135 |
0.5 |
Очевидно, что вязкость при температуре плавления (или равновесной кристаллизации) может быть любой, но время релаксации при температуре стеклования Tg всегда по порядку величины близко к 103 с. Естественно предположение, что кристаллизация расплава будет происходить легче при малой вязкости, когда время релаксации мало. Мы забегаем вперёд и упомянем здесь лишь, что время релаксации и сдвиговая вязкость пропорциональны в соответствии с уравнением релаксации Максвелла.
2.2 Кристаллизация расплавов стекол
2.2.1 Термодинамические особенности метастабильной жидкости
Выше
мы уже ввели определение переохлажденной
метастабильной
жидкости как состояния, которое
может сохраняться без изменений сколь
угодно долго, если в жидкость не внести
кристаллик (затравку кристаллизации)19.
В термодинамике
устойчивость системы определяет
свободная энергия Гиббса G.
При переохлаждении (при переходе через
температуру равновесной кристаллизации
или плавления) свободная энергия жидкости
изменяется плавно, в своей зависимости
от температуры кривая не претерпевает
никаких изломов (штриховая линия на
рис. 29); состояние стабильной жидкости
(ж) сменяется состоянием метастабильной
жидкости (мсж). Напротив, при кристаллизации
ход свободной энергии претерпевает
излом (он связан с энтропией плавления,
так как
![]() =
-∆S) и свободная энергия
кристалла становится ниже таковой
для метастабильной переохлажденной
жидкости на величину G(мсж)
– G(к) = ∆G(мсж-к).
Таким образом, при переохлаждении
метастабильная жидкость приобретает
избыток свободной энергии по
отношению к кристаллу при той же
температуре.
=
-∆S) и свободная энергия
кристалла становится ниже таковой
для метастабильной переохлажденной
жидкости на величину G(мсж)
– G(к) = ∆G(мсж-к).
Таким образом, при переохлаждении
метастабильная жидкость приобретает
избыток свободной энергии по
отношению к кристаллу при той же
температуре.
|
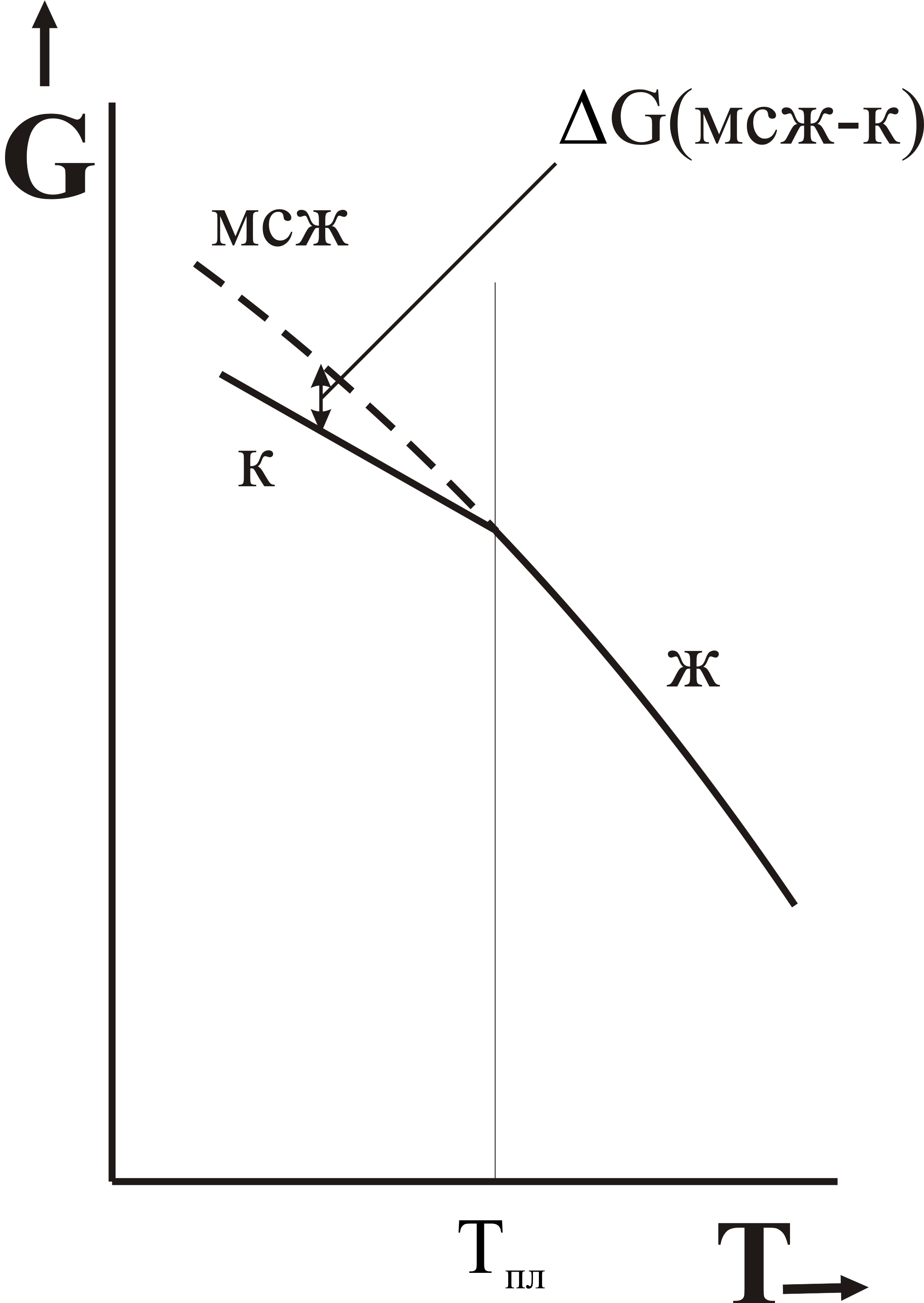
Рис. 29. Возникновение избытка свободной энергии переохлажденной метастабильной жидкости (мсж) относительно состояния кристалла (к). |
С ростом переохлаждения (разницы Tпл – Т) величина ∆G(мсж-к) увеличивается. Её значение приближенно может быть рассчитано по соотношению ∆G(мсж-к) = ∆Sпл∙(Tпл – Т), где ∆Sпл – энтропия плавления, находимая как ∆Hпл/Тпл.
Кристаллизация стеклообразующего расплава – это тоже фазовый переход I рода. Но он в условиях переохлаждения протекает необратимо. Движущей силой этого процесса является избыток свободной энергии расплава по отношению к кристаллической фазе, ∆G(мсж-к). Природа этого процесса кратко рассмотрена ниже.