- •Специальные разделы оптического материаловедения
- •Термодинамика фазовых равновесий
- •1.1 Общие сведения о термодинамике
- •1 Предмет термодинамики1
- •1.1.2 Термодинамическая система, виды систем
- •Изолированные системы – те, которые не имеют возможности обмениваться веществом и энергией с окружением и имеющие постоянный объем.
- •1.1.3 Параметры состояния, параметры процессов
- •1.1.4 Функции состояния
- •1.1.5 Виды процессов
- •1.1.6 Внутренняя энергия, теплота и работа
- •1.1.7 Максимальная работа при изобарических, изотермических, адиабатических и изохорных процессах
- •1.2 Законы термодинамики
- •1.2.2 II закон термодинамики и энтропия как термодинамическая функция
- •1.2.3 Энтропия и термодинамическая вероятность. III закон термодинамики
- •Следствия Законов
- •1.2.5 Термодинамические функции, важные для материаловедения.
- •1.2.6 Применение термодинамических понятий в других областях науки
- •1.3 Производные термодинамических потенциалов и фазовые переходы
- •1.3.1 Первые производные термодинамических потенциалов, их физический
- •1.3.2 Вторые производные термодинамических потенциалов (соотношения
- •1.3.3 Фазовые переходы I и II рода.
- •1.3.4 Фазовые переходы I рода. Барическая зависимость фазовых переходов I рода:
- •1.4 Теория фазовых равновесий
- •1.4.1 Понятия «фазовые равновесия», «компонент», «диаграмма состояний»,
- •1.4.2 Понятие химического потенциала. Условия равновесия фаз. Правило фаз
- •1.4.3 Диаграмма состояний однокомпонентной системы
- •1.4.5 Эвтектики (двухкомпонентные системы). Линии ликвидуса и солидуса.
- •1.4.6 Твердые растворы (двухкомпонентные системы). Значение твердых
- •1.4.7 Ограниченные твердые растворы
- •1.4.8 Упорядочение твердых растворов
- •1.4.9 Полная несмешиваемость в жидком и в твердом состояниях
- •1.4.10 Системы с расслаиванием в жидком состоянии. Стабильное и
- •1.4.11 Системы с образованием химических соединений (двухкомпонентные
- •1.4.12 Системы с образованием химических соединений (двухкомпонентные
- •1.4.13 Трёхкомпонентные системы (принципы изображения,
- •1.4.14 Комбинация элементов диаграмм состояний. Физико-химический анализ.
- •2. Фазовые переходы и кинетическая теория стеклования
- •2.1 Стеклование
- •2.1.1 Принципиальная особенность фазовых переходов I и II рода в общей
- •2.1.2 Природа взаимодействия в конденсированных системах (общие
- •Ионное взаимодействие
- •Взаимодействие в металлах
- •Ковалентное взаимодействие
- •Водородные связи
- •Взаимодействие Ван-дер-Ваальса
- •Энергия химических связей
- •2.1.3 Основные особенности строения жидкостей и принцип их обобщенного
- •2.1.4 Общие сведения о релаксационных процессах как о процессах перехода от
- •2.1.5 Равновесные и мгновенные свойства жидкостей
- •2.1.6 Переохлажденные жидкости как частный случай метастабильного
- •2.1.7 Проявление стеклования на свойствах жидкостей
- •2.1.8 Определение стеклообразного состояния как лабильного (абсолютно
- •2.1.9 Математическое описание стеклования в кинетической теории. Твердо- и
- •2.1.10 Время релаксации структуры и его зависимость от температуры.
- •2.1.11 Соотношение температур стеклования и плавления (правило «2/3»
- •2.2 Кристаллизация расплавов стекол
- •2.2.1 Термодинамические особенности метастабильной жидкости
- •2.2.2 Работа образования зародыша кристаллизации20
- •2.2.3 Кривые Таммана а) скорость зарождения и кривая зарождения.
- •Б) скорость роста и кривая роста.
- •2.2.4 Методы изучения кристаллизационной способности и её
- •А) политермический метод и диаграммы кристаллизационной способности
- •Б) фазовый состав и морфология кристаллов.
- •В) дифференциальный термический анализ.
- •Г) скорость кристаллизации
- •2.2.5 Типы кристаллизации
- •2.2.6 Катализированная кристаллизация; ситаллы
- •2.2.7 Связь кристаллизационной способности с диаграммой состояния
- •3.Термодинамика стеклообразного состояния
- •3.1.1 Термодинамические переменные, используемые при математическом
- •3.1.2 Математическое описание избыточной свободной энергии лабильной
- •3.1.3 Математическое условие стеклования, налагаемое на изменения
- •3.1.4 Соотношение Пригожина-Дефея и его экспериментальная проверка
- •3.1.5 Термодинамический инвариант стеклообразного состояния
- •3.1.6 Следствия, вытекающие из соотношений термодинамики
- •5. Релаксационные процессы в стеклообразном состоянии. Ионная проводимость и ионный обмен
- •5.1.1 Зависимость температуры стеклования от скорости охлаждения
- •5.1.2 Процессы и законы релаксационных изменений свойств, структурная
- •5.1.3 Оценка времени достижения равновесного состояния в процессе отжига
- •5.1.4 Физическое старение стекла при комнатной температуре52
- •5.1.5 Релаксационные явления при переходе через температуру стеклования
- •5.1.6 «Кроссовер эффект»
- •5.1.7 Расчёт изменения свойств при отжиге стекол на основании
- •5.2 Природа ионной проводимости и диффузии в стеклах.
- •5.2.1 Структура стекла и основы механизма
- •5.2.2 Законы диффузии и соотношение Нернста – Эйнштейна
- •5.2.3 Основное статистическое уравнение проводимости. Энергия активации.
- •5.2.4 Общие корреляции, ряд подвижностей
- •5.2.5 Основные закономерности электропроводности, определяемые составом
- •5.2.6 Ионообменные процессы и проблемы современной оптической технологии
- •5.2.7 Ионообменные процессы с растворами. Стеклянный электрод.
- •6. Взаимосвязь между основными видами релаксационных процессов в стеклах
- •6.4.1 Соотношение Максвелла для проводимости диэлектриков
- •6.4.2 Соотношение Максвелла для проводимости диэлектриков как основа связи
- •6.4.3 Экспериментальная проверка возможности расчёта температуры «ионного» максимума внутреннего трения по данным проводимости
- •7. Основные принципы химической устойчивости стекол
- •7.1.1 Практическая значимость свойства и его физико-химическое
- •7.1.2 Методы испытания и классификация стекол по группам
- •Группы химической устойчивости бесцветного оптического стекла к действию кислоты и дистиллированной воды
- •Группы химической устойчивости бесцветного оптического стекла к действию влажной атмосферы
- •7.1.3 Влияние компонентов состава стекла на химическую устойчивость
- •7.1.4 Способы защиты оптических деталей от химического разрушения
- •8. Специфика некоторых структурных явлений в регистрирующих средах
- •8.1. Фотоструктурные изменения в халькогенидных стеклах, их существо и
- •8.2 Структурно-фазовые изменения в жидких кристаллах и физико-химическая
- •8.2.1 Общие представления о жидких кристаллах
- •8.2.2 Специфика изменения электрических и магнитных свойств при
5.2.4 Общие корреляции, ряд подвижностей
Строгое выражение для фактора подвижности по Мюллеру имеет вид:
ω = 1.1∙10-3(r0)2νe(kБT)-2∙exp(–Ea/RT).
Этот сомножитель от концентрации практически не зависит,
lgω = –Ea/2.3·RT + P0 ,
где P0 = -1.25±1, неточность предполагается обусловленной неточностью знания частоты колебаний, величин единичных смещений и т.д..
В итоге
lglg[M] + PT – ψ/2.3RT, где ψ = ∆Ф + 2 Еа.
Здесь PT = 4.98 + P0 = 3.7±1.
Теория позволяет оценивать предэкспоненциальный сомножитель исходя из концентрации проводящих ток ионов и позволяет установить различие в подвижности ионов – переносчиков тока. В пределах ∆P = Pэксперим.– Pтеоретич. = ±1 наблюдается последовательность уменьшения подвижностей катионов (боратные стекла):
Ag+ >Li+ >Na+ ≥K+> Rb+ ≥Cs+.
Эта последовательность предопределена величинами Еа. Представленный ряд подвижностей признан универсальным для всех типов стекол (силикатных, боратных, фосфатных). Чрезвычайно высокая проводимость содержащих серебро фосфатных стекол общеизвестна.
5.2.5 Основные закономерности электропроводности, определяемые составом
Влияние оксидов R2O и R′O
С ростом концентрации щелочного оксида в двухкомпонентных щелочносиликатных стеклах удельное сопротивление падает, проводимость растет. На рис. 69 приведен для
системы Na2O – SiO2, но характер зависимости один и тот же для всех щелочных ионов.
-
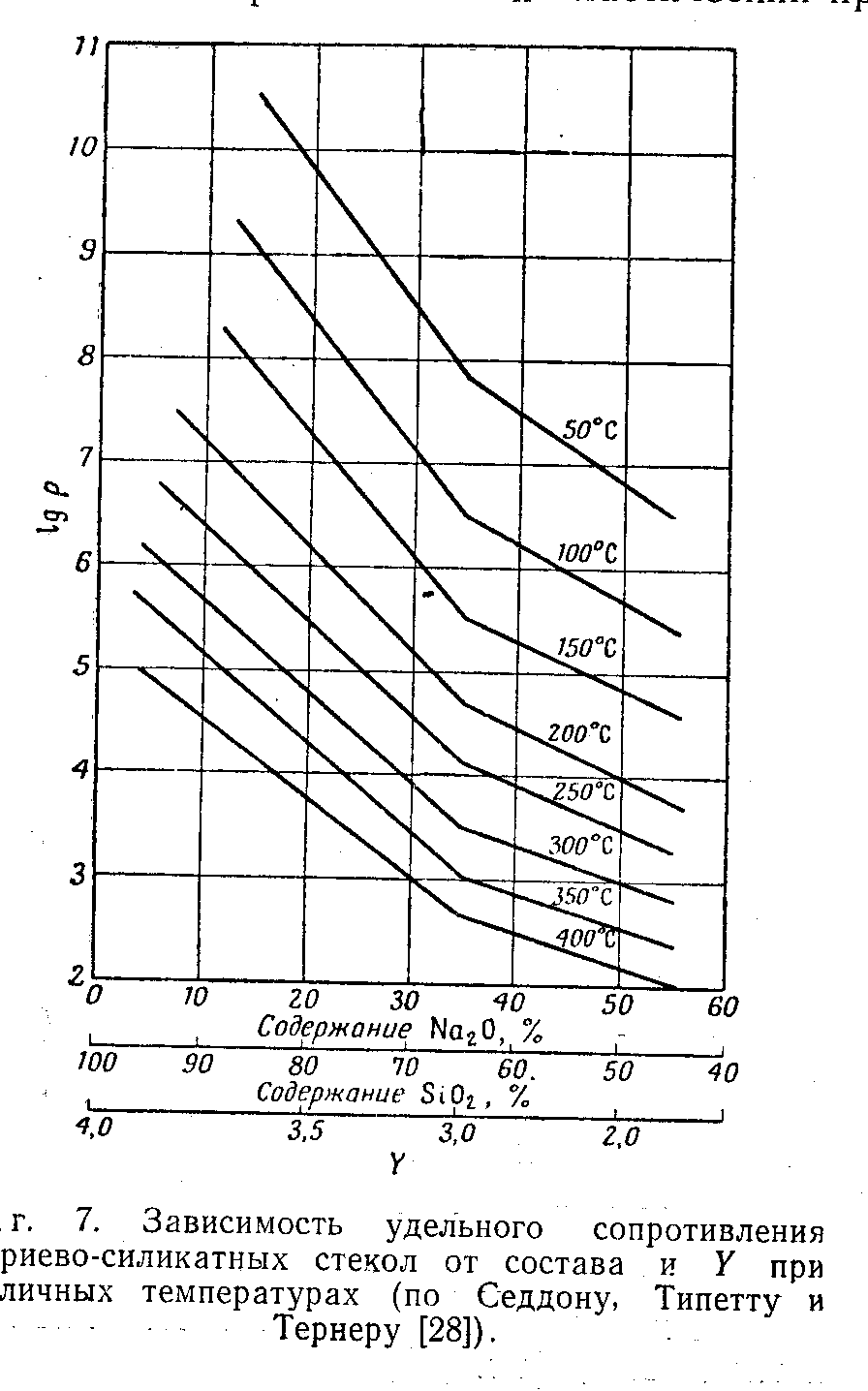
Рис. 69. Зависимость удельного
сопротивления стекол системы
Na2O-SiO2 от состава при
различных температурах
(E. Seddon, E.J.Tippett,
E.S.Turner. J. Soc. Glass
Technol.V.16, 450,1932).
|
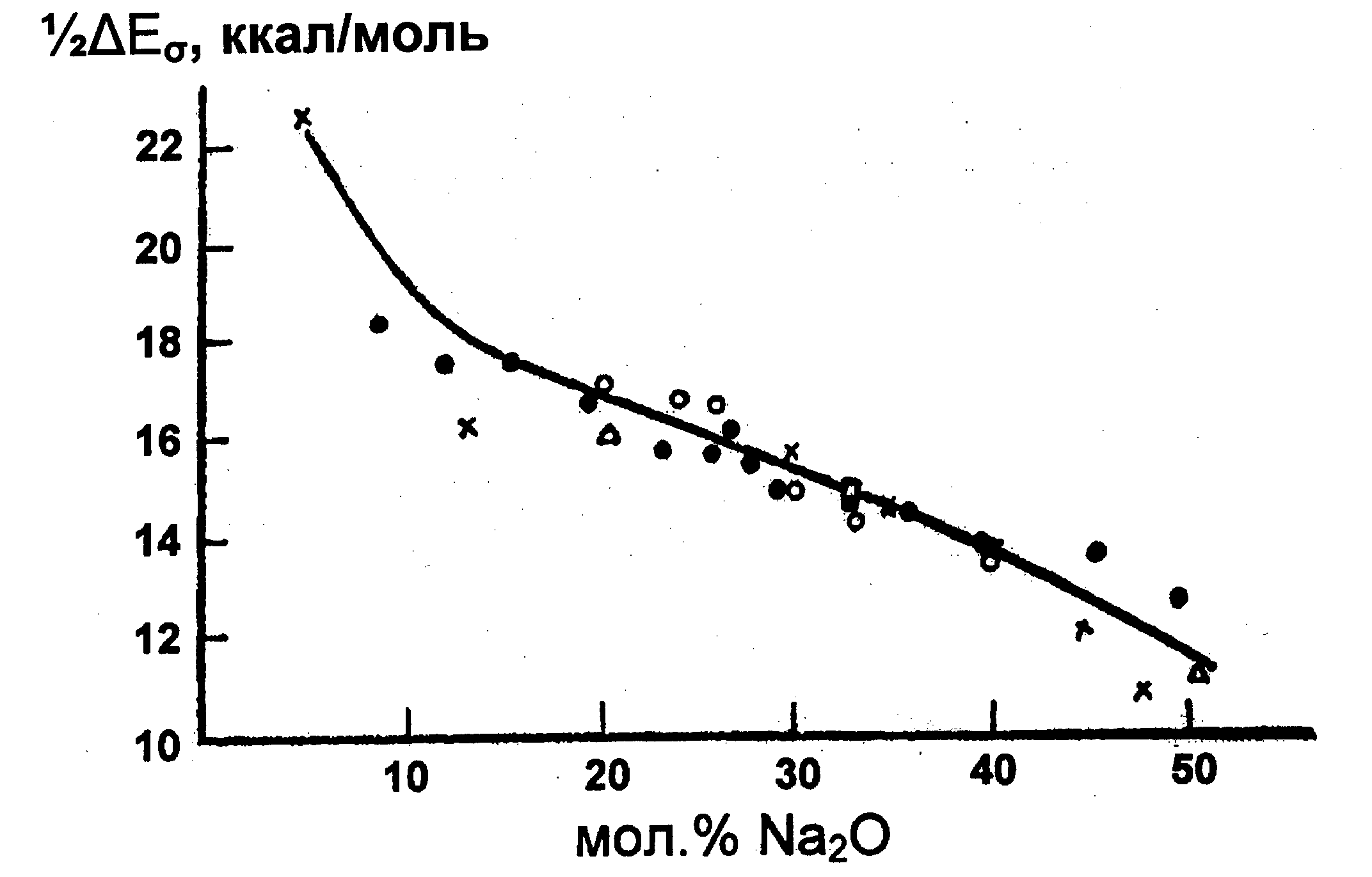
Рис. 70. Энергии активации проводимости стекол системы Na2O-SiO2 по данным различных авторов. Немилов, 1974.
|
Это – иллюстрация справедливости теоретических положений, изложенных выше. Энергия активации с составом изменяется подобным же образом (рис. 70).
|
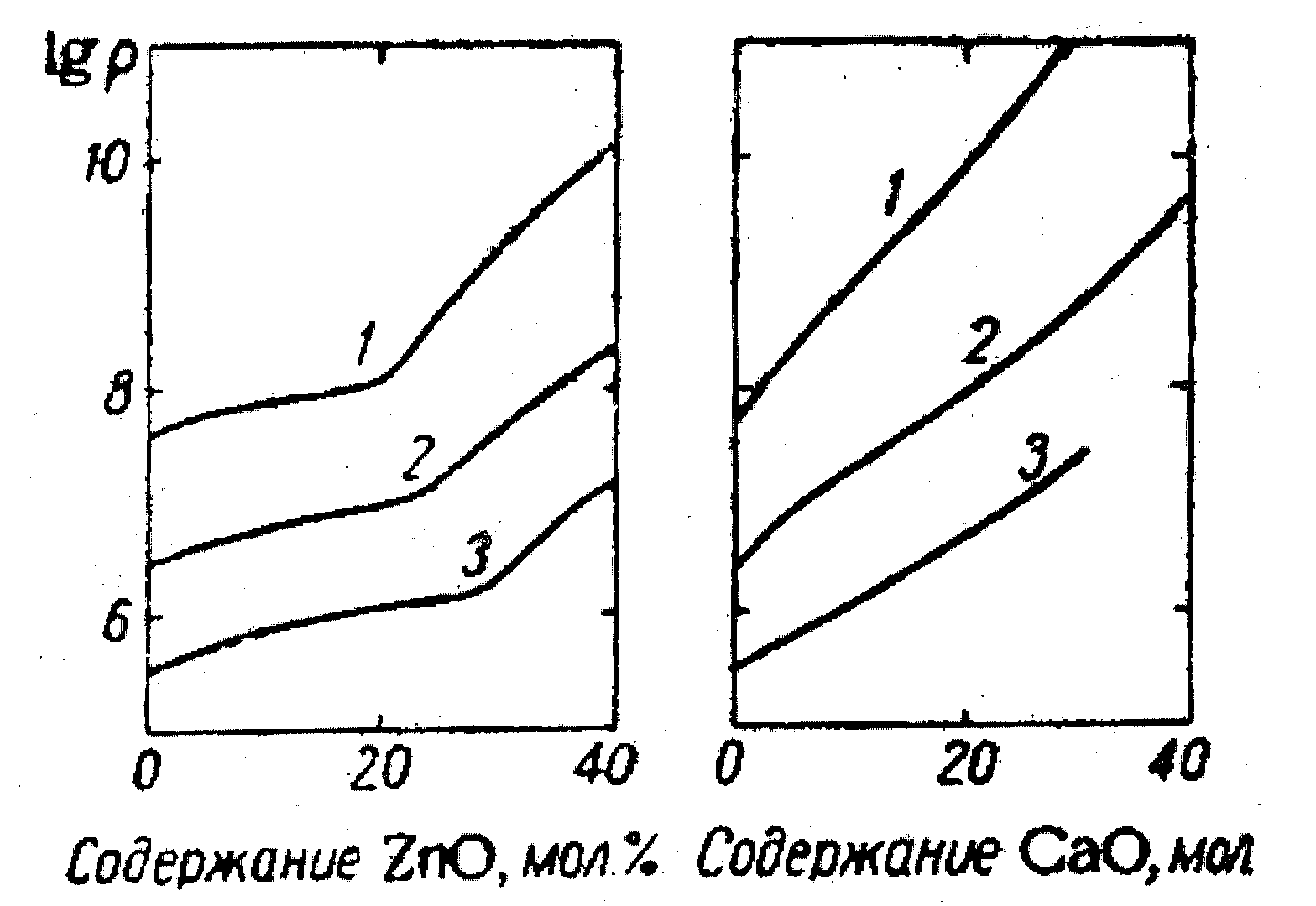
Рис. 71. Зависимость удельного сопротивления стекол систем Na2O-ZnO-SiO2 и Na2O-CaO- SiO2 при 150°С от состава (см. текст). О.В.Мазурин, Электрические свойства стекла. Л. 1962.
|
С ростом концентрации щелочноземельного оксида сопротивление возрастает на несколько порядков, что необъяснимо простым уменьшением количества ионов в единице объема. Кривые 1, 2, 3 на этом рисунке соответствуют сериям стекол с постоянным содержанием Na2O (10, 20 и 30 мол.%, соответственно номерам 1,2, 3). Такой же тип зависимостей наблюдается для систем с оксидами Mg, Be. При одной и той же концентрации оксида натрия бòльшее возрастание сопротивление вызывает катион R′ c бòльшим радиусом. Это было объяснено бòльшим влиянием на подвижность щелочного иона бòльшего по размеру катиона R′ («эффект торможения», О.В.Мазурин, Электрические свойства стекла, Л. 1962).. Таков ли этот механизм, сейчас не ясно. Очевидно, однако, что этот эффект велик и его нужно учитывать на практике.
Влияние оксидов Al2O3, B2O3 и Fe2O3
Пример влияния на сопротивление величины отношения Al2O3/Na2O в стеклах трехкомпонентной силикатной системы показан на рис. 72. Точно такого же типа зависимости наблюдались в системах с Ga2O3, B2O3 и Fe2O3.
-
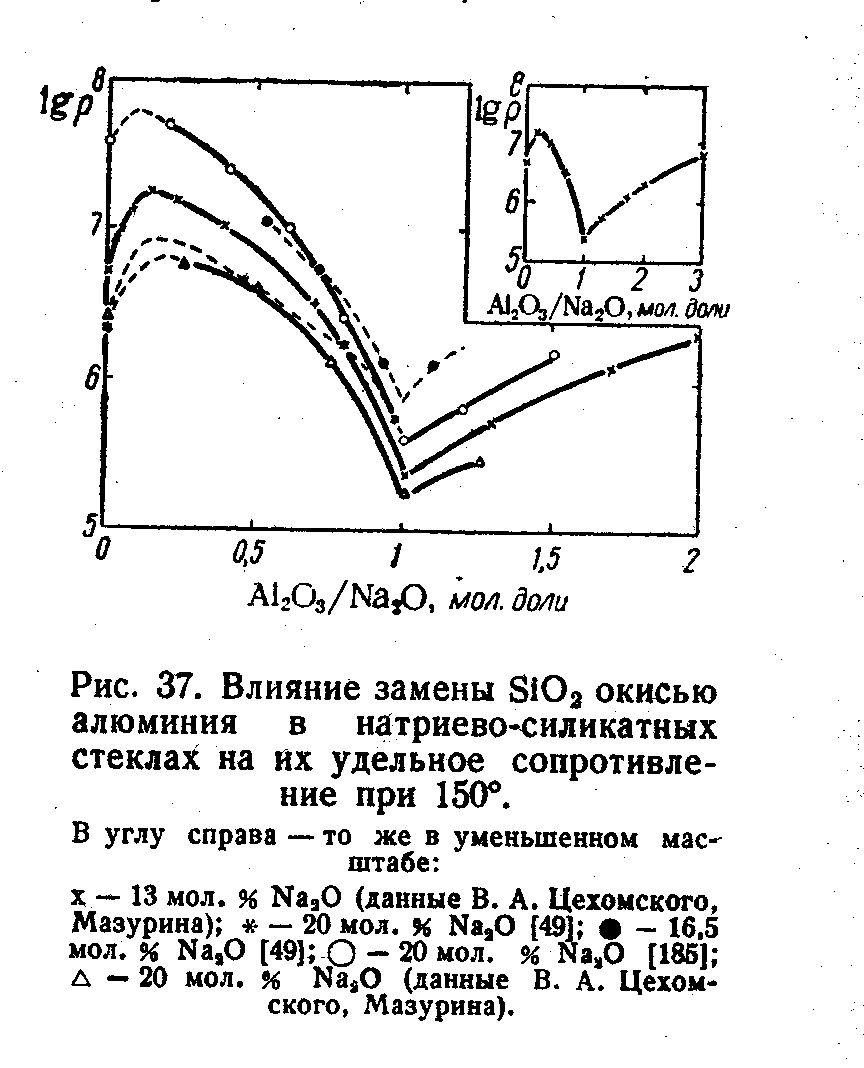
Рис. 72. Влияние замены SiO2 оксидом алюминия
в натриево-силикатных стеклах на их удельное
сопротивление при 150°С. Разные обозначения
точек соответствуют разным авторам. Из книги
О.В.Мазурин, Электрические свойства стекла,
Л. 1962.
Объяснение этому следует искать в образовании структурных групп [AlO4/2]-Na+. Ион Na+ может занимать неоднозначное положение вблизи тетраэдра AlO4/2: например, справа и слева. Такая структура приводит к большому значению диэлектрической проницаемости. А последнее имеет следствием низкую энергию активации проводимости и минимум электросопротивления. Вообще говоря, в последовательности М+[AlO4/2]-; M+[SiO3/2O]-; M+[BO4/2]- энергии активации растут по той же причине (Р.Л.Мюллер).
Проявление фазового разделения
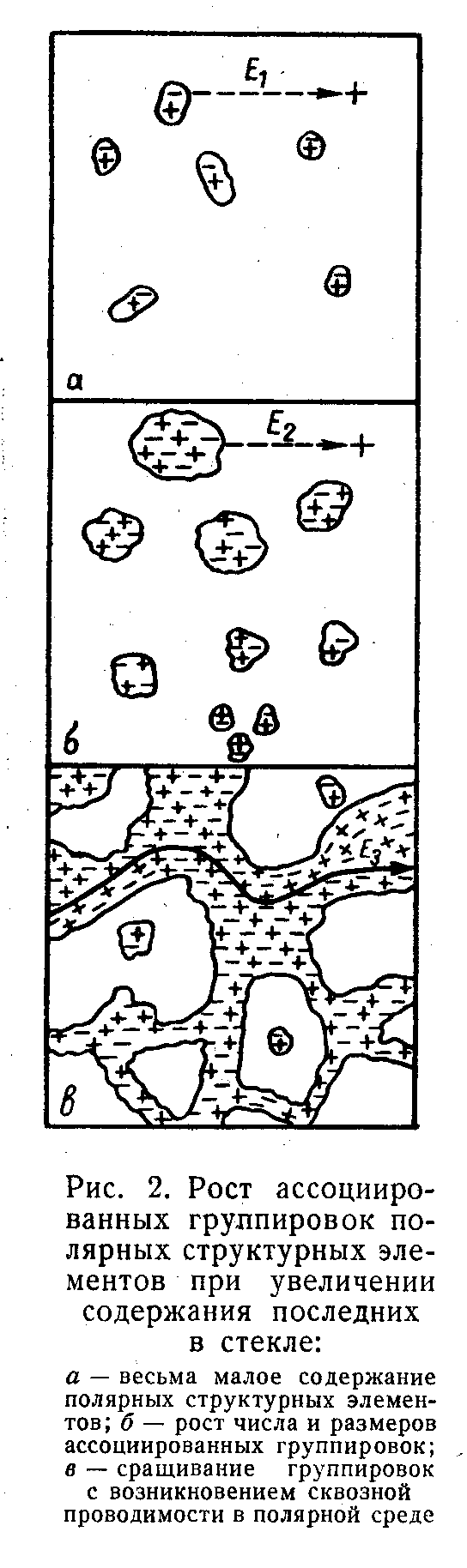
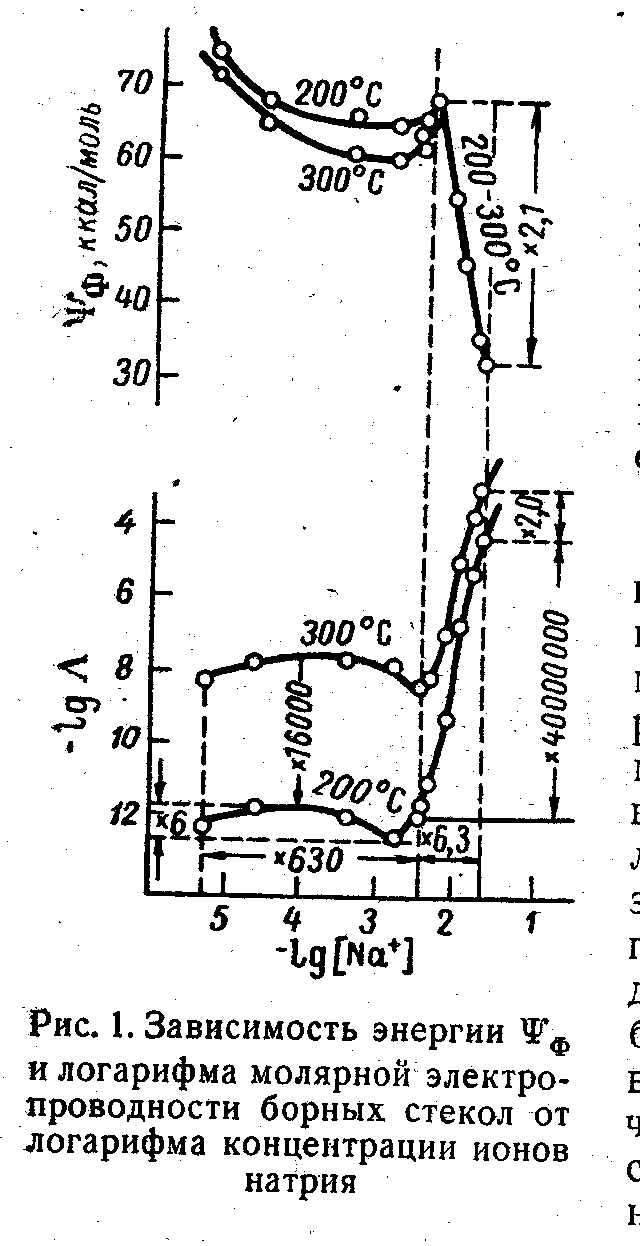
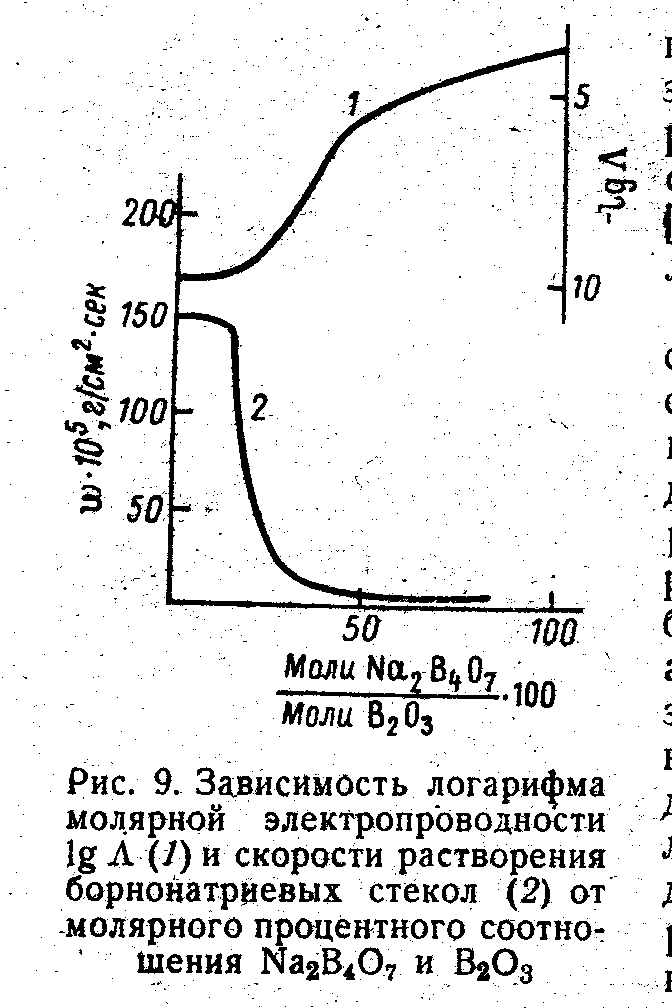
Фазовое разделение приводит к тому, что пространственное распределение «хорошо» и «плохо» проводящих фаз меняется таким образом, что при некоторых составах становится возможным протекание тока по всему образцу по одной из фаз. Вторая при этом роли как бы не играет. Подобные представления существовали еще в самом начале 20 века (теория «протекания» Г.Тамманна). При этом даже не играет особой роли существование фазовых границ. Простая пространственная ассоциация полярных и неполярных структурных единиц приводит к тому же результату (Р.Л.Мюллер, 1940, 1956). На рис. 73 показан принцип таких структурных изменений (по Мюллеру) в системе Na2O – B2O3. Как только происходит слияние полярных областей (высокая диэлектрическая проницаемость), в системе устанавливается высокая сквозная проводимость по этой матрице с низкой энергией активации (рис. 74). Тут же резко уменьшается скорость растворения стекла (рис. 75), потому что бораты растворяются медленнее борного ангидрида.
Такого же типа закономерности наблюдаются и в случае стекол с фазовым разделением (О.В.Мазурин).
|
|
|
Рис. 73. Рост ассоциированных группировок полярных структурных элементов при увеличении содержания последних в стекле. а- весьма малое содержание структурных элементов; б- рост числа и размеров ассоциированных группировок; в – сращивание группировок с возникновением сквозной проводимости в полярной среде. Из книги: Р.Л.Мюллер, Электропроводность стеклообразных веществ. Изд. ЛГУ, Л., 1968. |
|
|
|
|
|
Рис. 74 (слева). Зависимость энергии диссоциации полярных групп и молярой электропроводности натриево-боратных стекол от логарифма концентрации ионов натрия. Рис. 75 (справа). Зависимость логарифма молярной электропроводности lgΛ (1) и скорости растворения стекол (2) от молярного процентного соотношения Na2B4O7 и В2O3. Из книги: Р.Л.Мюллер, Электропроводность стеклообразных веществ. Изд. ЛГУ, Л., 1968.
|
||
Полищелочной эффект
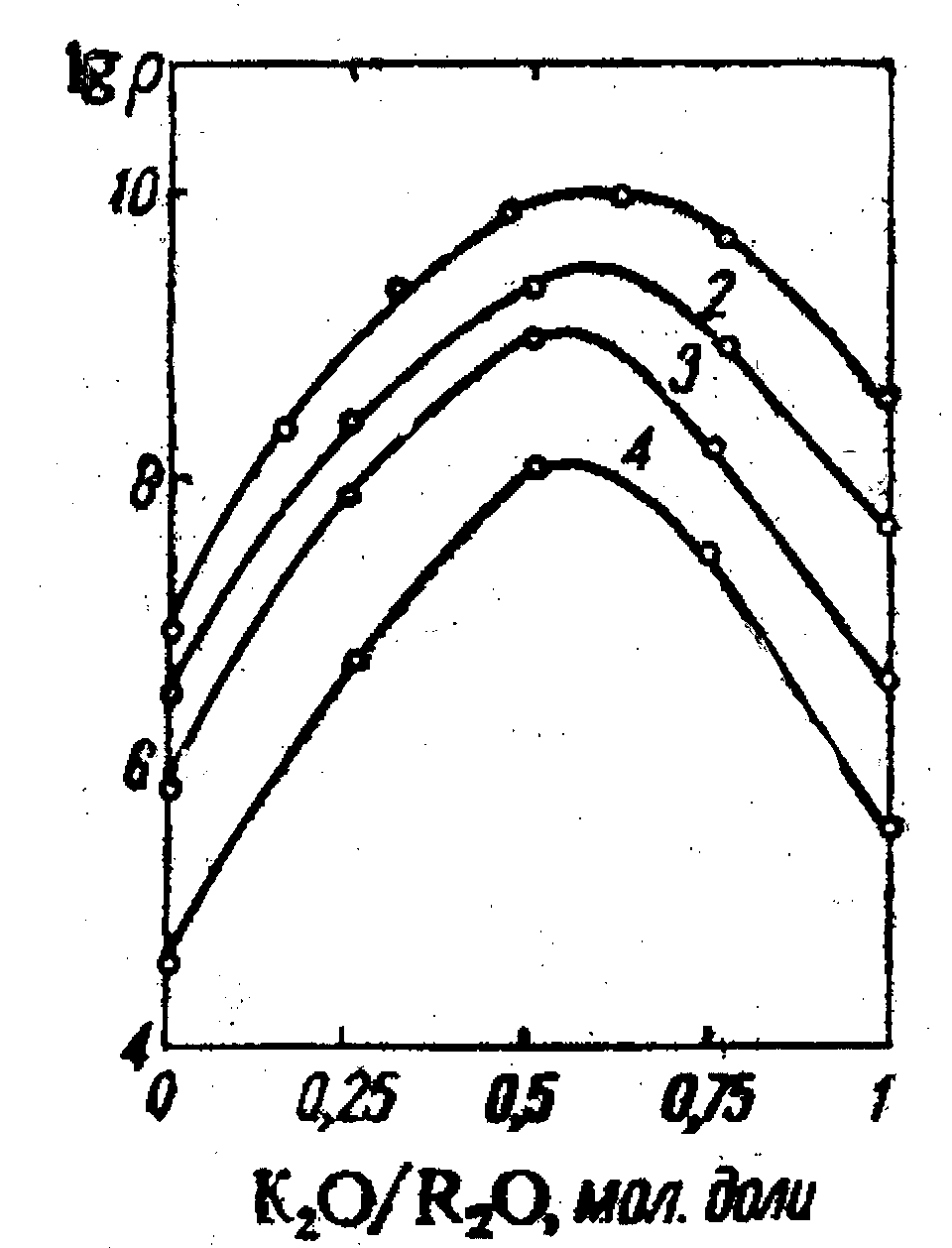
Полищелочной эффект состоит в том, что эквивалентное замещение одной щелочи на другую (или на сумму нескольких щелочей) приводит к росту энергии активации и увеличению сопротивления на несколько порядков, рис. 76. Эффект проявляется совершенно аналогичным образом и на коэффициенте диффузии.
Эффект отсутствует при малом суммарном содержании щелочи (менее ~10 мол.%). Эффект тем больше, чем больше различие в размерах взаимозамещающих катионов, в их массе. В стеклах, содержащих примесь воды (протоны ведут себя как щелочной катион) эффект тот же.
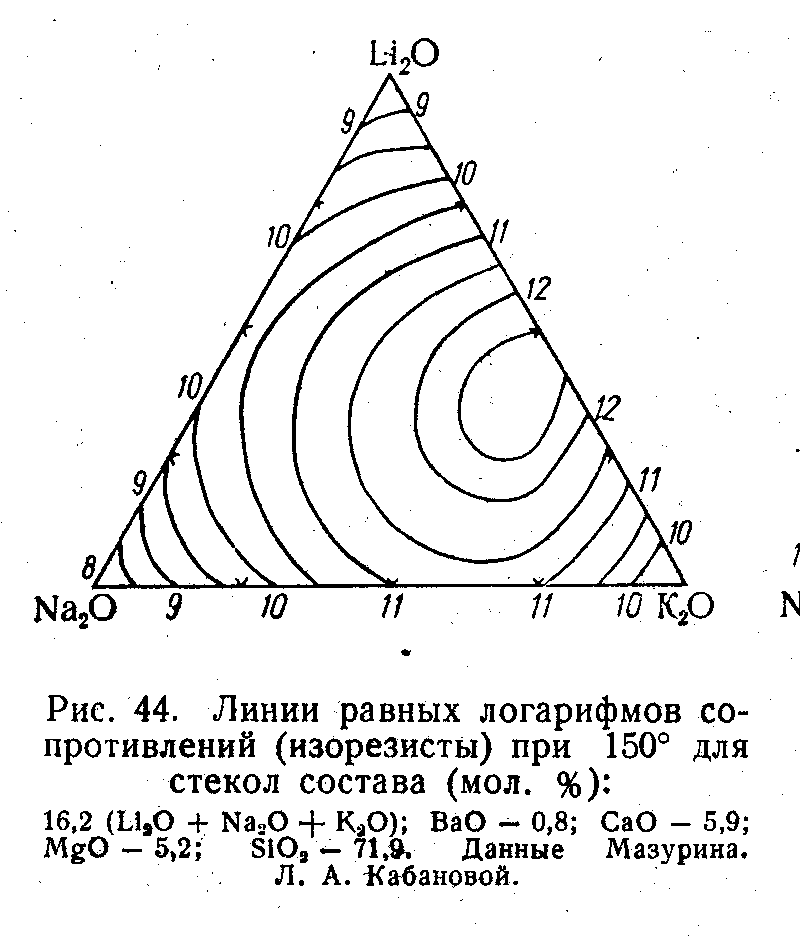
В тройных системах эффект аналогичен и проявляется в виде максимума поверхности электросопротивления (рис. 77).
Исследование чисел переноса показало, что числа переноса плавно уменьшаются для данного катиона при его замещении на другой катион. Но этого и следовало ожидать, поскольку производят замену одного носителя тока на другой. Вместе с тем анализ возможности возникновения стерических (пространственных) препятствий при замещениях показал, что стерические причины эффекта не объясняют. Мюллер полагал, что происходит ассоциация разнотипных (по типу катиона) полярных групп и образование более однородной структуры стекла в смысле разделения полярных и неполярных областей. Диссоциация в этих условиях требует значительной энтропийной составляющей (энтропия активации проводимости велика), что и является причиной повышенной экспериментальной энергии активации. Предлагались также модели электродинамической стабилизации двух сопряженных осцилляторов с
|
|
Рис. 76 (слева). Пример полищелочного эффекта в силикатных стеклах, замена натрия на калий (система Na2O-K2O-SiO2, 150°С, сумамарное содержание щелочных оксидов 1 – 13; 2 – 20; 3 – 330; 4- 40 мол. %). Рис. 77 (справа). Полищелочной эффект (линии равных удельных сопротивлений при 150°С для системы (мол.%) 16.2 R2O; 0.8 BaO; 5.9 СаО; 5.2 MgO; 71.9 SiO2 ). Цифры у кривых – lgρ. О.В.Мазурин, Электрические свойства стекла, Л. 1962 |
|
разными приведенными массами. В этой модели два соседствующих катиона с разными массами колеблются в резонанс с выигрышем энергии. Диссоциация требует дополнительной работы по разрушению этой энергетически выгодной электродинамической системы. Предлагались также модели, в которых играла роль дополнительная энергии смешения диполей с разным дипольным моментом, и другие. Однако пока ни одна модель не доказана и не позволяет количественно рассчитать этот эффект.
Полищелочной эффект исключительно важен во всех современных технологических процессах.