- •Специальные разделы оптического материаловедения
- •Термодинамика фазовых равновесий
- •1.1 Общие сведения о термодинамике
- •1 Предмет термодинамики1
- •1.1.2 Термодинамическая система, виды систем
- •Изолированные системы – те, которые не имеют возможности обмениваться веществом и энергией с окружением и имеющие постоянный объем.
- •1.1.3 Параметры состояния, параметры процессов
- •1.1.4 Функции состояния
- •1.1.5 Виды процессов
- •1.1.6 Внутренняя энергия, теплота и работа
- •1.1.7 Максимальная работа при изобарических, изотермических, адиабатических и изохорных процессах
- •1.2 Законы термодинамики
- •1.2.2 II закон термодинамики и энтропия как термодинамическая функция
- •1.2.3 Энтропия и термодинамическая вероятность. III закон термодинамики
- •Следствия Законов
- •1.2.5 Термодинамические функции, важные для материаловедения.
- •1.2.6 Применение термодинамических понятий в других областях науки
- •1.3 Производные термодинамических потенциалов и фазовые переходы
- •1.3.1 Первые производные термодинамических потенциалов, их физический
- •1.3.2 Вторые производные термодинамических потенциалов (соотношения
- •1.3.3 Фазовые переходы I и II рода.
- •1.3.4 Фазовые переходы I рода. Барическая зависимость фазовых переходов I рода:
- •1.4 Теория фазовых равновесий
- •1.4.1 Понятия «фазовые равновесия», «компонент», «диаграмма состояний»,
- •1.4.2 Понятие химического потенциала. Условия равновесия фаз. Правило фаз
- •1.4.3 Диаграмма состояний однокомпонентной системы
- •1.4.5 Эвтектики (двухкомпонентные системы). Линии ликвидуса и солидуса.
- •1.4.6 Твердые растворы (двухкомпонентные системы). Значение твердых
- •1.4.7 Ограниченные твердые растворы
- •1.4.8 Упорядочение твердых растворов
- •1.4.9 Полная несмешиваемость в жидком и в твердом состояниях
- •1.4.10 Системы с расслаиванием в жидком состоянии. Стабильное и
- •1.4.11 Системы с образованием химических соединений (двухкомпонентные
- •1.4.12 Системы с образованием химических соединений (двухкомпонентные
- •1.4.13 Трёхкомпонентные системы (принципы изображения,
- •1.4.14 Комбинация элементов диаграмм состояний. Физико-химический анализ.
- •2. Фазовые переходы и кинетическая теория стеклования
- •2.1 Стеклование
- •2.1.1 Принципиальная особенность фазовых переходов I и II рода в общей
- •2.1.2 Природа взаимодействия в конденсированных системах (общие
- •Ионное взаимодействие
- •Взаимодействие в металлах
- •Ковалентное взаимодействие
- •Водородные связи
- •Взаимодействие Ван-дер-Ваальса
- •Энергия химических связей
- •2.1.3 Основные особенности строения жидкостей и принцип их обобщенного
- •2.1.4 Общие сведения о релаксационных процессах как о процессах перехода от
- •2.1.5 Равновесные и мгновенные свойства жидкостей
- •2.1.6 Переохлажденные жидкости как частный случай метастабильного
- •2.1.7 Проявление стеклования на свойствах жидкостей
- •2.1.8 Определение стеклообразного состояния как лабильного (абсолютно
- •2.1.9 Математическое описание стеклования в кинетической теории. Твердо- и
- •2.1.10 Время релаксации структуры и его зависимость от температуры.
- •2.1.11 Соотношение температур стеклования и плавления (правило «2/3»
- •2.2 Кристаллизация расплавов стекол
- •2.2.1 Термодинамические особенности метастабильной жидкости
- •2.2.2 Работа образования зародыша кристаллизации20
- •2.2.3 Кривые Таммана а) скорость зарождения и кривая зарождения.
- •Б) скорость роста и кривая роста.
- •2.2.4 Методы изучения кристаллизационной способности и её
- •А) политермический метод и диаграммы кристаллизационной способности
- •Б) фазовый состав и морфология кристаллов.
- •В) дифференциальный термический анализ.
- •Г) скорость кристаллизации
- •2.2.5 Типы кристаллизации
- •2.2.6 Катализированная кристаллизация; ситаллы
- •2.2.7 Связь кристаллизационной способности с диаграммой состояния
- •3.Термодинамика стеклообразного состояния
- •3.1.1 Термодинамические переменные, используемые при математическом
- •3.1.2 Математическое описание избыточной свободной энергии лабильной
- •3.1.3 Математическое условие стеклования, налагаемое на изменения
- •3.1.4 Соотношение Пригожина-Дефея и его экспериментальная проверка
- •3.1.5 Термодинамический инвариант стеклообразного состояния
- •3.1.6 Следствия, вытекающие из соотношений термодинамики
- •5. Релаксационные процессы в стеклообразном состоянии. Ионная проводимость и ионный обмен
- •5.1.1 Зависимость температуры стеклования от скорости охлаждения
- •5.1.2 Процессы и законы релаксационных изменений свойств, структурная
- •5.1.3 Оценка времени достижения равновесного состояния в процессе отжига
- •5.1.4 Физическое старение стекла при комнатной температуре52
- •5.1.5 Релаксационные явления при переходе через температуру стеклования
- •5.1.6 «Кроссовер эффект»
- •5.1.7 Расчёт изменения свойств при отжиге стекол на основании
- •5.2 Природа ионной проводимости и диффузии в стеклах.
- •5.2.1 Структура стекла и основы механизма
- •5.2.2 Законы диффузии и соотношение Нернста – Эйнштейна
- •5.2.3 Основное статистическое уравнение проводимости. Энергия активации.
- •5.2.4 Общие корреляции, ряд подвижностей
- •5.2.5 Основные закономерности электропроводности, определяемые составом
- •5.2.6 Ионообменные процессы и проблемы современной оптической технологии
- •5.2.7 Ионообменные процессы с растворами. Стеклянный электрод.
- •6. Взаимосвязь между основными видами релаксационных процессов в стеклах
- •6.4.1 Соотношение Максвелла для проводимости диэлектриков
- •6.4.2 Соотношение Максвелла для проводимости диэлектриков как основа связи
- •6.4.3 Экспериментальная проверка возможности расчёта температуры «ионного» максимума внутреннего трения по данным проводимости
- •7. Основные принципы химической устойчивости стекол
- •7.1.1 Практическая значимость свойства и его физико-химическое
- •7.1.2 Методы испытания и классификация стекол по группам
- •Группы химической устойчивости бесцветного оптического стекла к действию кислоты и дистиллированной воды
- •Группы химической устойчивости бесцветного оптического стекла к действию влажной атмосферы
- •7.1.3 Влияние компонентов состава стекла на химическую устойчивость
- •7.1.4 Способы защиты оптических деталей от химического разрушения
- •8. Специфика некоторых структурных явлений в регистрирующих средах
- •8.1. Фотоструктурные изменения в халькогенидных стеклах, их существо и
- •8.2 Структурно-фазовые изменения в жидких кристаллах и физико-химическая
- •8.2.1 Общие представления о жидких кристаллах
- •8.2.2 Специфика изменения электрических и магнитных свойств при
1.4.11 Системы с образованием химических соединений (двухкомпонентные
системы, конгруэнтное плавление)
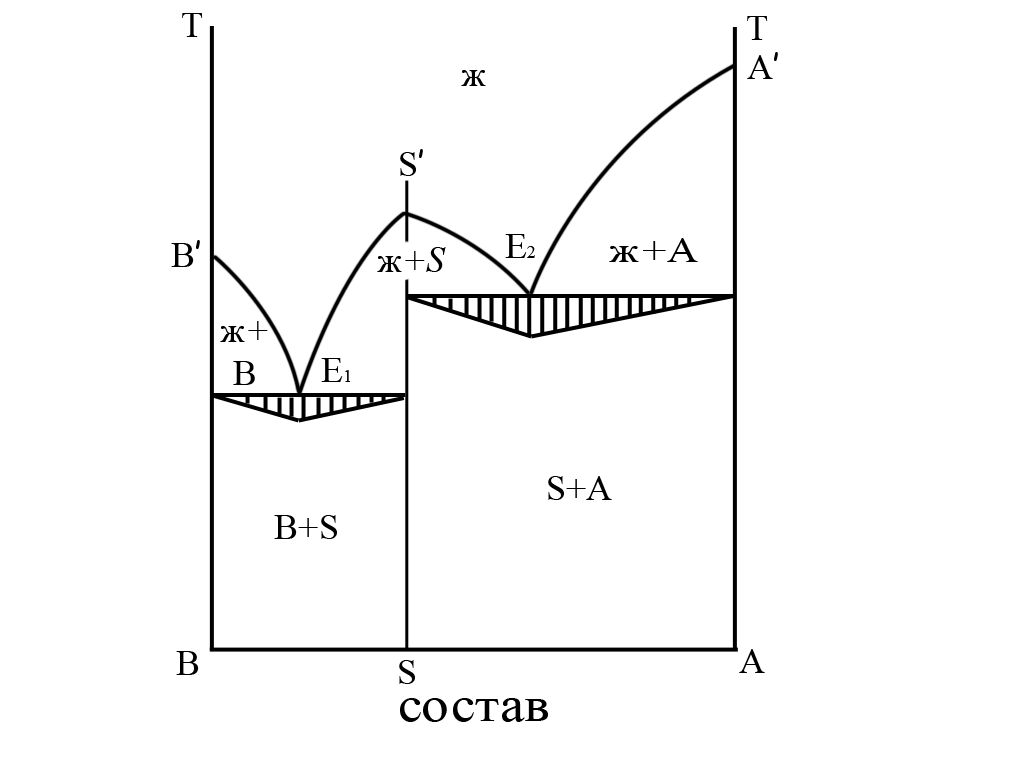
Диаграмма такого типа представлена а рис.14. Состав S отвечает составу
|
Рис. 14. Диаграмма состояния двухкомпонентной системы с образованием конгруэнтно плавящегося соединения. Пояснения в тексте. |
некоторого соединения, имеющего определенную стехиометрию (соотношение компонентов А и В 1:2; 1:1; 2:1 или какое-то другое). Состав жидкости, отвечающей этому соединению, точно соответствует составу кристаллизующейся фазы – условие конгруэнтности. Левее и правее соединения система разбивается на две простые эвтектические, в которых кристаллизуются справа В и S, слева – S и А. Степень остроты (закругленности) максимума ликвидуса в области соединения определяется его большей или меньшей склонностью к диссоциации (разложению) в жидком состоянии при повышении температуры. На рисунке заштрихованы перевернутые треугольники Таммана, соответствующие кристаллизации эвтектик Е1 и Е2.
1.4.12 Системы с образованием химических соединений (двухкомпонентные
системы, инконгруэнтное плавление)
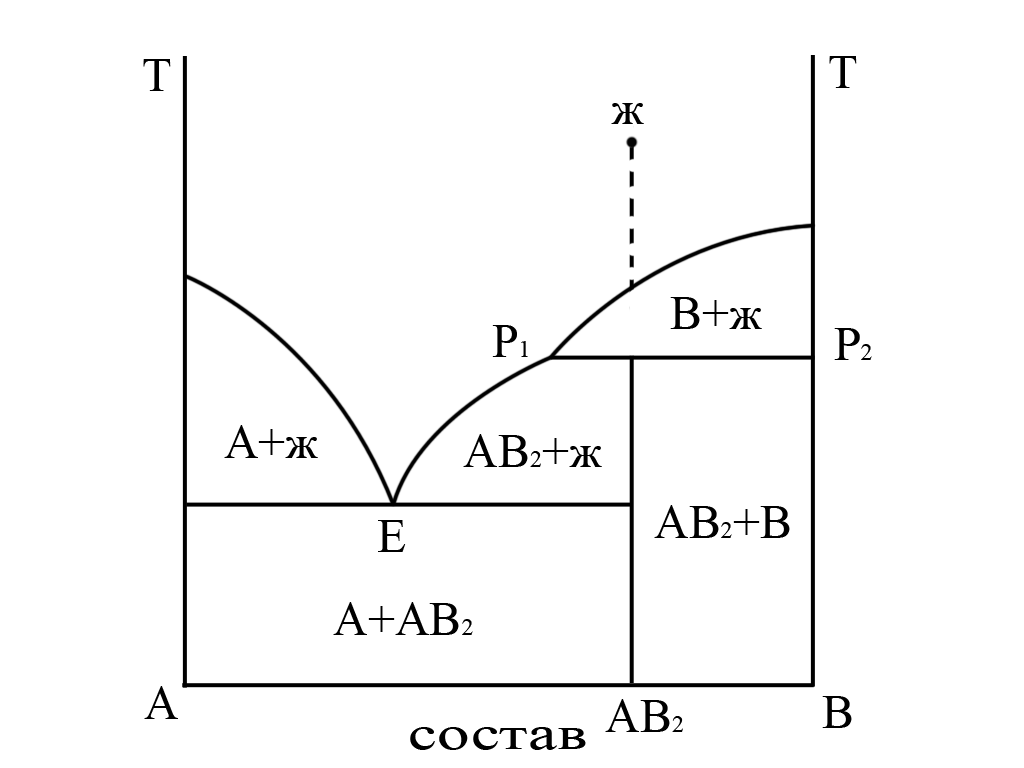
Диаграмма такого типа приведена на рис. 15. Соединение АВ2 при нагревании разлагается без плавления на жидкость, обогащенную компонентом А (состав точки р1), и твердую фазу В.
При охлаждении жидкости такого же стехиометрического состава (от точки «ж») при достижении линии ликвидуса начинают выделяться кристаллы В. По мере понижения температуры состав жидкости смещается по линии ликвидуса до точки излома р1 (как при первых стадиях эвтектической кристаллизации). При этой температуре, которая называется температурой перитектики, происходит перитектическая реакция между жидкостью и кристаллами В, то есть идёт взаимодействие между составами р1 расплава и р2 (кристаллической фазы В). В результате этого взаимодействия образуются твердые кристаллы соединения АВ2. С правой стороны от этого состава ниже температуры перитектики кристаллизуются эвтектические смеси А и АВ2, слева – смеси АВ2 и В.
|
Рис. 15. Диаграмма состояния двухкомпонентной системы с образованием инконгруэнтно плавящегося соединения. Пояснения в тексте. |
1.4.13 Трёхкомпонентные системы (принципы изображения,
концентрационный треугольник Гиббса)
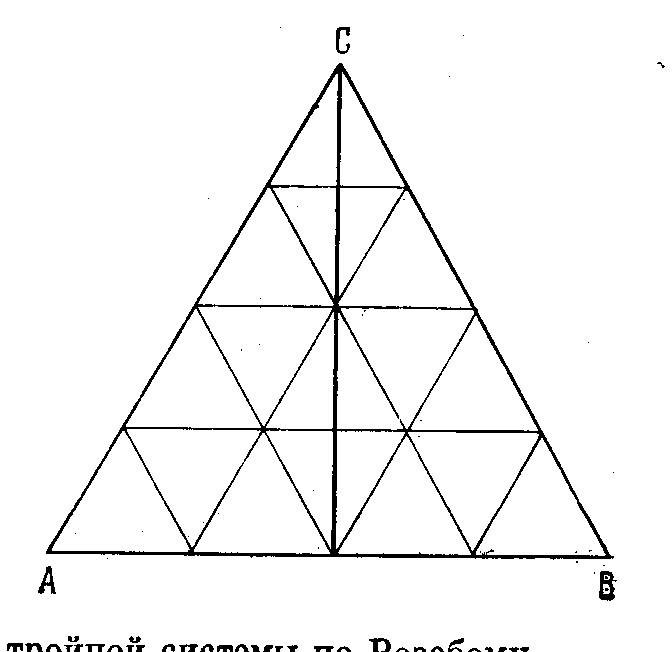
Для изображения трёхкомпонентных составов используется равносторонний треугольник, рассеченный сеткой линий, параллельных каждой из трёх сторон (треугольник Гиббса). На рис. 16 показано, что компоненты А, В, С находятся в его вершинах. Каждая сторона треугольника – это составы двухкомпонентной системы.
Линия, идущая по биссектрисе, соответствует всем составам с равным соотношением компонентов А и В.
Все составы, идущие по линии, параллельной противоположной к вершине стороне, содержат постоянную концентрацию того компонента, который стоит в вершине, против которого идёт эта сторона.
Например, на рисунке линии проведены так, что шаг в изменении состава равен 25%. Спускаясь от вершины С вниз, мы получаем первое пересечение с сеткой при составе, содержащем 75% С, 12.5% В и 12.5% А. Следующее пересечение соответствует составу с 50%С, 25%В и 25%А, и т.д. Обычно такие треугольники имеют более подробную сетку (через 5% и 1%).
|
Рис. 16. Концентрационный треугольник Гиббса. |
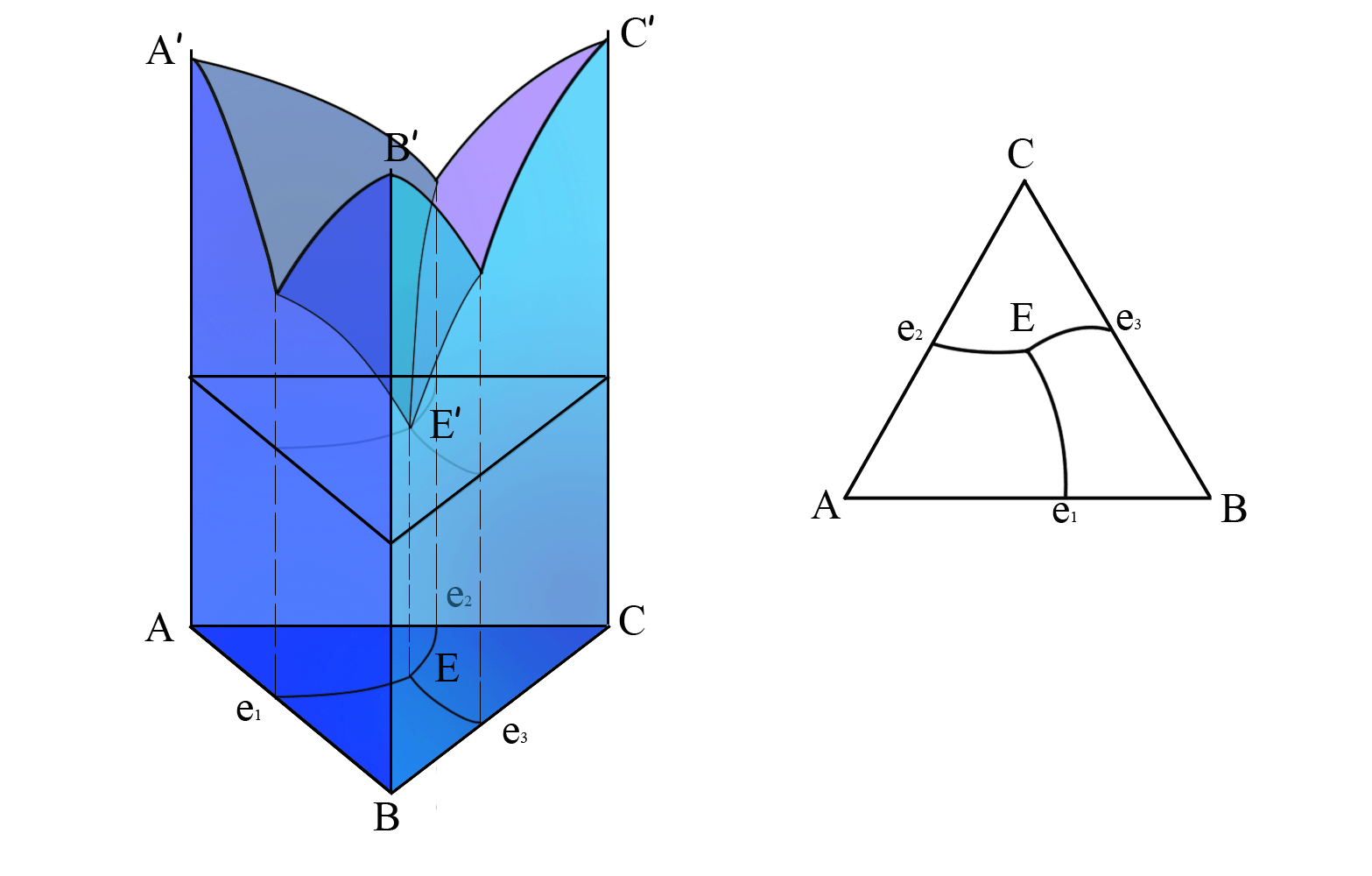
Естественно, что для трёхкомпонентных систем откладывать величину свойства (например, температуру фазового равновесия) на плоскости уже невозможно. В трехмерном пространстве получается поверхность, напоминающая географический рельеф. На рис. 17 показан случай трёхкомпонентной эвтектики12. В левой части рисунка – так, как это можно представить в пространстве. В правой части рисунка даны проекции линий эвтектической кристаллизации на плоскость треугольника. Это ложбины (или стоки) в пространственной картине, начинающиеся от составов двойных эвтектик е1, е2, е3 и сходящиеся в точку кристаллизации тройной эвтектики Е.
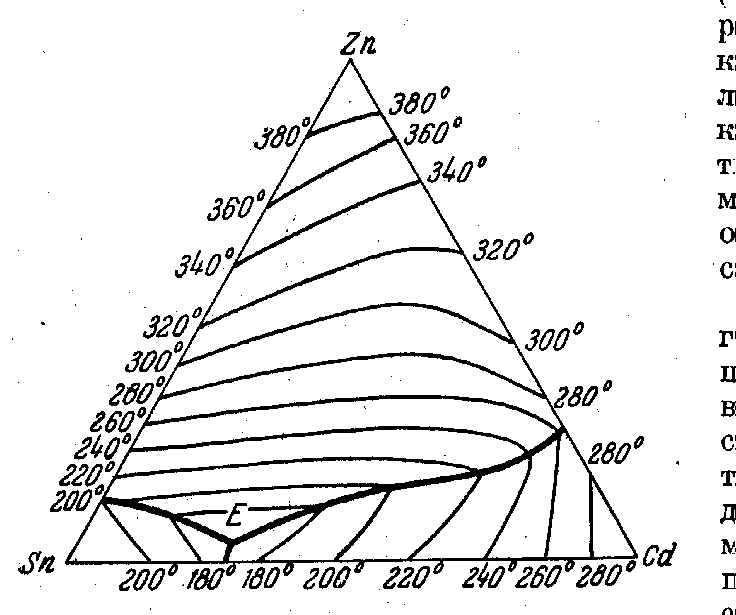
Для представления о характере поверхности строят проекции линий изотермических сечений поверхностей на площадь концентрационного треугольника. На рис. 18 показаны такие проекции для поверхностей ликвидуса системы Zn-Sn-Cd13 по данным Лоренца и Пломбриджа (1913), соответствующие секущим плоскостям постоянной температуры с шагом 20º.
В практике материаловедения стекла мы столкнемся не только с диаграммами состояния, представляемыми таким образом, но и с диаграммами состав-свойство тройных систем. Например, при определении областей стеклообразования (областей составов, которые при охлаждении их расплавов образуют стёкла) строят концентрационные треугольники и очерчивают области этих составов. С использованием такого же приема изображают поверхности температур стеклования, и т.д. По внешнему виду такие графики напоминают географическую карту, на которой горы представлены линиями изовысот.
Состав четырёхкомпонентной системы выражается координатами точки в тетраэдре. Свойства такой системы изображаются также как и свойства тройной системы, но в основании диаграммы находятся выбранные сечения тетраэдра концентраций.
|
Рис. 17. Пространственная диаграмма состояния тройной системы с простой эвтектикой. См. текст. |
|
Рис. 18. Проекции на плоскость концентрационного треугольника линий пересечения поверхности ликвидуса с плоскостями, соответствующими постоянным температурам (пример системы Zn-Sn-Cd). Е – тройная эвтектика. |