- •Специальные разделы оптического материаловедения
- •Термодинамика фазовых равновесий
- •1.1 Общие сведения о термодинамике
- •1 Предмет термодинамики1
- •1.1.2 Термодинамическая система, виды систем
- •Изолированные системы – те, которые не имеют возможности обмениваться веществом и энергией с окружением и имеющие постоянный объем.
- •1.1.3 Параметры состояния, параметры процессов
- •1.1.4 Функции состояния
- •1.1.5 Виды процессов
- •1.1.6 Внутренняя энергия, теплота и работа
- •1.1.7 Максимальная работа при изобарических, изотермических, адиабатических и изохорных процессах
- •1.2 Законы термодинамики
- •1.2.2 II закон термодинамики и энтропия как термодинамическая функция
- •1.2.3 Энтропия и термодинамическая вероятность. III закон термодинамики
- •Следствия Законов
- •1.2.5 Термодинамические функции, важные для материаловедения.
- •1.2.6 Применение термодинамических понятий в других областях науки
- •1.3 Производные термодинамических потенциалов и фазовые переходы
- •1.3.1 Первые производные термодинамических потенциалов, их физический
- •1.3.2 Вторые производные термодинамических потенциалов (соотношения
- •1.3.3 Фазовые переходы I и II рода.
- •1.3.4 Фазовые переходы I рода. Барическая зависимость фазовых переходов I рода:
- •1.4 Теория фазовых равновесий
- •1.4.1 Понятия «фазовые равновесия», «компонент», «диаграмма состояний»,
- •1.4.2 Понятие химического потенциала. Условия равновесия фаз. Правило фаз
- •1.4.3 Диаграмма состояний однокомпонентной системы
- •1.4.5 Эвтектики (двухкомпонентные системы). Линии ликвидуса и солидуса.
- •1.4.6 Твердые растворы (двухкомпонентные системы). Значение твердых
- •1.4.7 Ограниченные твердые растворы
- •1.4.8 Упорядочение твердых растворов
- •1.4.9 Полная несмешиваемость в жидком и в твердом состояниях
- •1.4.10 Системы с расслаиванием в жидком состоянии. Стабильное и
- •1.4.11 Системы с образованием химических соединений (двухкомпонентные
- •1.4.12 Системы с образованием химических соединений (двухкомпонентные
- •1.4.13 Трёхкомпонентные системы (принципы изображения,
- •1.4.14 Комбинация элементов диаграмм состояний. Физико-химический анализ.
- •2. Фазовые переходы и кинетическая теория стеклования
- •2.1 Стеклование
- •2.1.1 Принципиальная особенность фазовых переходов I и II рода в общей
- •2.1.2 Природа взаимодействия в конденсированных системах (общие
- •Ионное взаимодействие
- •Взаимодействие в металлах
- •Ковалентное взаимодействие
- •Водородные связи
- •Взаимодействие Ван-дер-Ваальса
- •Энергия химических связей
- •2.1.3 Основные особенности строения жидкостей и принцип их обобщенного
- •2.1.4 Общие сведения о релаксационных процессах как о процессах перехода от
- •2.1.5 Равновесные и мгновенные свойства жидкостей
- •2.1.6 Переохлажденные жидкости как частный случай метастабильного
- •2.1.7 Проявление стеклования на свойствах жидкостей
- •2.1.8 Определение стеклообразного состояния как лабильного (абсолютно
- •2.1.9 Математическое описание стеклования в кинетической теории. Твердо- и
- •2.1.10 Время релаксации структуры и его зависимость от температуры.
- •2.1.11 Соотношение температур стеклования и плавления (правило «2/3»
- •2.2 Кристаллизация расплавов стекол
- •2.2.1 Термодинамические особенности метастабильной жидкости
- •2.2.2 Работа образования зародыша кристаллизации20
- •2.2.3 Кривые Таммана а) скорость зарождения и кривая зарождения.
- •Б) скорость роста и кривая роста.
- •2.2.4 Методы изучения кристаллизационной способности и её
- •А) политермический метод и диаграммы кристаллизационной способности
- •Б) фазовый состав и морфология кристаллов.
- •В) дифференциальный термический анализ.
- •Г) скорость кристаллизации
- •2.2.5 Типы кристаллизации
- •2.2.6 Катализированная кристаллизация; ситаллы
- •2.2.7 Связь кристаллизационной способности с диаграммой состояния
- •3.Термодинамика стеклообразного состояния
- •3.1.1 Термодинамические переменные, используемые при математическом
- •3.1.2 Математическое описание избыточной свободной энергии лабильной
- •3.1.3 Математическое условие стеклования, налагаемое на изменения
- •3.1.4 Соотношение Пригожина-Дефея и его экспериментальная проверка
- •3.1.5 Термодинамический инвариант стеклообразного состояния
- •3.1.6 Следствия, вытекающие из соотношений термодинамики
- •5. Релаксационные процессы в стеклообразном состоянии. Ионная проводимость и ионный обмен
- •5.1.1 Зависимость температуры стеклования от скорости охлаждения
- •5.1.2 Процессы и законы релаксационных изменений свойств, структурная
- •5.1.3 Оценка времени достижения равновесного состояния в процессе отжига
- •5.1.4 Физическое старение стекла при комнатной температуре52
- •5.1.5 Релаксационные явления при переходе через температуру стеклования
- •5.1.6 «Кроссовер эффект»
- •5.1.7 Расчёт изменения свойств при отжиге стекол на основании
- •5.2 Природа ионной проводимости и диффузии в стеклах.
- •5.2.1 Структура стекла и основы механизма
- •5.2.2 Законы диффузии и соотношение Нернста – Эйнштейна
- •5.2.3 Основное статистическое уравнение проводимости. Энергия активации.
- •5.2.4 Общие корреляции, ряд подвижностей
- •5.2.5 Основные закономерности электропроводности, определяемые составом
- •5.2.6 Ионообменные процессы и проблемы современной оптической технологии
- •5.2.7 Ионообменные процессы с растворами. Стеклянный электрод.
- •6. Взаимосвязь между основными видами релаксационных процессов в стеклах
- •6.4.1 Соотношение Максвелла для проводимости диэлектриков
- •6.4.2 Соотношение Максвелла для проводимости диэлектриков как основа связи
- •6.4.3 Экспериментальная проверка возможности расчёта температуры «ионного» максимума внутреннего трения по данным проводимости
- •7. Основные принципы химической устойчивости стекол
- •7.1.1 Практическая значимость свойства и его физико-химическое
- •7.1.2 Методы испытания и классификация стекол по группам
- •Группы химической устойчивости бесцветного оптического стекла к действию кислоты и дистиллированной воды
- •Группы химической устойчивости бесцветного оптического стекла к действию влажной атмосферы
- •7.1.3 Влияние компонентов состава стекла на химическую устойчивость
- •7.1.4 Способы защиты оптических деталей от химического разрушения
- •8. Специфика некоторых структурных явлений в регистрирующих средах
- •8.1. Фотоструктурные изменения в халькогенидных стеклах, их существо и
- •8.2 Структурно-фазовые изменения в жидких кристаллах и физико-химическая
- •8.2.1 Общие представления о жидких кристаллах
- •8.2.2 Специфика изменения электрических и магнитных свойств при
5.1.4 Физическое старение стекла при комнатной температуре52
Стекло – система в лабильном (абсолютно неустойчивом) состоянии. Поэтому и при комнатной температуре объем стекла также спонтанно релаксирует. Этот случай соответствует изотермическому процессу релаксации. Амплитуда изменений свойств в этом процессе составляет доли процентов от тех изменений, которые происходят при высокой температуре, при отжиге недалеко от Tg.
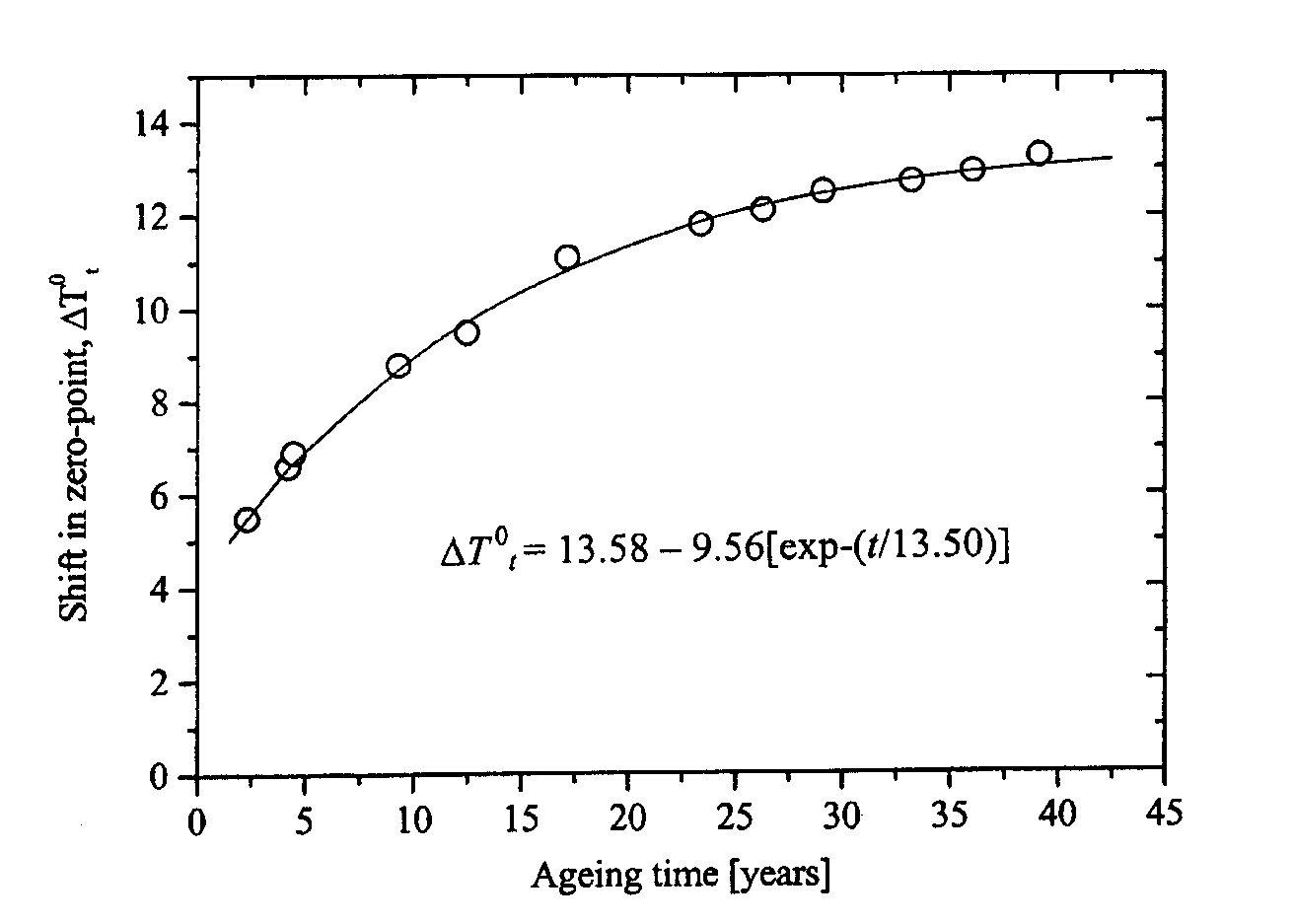
Первым кто описал такой процесс по наблюдениям смещения нуля термометра, был Джоуль. В течение около 40 лет он записывал положение нуля термометра, в котором шарик был сделан из стекла. При усадке объема размер шарика уменьшается и термометр показывает для температуры таяния льда (всегда 0ºС) завышенные значения. Рис. 58 иллюстрирует его наблюдения.
В отличие от релаксации в области высоких температур (где происходит обычный отжиг), здесь процесс всегда описывается простым экспоненциальным законом, но времена релаксации, которые реально определяют скорость этого процесса, очень велики (недели, месяцы, года, десятки лет). Данные Джоуля описываются законом простой экспоненты при времени релаксации 13.5 лет.
|
Рис. 58. Изменение со временем эксплуатации положения нулевой точки термометра (в град. Фаренгейта). Данные Джоуля (J.P. Joule, The Scientific Papers V. 1. London, 1884, p. 558) |
Анализ весьма скудных экспериментальных данных по старению шкал термометров, стекол специального назначения (для линий задержки в телевизионных системах и других) показал, что все эти данные оптимально могут быть представлены как линейная функция температуры при вязкости 1013.5 П (то есть свободной энергии активации)
lgτi = γi×T13.5 + b.
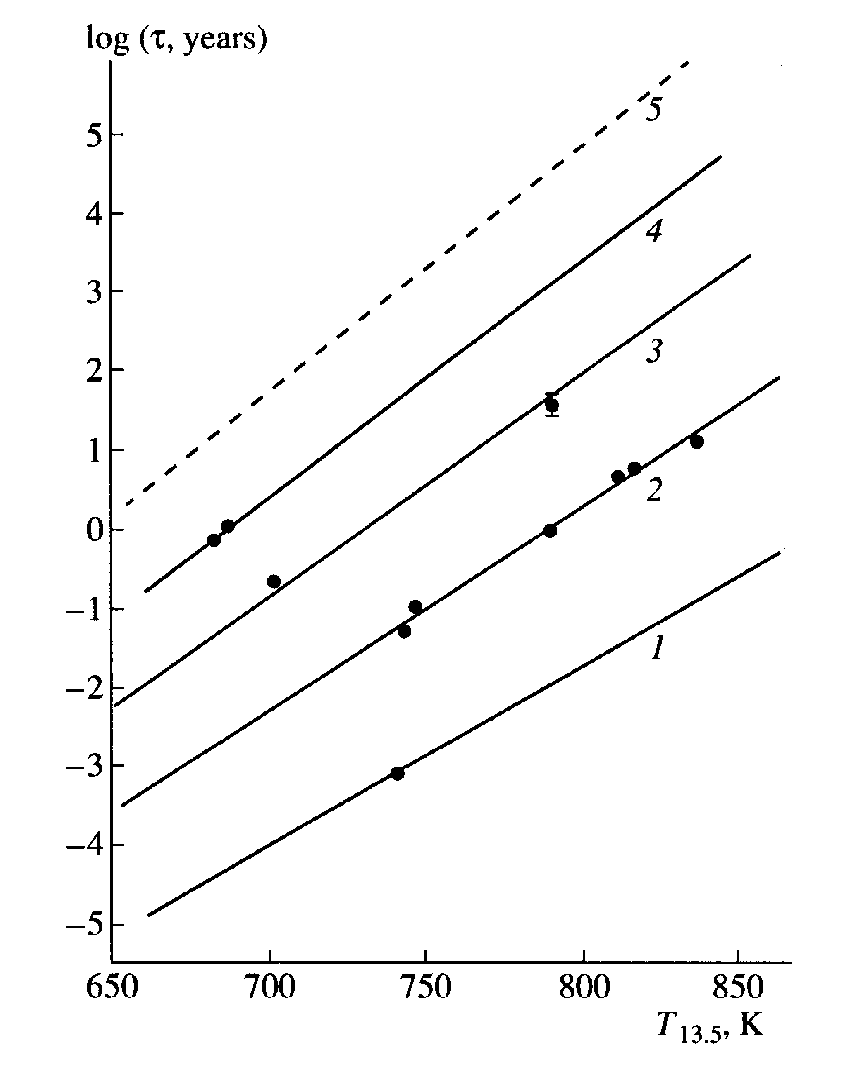
Оказывается, что в одном и том же стекле при комнатной температуре одновременно могут протекать несколько процессов с очень сильно отличающимися временами релаксации τi. Времена релаксации рассчитывается исходя из фиктивной температурой стекла Т13.5, определяемой как соответствующую вязкости 1013.5П, следующим соотношением (рис. 59):
logτ1 = 0.0234∙T13.5 – 20.400
logτ2 = 0.0260·T13.5 – 20.414
log3 = 0.0280·T13.5 – 20.400
log4 = 0.0298·T13.5 – 20.400
Значение свободного члена близко к 20.4. В аппарате теории оно соответствует значению времени релаксации τ0 в уравнении
τ = τ0exp(∆G≠/RT),
которое
точно совпадает со значением 10-13
с, ожидаемым по классическим представлениям
как обратная частота термических
колебаний. Очевидно, что существует
несколько каналов релаксации (здесь их
4). Они отличаются только свободными
энергиями активации (∆G![]() ),
которые составляют некоторую часть
потенциального барьера структурной
релаксации при стекловании; последний
соответствовал фиктивной температуре
при вязкости 1013.5П. Именно такой
фиктивной температуре примерно
соответствовал режим предварительного
отжига стекол, использовавшихся для
термометрических и др. целей и данные
по старению которых были использованы
для построения графика рис. 59. Таким
образом, для расчёта изменений показателя
при старении необходимо знать Т13.5
и амплитуду прироста показателя для
каждого канала старения.
),
которые составляют некоторую часть
потенциального барьера структурной
релаксации при стекловании; последний
соответствовал фиктивной температуре
при вязкости 1013.5П. Именно такой
фиктивной температуре примерно
соответствовал режим предварительного
отжига стекол, использовавшихся для
термометрических и др. целей и данные
по старению которых были использованы
для построения графика рис. 59. Таким
образом, для расчёта изменений показателя
при старении необходимо знать Т13.5
и амплитуду прироста показателя для
каждого канала старения.
Расчет прироста показателя преломления к возрасту стекла t должен осуществляться по формуле
∆n
=
![]() ∆ni
mаx∙(1
– e-t/τ
∆ni
mаx∙(1
– e-t/τ![]() ),
в которую входит максимальный
прирост показателя ∆ni
mаx,
приходящийся на кинетический «канал»
процесса старения. Нахождение величин
∆ni
mаx
оказывается нетрудным в силу
следующих обстоятельств:
),
в которую входит максимальный
прирост показателя ∆ni
mаx,
приходящийся на кинетический «канал»
процесса старения. Нахождение величин
∆ni
mаx
оказывается нетрудным в силу
следующих обстоятельств:
из-за различия времен релаксации соседних каналов более чем на 1.5 порядка реально старение каждого стекла определено только одним каналом релаксации.
прирост показателя можно выразить через прирост объема стекла, воспользовавшись свойством молекулярной рефракции сохранять своё значение независимо от объема,
амплитуда полного изменения объема 1 см3 стекла при релаксации, приходящаяся на один канал старения, экспериментально не зависит от состава стекла и составляет ∆V = 3(Δl/l) = −(6.0±0.9)10-5. Здесь Δl/l - величина относительной усадки шкал, изготовленных из стекла.
Если исходить из соотношения Гледстона-Дейла для рефракции R (R=(n−1)V) и продифференцировать это соотношение при постоянном R, то амплитуду прироста показателя для каждого стекла можно рассчитать на основании соотношения
∆n
= 6∙10-5(nе-1)(1
–![]() ).
).
Численный сомножитель учитывает прирост объема, а произведение 6∙10-5(nе-1) соответствует приросту показателя для одного канала старения. Для каждого стекла это значение индивидуально, так как значение показателя nе для спектральной линии в середине видимого спектра для каждого стекла индивидуально и берётся из таблиц.
В результате стало возможным производить расчёт изменения показателя преломления любого стекла за временной промежуток до 50 лет, начиная с даты его производства, с точностью не хуже ±4×10−6 единиц показателя преломления. Последнее следует из сопоставления расчёта с экспериментом и из анализа величин загрублений, сделанных в теории. Расчёт учитывает и качество предварительного отжига оптического стекла.
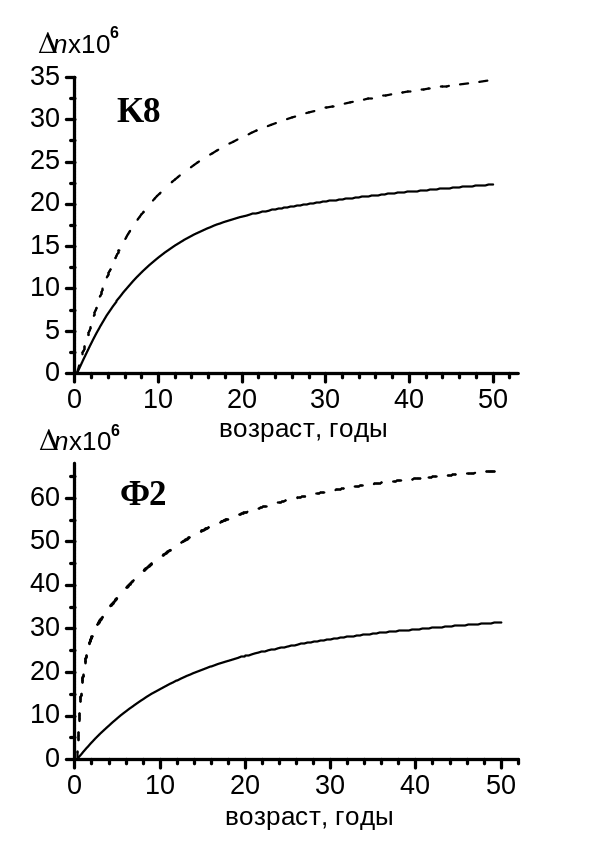
Анализ результатов показывает, что наиболее устойчивы к старению стёкла, не содержащие щелочей и имеющие высокие температуры стеклования (ОК, СТК, ТБФ и подобные им). Cтекла с низкими температурами стеклования старятся быстрее (рис. 60).
Таким образом, моделирование процесса старения при комнатной температуре приводит к выводу, что наиболее вероятно существование нескольких независимых каналов старения, потенциальные барьеры активации этих каналов составляют доли наибольшего потенциального барьера, который соответствовал замораживанию структуры стекла ещё в процессе его получения. Объяснение этому можно искать на основании соотношения между ∆G , мгновенным модулем сдвига F∞ и объемом частиц, преодолевающих барьер. Модуль сдвига – характеристика всего образца. Он определяет реакцию среды на перемещение частицы.
|
Рис. 59. Зависимость времени релаксации в процессе старения различных стекол в зависимости от величины фиктивной температуры, соответствующей вязкости 1013.5 П. |
|
Рис. 60. Рассчитанное изменение показателя преломления в процессе старения крона К8 (T13.5 =820 К) и флинта Ф2 (T13.5 =719.7 K). Пунктирные линии соответствует грубо отожженному, сплошные – тонко отожженному стеклу.
|
При вязком течении объем соответствует мостиковому атому. Меньшие значения объема (и меньшие свободные энергии активации) могут говорить только о том, что перемещения атомов происходят на очень небольшие расстояния. Было высказано предположение , что при старении происходит небольшое перемещение атомов в более равновесные положения без изменения топологии структуры. Примечательно, что частоты релаксации, соответствующие различным каналам старения, полностью вписываются в контур релаксационных механических потерь стекла, которые относят к активированным смещениям немостиковых атомов кислорода (S.V.Nemilov Glass Sci. and Technol. v.78, No 6, p. 269, 2005). Об этом будет идти речь позже.