- •Специальные разделы оптического материаловедения
- •Термодинамика фазовых равновесий
- •1.1 Общие сведения о термодинамике
- •1 Предмет термодинамики1
- •1.1.2 Термодинамическая система, виды систем
- •Изолированные системы – те, которые не имеют возможности обмениваться веществом и энергией с окружением и имеющие постоянный объем.
- •1.1.3 Параметры состояния, параметры процессов
- •1.1.4 Функции состояния
- •1.1.5 Виды процессов
- •1.1.6 Внутренняя энергия, теплота и работа
- •1.1.7 Максимальная работа при изобарических, изотермических, адиабатических и изохорных процессах
- •1.2 Законы термодинамики
- •1.2.2 II закон термодинамики и энтропия как термодинамическая функция
- •1.2.3 Энтропия и термодинамическая вероятность. III закон термодинамики
- •Следствия Законов
- •1.2.5 Термодинамические функции, важные для материаловедения.
- •1.2.6 Применение термодинамических понятий в других областях науки
- •1.3 Производные термодинамических потенциалов и фазовые переходы
- •1.3.1 Первые производные термодинамических потенциалов, их физический
- •1.3.2 Вторые производные термодинамических потенциалов (соотношения
- •1.3.3 Фазовые переходы I и II рода.
- •1.3.4 Фазовые переходы I рода. Барическая зависимость фазовых переходов I рода:
- •1.4 Теория фазовых равновесий
- •1.4.1 Понятия «фазовые равновесия», «компонент», «диаграмма состояний»,
- •1.4.2 Понятие химического потенциала. Условия равновесия фаз. Правило фаз
- •1.4.3 Диаграмма состояний однокомпонентной системы
- •1.4.5 Эвтектики (двухкомпонентные системы). Линии ликвидуса и солидуса.
- •1.4.6 Твердые растворы (двухкомпонентные системы). Значение твердых
- •1.4.7 Ограниченные твердые растворы
- •1.4.8 Упорядочение твердых растворов
- •1.4.9 Полная несмешиваемость в жидком и в твердом состояниях
- •1.4.10 Системы с расслаиванием в жидком состоянии. Стабильное и
- •1.4.11 Системы с образованием химических соединений (двухкомпонентные
- •1.4.12 Системы с образованием химических соединений (двухкомпонентные
- •1.4.13 Трёхкомпонентные системы (принципы изображения,
- •1.4.14 Комбинация элементов диаграмм состояний. Физико-химический анализ.
- •2. Фазовые переходы и кинетическая теория стеклования
- •2.1 Стеклование
- •2.1.1 Принципиальная особенность фазовых переходов I и II рода в общей
- •2.1.2 Природа взаимодействия в конденсированных системах (общие
- •Ионное взаимодействие
- •Взаимодействие в металлах
- •Ковалентное взаимодействие
- •Водородные связи
- •Взаимодействие Ван-дер-Ваальса
- •Энергия химических связей
- •2.1.3 Основные особенности строения жидкостей и принцип их обобщенного
- •2.1.4 Общие сведения о релаксационных процессах как о процессах перехода от
- •2.1.5 Равновесные и мгновенные свойства жидкостей
- •2.1.6 Переохлажденные жидкости как частный случай метастабильного
- •2.1.7 Проявление стеклования на свойствах жидкостей
- •2.1.8 Определение стеклообразного состояния как лабильного (абсолютно
- •2.1.9 Математическое описание стеклования в кинетической теории. Твердо- и
- •2.1.10 Время релаксации структуры и его зависимость от температуры.
- •2.1.11 Соотношение температур стеклования и плавления (правило «2/3»
- •2.2 Кристаллизация расплавов стекол
- •2.2.1 Термодинамические особенности метастабильной жидкости
- •2.2.2 Работа образования зародыша кристаллизации20
- •2.2.3 Кривые Таммана а) скорость зарождения и кривая зарождения.
- •Б) скорость роста и кривая роста.
- •2.2.4 Методы изучения кристаллизационной способности и её
- •А) политермический метод и диаграммы кристаллизационной способности
- •Б) фазовый состав и морфология кристаллов.
- •В) дифференциальный термический анализ.
- •Г) скорость кристаллизации
- •2.2.5 Типы кристаллизации
- •2.2.6 Катализированная кристаллизация; ситаллы
- •2.2.7 Связь кристаллизационной способности с диаграммой состояния
- •3.Термодинамика стеклообразного состояния
- •3.1.1 Термодинамические переменные, используемые при математическом
- •3.1.2 Математическое описание избыточной свободной энергии лабильной
- •3.1.3 Математическое условие стеклования, налагаемое на изменения
- •3.1.4 Соотношение Пригожина-Дефея и его экспериментальная проверка
- •3.1.5 Термодинамический инвариант стеклообразного состояния
- •3.1.6 Следствия, вытекающие из соотношений термодинамики
- •5. Релаксационные процессы в стеклообразном состоянии. Ионная проводимость и ионный обмен
- •5.1.1 Зависимость температуры стеклования от скорости охлаждения
- •5.1.2 Процессы и законы релаксационных изменений свойств, структурная
- •5.1.3 Оценка времени достижения равновесного состояния в процессе отжига
- •5.1.4 Физическое старение стекла при комнатной температуре52
- •5.1.5 Релаксационные явления при переходе через температуру стеклования
- •5.1.6 «Кроссовер эффект»
- •5.1.7 Расчёт изменения свойств при отжиге стекол на основании
- •5.2 Природа ионной проводимости и диффузии в стеклах.
- •5.2.1 Структура стекла и основы механизма
- •5.2.2 Законы диффузии и соотношение Нернста – Эйнштейна
- •5.2.3 Основное статистическое уравнение проводимости. Энергия активации.
- •5.2.4 Общие корреляции, ряд подвижностей
- •5.2.5 Основные закономерности электропроводности, определяемые составом
- •5.2.6 Ионообменные процессы и проблемы современной оптической технологии
- •5.2.7 Ионообменные процессы с растворами. Стеклянный электрод.
- •6. Взаимосвязь между основными видами релаксационных процессов в стеклах
- •6.4.1 Соотношение Максвелла для проводимости диэлектриков
- •6.4.2 Соотношение Максвелла для проводимости диэлектриков как основа связи
- •6.4.3 Экспериментальная проверка возможности расчёта температуры «ионного» максимума внутреннего трения по данным проводимости
- •7. Основные принципы химической устойчивости стекол
- •7.1.1 Практическая значимость свойства и его физико-химическое
- •7.1.2 Методы испытания и классификация стекол по группам
- •Группы химической устойчивости бесцветного оптического стекла к действию кислоты и дистиллированной воды
- •Группы химической устойчивости бесцветного оптического стекла к действию влажной атмосферы
- •7.1.3 Влияние компонентов состава стекла на химическую устойчивость
- •7.1.4 Способы защиты оптических деталей от химического разрушения
- •8. Специфика некоторых структурных явлений в регистрирующих средах
- •8.1. Фотоструктурные изменения в халькогенидных стеклах, их существо и
- •8.2 Структурно-фазовые изменения в жидких кристаллах и физико-химическая
- •8.2.1 Общие представления о жидких кристаллах
- •8.2.2 Специфика изменения электрических и магнитных свойств при
5.2.2 Законы диффузии и соотношение Нернста – Эйнштейна
I закон Фика
I закон Фика определяет вообще линейную связь потока и градиента концентрации.
Пусть Q – количество
диффундирующего вещества за единицу
времени через единицу площади,
перпендикулярной градиенту концентрации,
а
![]()
![]() -
градиент концентрации в направлении
х. Тогда
-
градиент концентрации в направлении
х. Тогда
Q = –D∙ .
Тем самым определяется коэффициент диффузии D, который имеет размерность [L2t-1]. Градиент концентрации является как бы «движущей силой» процесса диффузии.
II закон Фика
II закон Фика описывает поток, когда концентрация в точке меняется во времени.
Если
![]() = -
= -
![]() ,
,
то скорость изменения концентрации связана с коэффициентом диффузии соотношением
= D∙![]() .
.
Это соотношение описывает процесс накопления вещества в объеме, поскольку концентрация определена объемным содержанием диффузанта.
Для экспериментального нахождения D проводят диффузию в плоский образец из расплава соли. Затем делают срез образца и сканируют рентгеновским или электронным микроанализатором его поперечное сечение. Иногда просто измеряют профиль показателя преломления, что позволяет рассчитать концентрацию на основании линейной связи показателя и концентрации. Коэффициент диффузии находят из этих профилей методом Больцмана по формуле
D(c) =
![]() ∙
∙![]() ∙
∙ .
Здесь сs –
концентрация на поверхности, с –
текущая концентрация в точке x.
.
Здесь сs –
концентрация на поверхности, с –
текущая концентрация в точке x.
Для изучения самодиффузии (например, диффузии иона натрия в натриевом стекле) производится шлифовка поверхности образца и находится количество диффузанта, снятого при этом (раньше для этого широко использовали метод «меченых атомов»). Математическая обработка таких измерений стандартизирована59.
Соотношение Нернста – Эйнштейна
Обобщенная форма соотношения имеет вид:
![]()
![]() .
.
Здесь - удельная электропроводность, Т – температура, kБ – постоянная Больцмана, n – число ионов в единице объема, Z – валентность диффундирующего иона, e – заряд электрона, t - число переноса (не время!), α – коэффициент корреляции (коэффициент Хавена). Обычно для стекол α = 0.4±0.2.60 Очевидно, что измерения D весьма трудоемки. Для суждения об изменении подвижности ионов при изменении состава стекла в большинстве практических случаев достаточно знать проводимость, поскольку энергии активации проводимости и диффузии (при их однотипном механизме) совпадают.
5.2.3 Основное статистическое уравнение проводимости. Энергия активации.
Общая зависимость проводимости от концентрации носителей тока
Представим, что носитель тока (катион, способный перемещаться) появляется в результате диссоциации структурных узлов; при этом появляется вакансия, а сам катион попадает в неполярную среду, например, образованную тетраэдрами SiO4/2:
SiO3/2O–Na+ + SiO4/2 ↔ SiO3/2O– + SiO4/2 Na+
n-nd N-nd nd nd
Здесь N – общее число неполярных структурных единиц в 1 см3, n – общее число катионов в 1 см3 (недиссоциированных и диссоциированных), nd – число диссоциированных катионов в 1 см3. Концентрации n и nd связаны законом химического равновесия:
ln![]() = -
= -
![]() ,
,
где ∆Ф – свободная энергия, требующаяся для диссоциации. Очевидно, что
nd
=
![]() exp(-
exp(-![]() )
)
и при n ≈ N и малом nd
nd = n∙exp(- ).
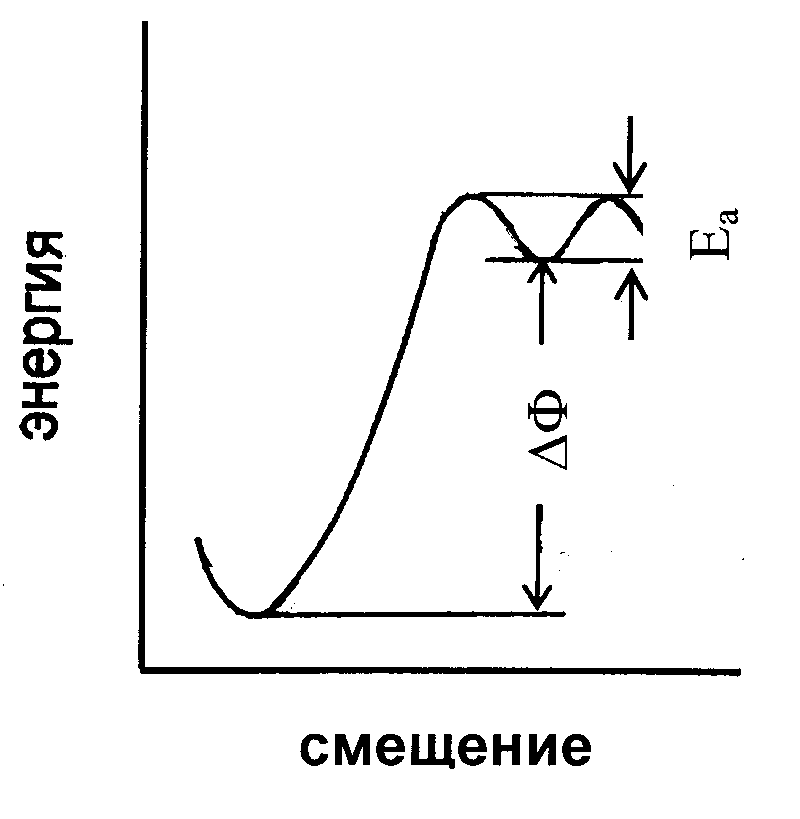
Без наложения электрического поля каждый диссоциированный катион может преодолевать сравнительно небольшие потенциальные барьеры Еа, называемые энергией активации подвижности, и перемещаться в направлении следующего междуузельного положения, оставаясь диссоциированным (рис. 68). Поскольку в декартовой системе координат имеется 6 таких возможных направлений и в каждом направлении катион может перепрыгнуть дважды при каждом термическом колебании (их частота в секунду равна ν), то общее число катионов, осуществляющих вероятные попытки покинуть своё место за секунду равно
na
= (nd/6)∙2ν∙exp(-![]() )
= (n/3)∙ν∙exp(-
)
= (n/3)∙ν∙exp(-![]() ).
).
При наличии электрического поля
напряженностью Е диссоциированные
катионы приобретают способность к
направленному смещению в направлении
поля. Это обусловлено тем, что потенциальный
барьер в направлении «против поля»
увеличивается на ∆U/NA
=
![]() E
(NA
–число
E
(NA
–число
|
Рис. 68. Схема потенциальных барьеров при ионной проводимости. |
Авогадро, NA ∙kБ = R, kБ – постоянная Больцмана, r0 – расстояние между двумя двумя междуузельными положениями). Потенциальный барьер «по полю» уменьшается на такое же значение. В итоге, записав поток переносящих ток частиц как разницу потоков «по полю» и «против поля» как
∆n =
![]() ∙ν∙exp(-
∙ν∙exp(-![]() )∙(e+∆U/RT
–e-∆U/RT),
)∙(e+∆U/RT
–e-∆U/RT),
получаем после разложения
(e+∆U/RT – e–∆U/RT)/ NA = (e∙E∙r0)/ kБT
(eα = 1 + α, если α мало), что в итоге приводит к
∆n
=
![]() ∙νeEr0∙exp(-
∙νeEr0∙exp(-![]() ).
).
Это выражение определяет общее число способных к движению ионов в присутствии напряжения.
Величина силы тока есть произведение числа носителей тока (∆n) на переносимый каждой частицей заряд (е) на расстояние единичного смещения иона за секунду (r0):
i = ∆nеr0.
Удельная электропроводность определена законом Ома: = i /E.
В результате имеем статистическое уравнение проводимости:
κ =
∙νe2r02exp(-![]() ).
).
Заметим, что в системе CGSE удельная проводимость имеет размерность
[c-1].
Это уравнение (известное как уравнение Френкеля-Йоста) представляет некоторый частный случай, определенный тем, что при выводе мы полагали некоторые частные приближения, например, n ≈ N и т.д. Тем не менее, более строгое рассмотрение приводит к аналогичному результату с точностью до сомножителя около 1.
Ионная проводимость может происходить по двум «сценариям». В первом случае освободившиеся от катионов вакантные места остаются неподвижными и их число невелико (равно числу освободившихся ионов), так что перемещение иона до попадания в ближайшую по направлению движения свободную потенциальную яму происходит по «междуузлиям», показанным на рис. 68. Это – механизм Френкеля. Во втором случае число вакантных потенциальных ям сравнительно велико, эти дефекты являются дефектами самой структуры. Ион перескакивает на очень небольшое расстояние и попадает в устойчивое положение. Это – механизм Шоттки. Поскольку в стеклах реализуется первый механизм, а формальная сторона описания обоих случаев различается несущественно, на этом вопросе мы более не останавливаемся61.
Энергия активации
Из экспериментальной зависимости электропроводности как функции обратной абсолютной температуры мы рассчитываем некоторую эффективную энергию активации, которая даже для твердых стекол имеет сложный смысл.
В полученном выражении четко разделяются два экспоненциальных сомножителя. Один, exp(– ), определяет степень диссоциации, он аналогичен степени диссоциации α в теории слабых электролитов (поэтому теорию ионной проводимости стекол относят к теории слабых электролитов). Второй экспоненциальный сомножитель, exp(–Ea/RT), определяет абсолютную скорость или фактор подвижности ω в той же теории.
В теории слабых электролитов = [M]∙F∙ω∙α, где [M] – число молей одновалентных катионов в кубическом сантиметре, F – число Фарадея, ω –подвижность, α – степень диссоциации.
Величина Ea сравнительно с ∆Ф невелика, основное влияние на электропроводность оказывает ∆Ф, задающая степень диссоциации структурных узлов на носители тока и вакансии. ∆Ф зависит от полярности среды, в которой идёт диссоциация. В неполярной среде она большая, в полярной среде – существенно меньшая.
Здесь имеется аналогия с растворами электролитов, в том числе и с водными. Расчёты ∆Ф на основании модельных структурных представлений с учётом диэлектрической постоянной были выполнены Р.Л.Мюллером (Р.Л.Мюллер, Электропроводность стеклообразных веществ, сб. трудов. Изд-во Ленинградского университета, Л., 1968.). Работы Р.Л.Мюллера признаны во всем мире как классические.
В качестве примера приведена зависимость ∆Ф для диссоциации ионов щелочных металлов при разных диэлектрических постоянных стекол.
-
катион
∆Ф,
ккал/моль
ε = 6
ε = 18
Li+
110
35
Na+
114
48
K+
139
95
Эмпирические зависимости ∆Ф от концентрации ионов щелочных металлов позволяют учесть влияние всех структурных факторов и диэлектрической постоянной на эту величину. Мюллером было найдено, что для бинарных боратных и силикатных стекол ∆Ф∙[M]1/х = L. Для боратных стекол х = 2 и L = 5.3±0.4; для силикатных х = 4 и L = 11.5±0.5.