
- •Экзаменационные вопросы по физике
- •Механика основные положения
- •Кинематика(от греческого kinematicos – движение)
- •Механическое движение
- •Относительность движения(уч.10кл.Стр.25-27)
- •Системы отсчета (уч.10кл.Стр.25-27)
- •Материальная точка (уч.10кл.Стр.24-25)
- •Траектория (уч.10кл.Стр.24-25)
- •Путь и перемещение (уч.10кл.Стр.28-30)
- •Скорость (уч.10кл.Стр.32-38)
- •Ускорение (уч.10кл.Стр.41-43)
- •Равномерное и равноускоренное прямолинейное движение (уч.10кл.Стр.38-40, 44-50)
- •Уравнение прямолинейного равноускоренного движения (уч.10кл.Стр.44-50)
- •Свободное падение тел (уч.10кл.Стр.52-55)
- •Ускорение свободного падения (уч.10кл.Стр.52-53)
- •Баллистическое движение(уч.10кл.Стр.61-68)
- •Криволинейное движение точки на примере движения по окружности с постоянной по модулю скоростью (уч.10кл.Стр.70-73)
- •Центростремительное ускорение (уч.10кл.Стр.70-73)
- •Основы динамики основные положения(уч.10кл.Стр.119-120)
- •Инерция. Преобразования галилея (уч.10кл.Стр.83- )
- •Первый закон ньютона (уч.10кл.Стр.87-88,уч.9кл.Стр.39-41)
- •Инерциальные системы отсчета (уч.10кл.Стр.83-86)
- •Принцип относительности галилея
- •Взаимодействие тел (уч.10кл.Стр.89-92)
- •Масса (уч.10кл.Стр.90-91)
- •Импульс (уч.10кл.Стр.121-126)
- •Сила (уч.10кл.Стр.90-92)
- •Второй закон ньютона (уч.10кл.Стр.89-92)
- •Принцип суперпозиции сил (уч.10кл.Стр.92)
- •Силы в природе закон всемирного тяготения (уч.10кл.Стр.96-99)
- •Сила тяготения (уч.10кл.Стр.96-99)
- •Вес тела (уч.10кл. Стр.100,105, 113-115)
- •Невесомость (уч.10кл. Стр.100-101, 113-115)
- •Первая космическая скорость (уч.10кл. Стр.161-163)
- •Сила упругости (уч.10кл. Стр.102-104, 317-320)
- •Закон гука (уч.10кл. Стр.102-105)
- •Деформация тела (уч.10кл.Стр.317-320)
- •Сила трения (уч.10кл. Стр.107-111)
- •Коэффициент трения (уч.10кл. Стр.107-111)
- •Закон трения скольжения (уч.10кл. Стр.107-111, 115-117)
- •Третий закон ньютона (уч.10кл. Стр.93-95)
- •Момент силы
- •Условия равновесия тел
- •Законы сохранения в механике основные положения (уч.10кл. Стр.158)
- •Закон сохранения импульса (уч.10кл. Стр.121-128, 153-157)
- •Ракеты (уч.10кл. Стр.128-129)
- •Механическая работа (уч.10кл. Стр.134)
- •Мощность (уч.10кл. Стр.146-148)
- •Кинетическая энергия (уч.10кл. Стр.142-145)
- •Потенциальная энергия (уч.10кл. Стр.135-142, 153)
- •Закон сохранения энергии в механике (уч.10кл. Стр.148-152, 153-157)
- •Простые механизмы (уч.7кл.Стр.136-150)
- •Коэффициент полезного действия механизма (уч.7кл.Стр.150-151)
- •Механика жидкостей и газов давление (уч.7кл.Стр.77)
- •Атмосферное давление (уч.7кл.Стр.97-103,181-182)
- •Изменение атмосферного давления с высотой (уч.7кл.Стр.106)
- •Закон паскаля для жидкостей и газов (уч.7кл.Стр.85-,176-178)
- •Барометры и манометры (уч.7кл.Стр.105, 108)
- •Сообщающиеся сосуды(уч.7кл.Стр.90)
- •Принцип устройства гидравлического пресса (уч.7кл.Стр.111-113)
- •Архимедова сила для жидкостей и газов (уч.7кл.Стр.114-125)
- •Условия плавания тел на поверхности жидкости (уч.7кл.Стр.120-125)
- •Термодинамика
- •Основы молекулярно-кинетической теории (уч.10кл.Стр.211- )
- •Опытное обоснование основных положений молекулярно-кинетической теории
- •Броуновское движение
- •Диффузия (уч.7кл.Стр.20)
- •Масса и размер молекул
- •Измерение скорости молекул. Опыт штерна(уч.10кл.Стр.236)
- •Количество вещества(уч.10кл.Стр.216-217)
- •Моль(уч.10кл.Стр.216-217)
- •Постоянная авогадро (уч.10кл.Стр.216-217)
- •Взаимодействие молекул
- •Модели газа, жидкости и твердого тела(уч.10кл.Стр.218-224)
- •Основы термодинамики (уч.10кл.Стр.284-285)
- •Тепловое равновесие температура и ее измерение(уч.10кл.Стр.239-241)
- •Абсолютная температурная шкала(уч.10кл.Стр.239-241)
- •Внутренняя энергия (уч.10кл.Стр.239-243, 261-264, уч.8кл.Стр.5-9)
- •Количество теплоты (уч.10кл.Стр.263-264, уч.8кл.Стр.18-29)
- •Работа в термодинамике(уч.10кл.Стр.265-267)
- •Первый закон термодинамики(уч.10кл.Стр.269-273)
- •Изотермический, изохорный и изобарный процессы(уч.10кл.Стр.252-257, 265-267, 270-271)
- •Адиабатный процесс(уч.10кл.Стр.272-274)
- •Необратимость тепловых процессов второй закон термодинамики и его статистическое истолкование (уч.10кл.Стр.281-283)
- •Преобразование энергии в тепловых двигателях (уч.10кл.Стр.275-280,уч.8кл.Стр.52-56 )
- •Кпд теплового двигателя. Цикл карно(уч.10кл.Стр.275-280 )
- •Идеальный газ (уч.10кл.Стр.222,229- )
- •Связь между давлением и средней кинетической энергией молекул идеального газа(уч.10кл.Стр.243-248)
- •Связь температуры со средней кинетической энергией частиц газа(уч.10кл.Стр.239-243)
- •Уравнение клайперона-менделеева(уч.10кл.Стр.248-251)
- •Универсальная газовая постоянная(уч.10кл.Стр.251- )
- •Жидкости и твердые тела основные положения (уч.10кл.Стр.307-308, 321-322)
- •Испарение и конденсация(уч.10кл.Стр.286-289,290-291)
- •Насыщенные и ненасыщенные пары(уч.10кл.Стр.286-291,292-293)
- •Влажность воздуха(уч.10кл.Стр.294-295,уч.8кл.Стр.46-47)
- •Кипение жидкости(уч.10кл.Стр.296-299,уч.8кл.Стр.44-45)
- •Поверхностное натяжение (уч.10кл.Стр.299-302)
- •Смачивание и каппилярность (уч.10кл.Стр.303-306)
- •Кристаллические и аморфные тела (уч.10кл.Стр.312-317)
- •Преобразование энергии при изменениях агрегатного состояния вещества(уч.10кл.Стр.218-224, 309-312,уч.8кл.Стр.48-50)
- •Измерение давления газа, влажности воздуха, температуры, плотности вещества
- •Основы электродинамики (уч.10кл.Стр.347 )
- •Электростатика основные положения (уч.10кл.Стр.376-377, 406-407)
- •Электризация тел(уч.10кл.Стр.350-352)
- •Электрический заряд(уч.10кл.Стр.347-349,356)
- •Взаимодействие зарядов(уч.10кл.Стр.347-349,)
- •Элементарный электрический заряд(уч.10кл.Стр.347-349)
- •Закон сохранения электрического заряда(уч.10кл.Стр.352-353)
- •Закон кулона(уч.10кл.Стр.354-362)
- •Электрическое поле
- •Напряженность электрического поля(уч.10кл.Стр.363-368, 374)
- •Электрическое поле точечного заряда(уч.10кл.Стр.363-365, 366-368)
- •Потенциальность электростатического поля(уч.10кл.Стр.378-381)
- •Разность потенциалов(уч.10кл.Стр.381-385)
- •Принцип суперпозиции полей(уч.10кл.Стр.368-375)
- •Проводники в электрическом поле(уч.10кл.Стр.392-396)
- •Электрическая емкость(уч.10кл.Стр.397-398 )
- •Конденсатор(уч.10кл.Стр.399-402)
- •Емкость плоского конденсатора(уч.10кл.Стр.400-402)
- •Диэлектрики в электрическом поле(уч.10кл.Стр.386-390)
- •Диэлектрическая проницаемость(уч.10кл.390-391)
- •Энергия электрического поля плоского конденсатора(уч.10кл.Стр.400-402, 403-406)
- •Постоянный электрический ток основные положения
- •Электрический ток
- •Сила тока
- •Напряжение
- •Носители свободных электрических зарядов в металлах, жидкостях и газах
- •Ток в газах
- •Ток в вакууме. Термоэлектронная эмиссия
- •Сопротивление проводников
- •Закон ома для участка цепи
- •Последовательное и параллельное соединение проводников
- •Электродвижущая сила
- •Работа и мощность тока. Кпд источника тока
- •Закон джоуля-ленца
- •Полупроводники основные положения
- •Проводимость полупроводников
- •Свободная и примесная проводимость полупроводников
- •Магнитное поле. Электромагнитная индукция основные положения
- •Взаимодействие магнитов
- •Магнитные свойства вещества. Магнитная проницаемость. Магнетики
- •Взаимодействие проводников с током
- •Магнитное поле
- •Действие магнитного поля на электрические заряды
- •Индукция магнитного поля. Поток магнитной индукции
- •Сила ампера
- •Сила лоренца
- •Электродвигатель (уч.8кл.Стр.143-145)
- •Электромагнитная индукция
- •Закон электромагнитной индукции фарадея-максвелла
- •Правило ленца
- •Вихревое электрическое поле
- •Самоиндукция (уч.11кл.Стр.123-126)
- •Индуктивность
- •Энергия магнитного поля
- •Измерение силы тока, напряжения, сопротивления проводника
- •Колебания и волны основные положения (уч.10кл. Стр.184-,345-346)
- •Механические колебания и волны основные положения ( уч.10кл.Стр.345-346)
- •Гармонические колебания (уч.10кл. Стр.69-70, уч.11кл.Стр.137)
- •Амплитуда, период и частота колебаний (уч.10кл. Стр.69-70)
- •Свободные колебания (уч.10кл. Стр.167-170)
- •Математический маятник (уч.10кл. Стр.167-172)
- •Период колебаний математического маятника (уч.10кл. Стр.167-172)
- •Превращения энергии при гармонических колебаниях
- •Вынужденные колебания (уч.10кл. Стр.167, 173-179)
- •Резонанс (уч.10кл. 177-183)
- •Понятие об автоколебаниях
- •Механические волны(уч.10кл.Стр.323-324)
- •Скорость распространения волны
- •Длина волны(уч.10кл.Стр.329)
- •Поперечные и продольные волны(уч.10кл.Стр.324-328)
- •Уравнение гармонической волны(уч.10кл.Стр.328-337)
- •Поляризация волн (уч.10кл.Стр.330-331)
- •Стоячие волны (уч.10кл.Стр.332-337)
- •Звук(уч.10кл.Стр.338-344)
- •Электромагнитные колебания и волны основные положения
- •Колебательный контур
- •Переменный электрический ток генератор переменного тока (уч.11кл.Стр.131)
- •Действующие значения силы тока и напряжения
- •Активное, емкостное и индуктивное сопротивления
- •Закон ома для переменного тока. Полное сопротивление цепи
- •Резонанс в электрической цепи
- •Трансформатор
- •Производство, передача и потребление электрической энергии (уч.11кл.Стр.134)
- •Идеи теории максвелла
- •Электромагнитные волны
- •Шкала электромагнитных волн
- •Скорость распространения электромагнитных волн
- •Свойства электромагнитный волн
- •Энергия электромагнитной волны
- •Принципы радиосвязи
- •Оптика основные положения
- •Принцип гюйгенса
- •Свет - электромагнитная волна
- •Прямолинейное распространение, отражение и преломление света
- •Законы преломления и отражения света
- •Показатель преломления
- •Полное внутреннее отражение
- •Предельный угол полного внутреннего отражения
- •Ход лучей в призме
- •Построение изображений в плоском зеркале
- •Собирающая и рассеивающая линзы
- •Формула тонкой линзы
- •Построение изображений в линзах (уч.11кл.Стр.243-249,257-259,
- •Оптические приборы
- •Фотоаппарат
- •Интерференция света
- •Зоны френеля
- •Когерентность
- •Дифракция света
- •Дифракционная решетка
- •Поляризация света. Поперечность световых волн
- •Дисперсия света
- •Поглощение света
- •Измерение фокусного расстояния собирающей линзы, показателя преломления вещества, длины волны света фотометрия .Световой поток. Освещенность
- •Спектры и спектральный анализ
- •Основы специальной теории относительности основные положения (уч.10кл.Стр.209)
- •Инвариантность скорости света (уч.10кл.Стр.186-187)
- •Принцип относительности эйнштейна (уч.10кл.Стр.186-189)
- •Пространство и время в специальной теории относительности (уч.10кл.Стр.186-205)
- •Связь массы и энергии (уч.10кл.Стр.205-209)
- •Квантовая физика основные положение (уч.10кл.Стр.227-228, уч.11кл.Стр. 345-346)
- •Тепловое излучение(уч.11кл.Стр.308-312)
- •Постоянная планка( уч.11кл.Стр.310)
- •Фотоэффект (уч.11кл.Стр.314-317)
- •Опыты столетова(уч.11кл.Стр.314)
- •Уравнение эйнштейна для фотоэффекта
- •Гипотеза луи де бройля(уч.11кл.Стр.322)
- •Дифракция электронов(уч.11кл.Стр.322-323)
- •Корпускулярно-волновой дуализм(уч.11кл.Стр.318-321,323-325)
- •Спектры(уч.11кл.Стр.336-339)
- •Люминесценция(уч.11кл.Стр.337-338)
- •Лазеры(уч.11кл.Стр.340-344)
- •1. Поглощение света
- •2. Спонтанное излучение
- •3. Индуцированное излучение
- •Ядерная физика основные положение (уч.10кл.Стр.227-228, уч.11кл.Стр.387-389,406)
- •Радиоактивность (уч.11кл.Стр.357-362,363-367)
- •Альфа-, бета-, гамма- излучения
- •Закон радиоактивного распада(уч.11кл.Стр.363-367)
- •Методы наблюдения и регистрации частиц в ядерной физике(уч.9кл.Стр.189-192)
- •Опыт резерфорда по рассеиванию альфа-частиц(уч.11кл.Стр.328)
- •Планетарная модель атома(уч.10кл.Стр.211-215,уч.11кл.Стр.329)
- •Модель атома резерфорда-бора. Квантовые постулаты бора(уч.11кл.Стр.330-336)
- •Нуклонная модель ядра (уч.10кл.Стр.211,уч.11кл.Стр.347)
- •Заряд ядра
- •Массовое число ядра
- •Энергия частиц в ядре. Энергия связи атомных ядер(уч.11кл.Стр.354-357)
- •Деление ядер. Цепная реакция(уч.11кл.Стр.367-372)
- •Синтез ядер(уч.11кл.Стр.378-383)
- •Ядерные реакции
- •Сохранение заряда и массового числа при ядерных реакциях
- •Выделение энергии при делении и синтезе ядер
- •Использование ядерной энергии(уч.11кл.Стр.373-377)
- •Дозиметрия. Биологическое действие ионизирующих излучений(уч.11кл.Стр.383- )
- •Элементарные частицы(уч.11кл.Стр.390-405)
- •Фундаментальные взаимодействия (уч.10кл.Стр.9-16)
- •Методы научного познания и физическая картина мира эксперимент и теория в процессе познания мира(уч.10кл.Стр.4-7)
- •Моделирование явлений и объектов природы (уч.10кл.Стр.7-9)
- •Научные гипотезы физические законы и границы их применимости(уч.10кл.Стр.9-16)
Кипение жидкости(уч.10кл.Стр.296-299,уч.8кл.Стр.44-45)
Физика кипения
Определение кипения
Определение температуры кипения
Зависимость температуры кипения от давления.
(Пример опреснительной установки)
Неизменность температуры кипения
Критическая температура
Понятие перегретой жидкости.
Испарение происходит с поверхности жидкости при любой температуре.
При определенных условиях процесс парообразования может происходить и внутри жидкости.
Кипение – парообразование, происходящее во всем объеме жидкости при определенной температуре.
Кипение – это интенсивный переход жидкости в пар, происходящий с образованием пузырьков пара по всему объему жидкости при определенной температуре.
При этой температуре, называемой температурой кипения, всплывают и лопаются
многочисленные пузырьки пара, вызывающие характерное бурление жидкости.
Температуру, при которой жидкость кипит, называют температурой кипения.
Во время кипения температура жидкости не меняется.
В жидкости всегда присутствуют растворенные газы, которые выделяются на дне и стенках сосуда, а так же на взвешенных в жидкости пылинках. Пары жидкости, которые находятся внутри пузырьков, являются ненасыщенными.
С увеличением температуры давление насыщенных паров возрастает, пузырьки увеличиваются в размерах. Под действием выталкивающей силы они всплывают.
Если верхние слои жидкости имеют более низкую температуру, то в этих слоях происходит конденсация пара в пузырьках. Давление стремительно падает и пузырьки захлопываются с характерным шумом..
При дальнейшем увеличении температуры жидкость внутри пузырьков с их поверхности испаряются молекулы жидкости. Замкнутый объем пузырька оказывается заполненным не только воздухом, но и насыщенным паром.
С повышением температуры давление насыщенного пара растет быстрее, чем давление воздуха, поэтому в достаточно нагретой жидкости давление внутри пузырька можно считать равным давлению насыщенного пара.
Увеличение объема пузырька происходит, когда давление насыщенного пара внутри него превосходит внешнее давление, равно сумме атмосферного и гидростатического давления столба жидкости.
p = pa + ρgh
При дальнейшем нагреве объем пузырька возрастает. Когда сила Архимеда превосходит силу сцепления пузырька со стенкой сосуда и силу тяжести пузырька mg, он отрывается от стенки и всплывает.

При подъеме в жидкости, имеющей постоянную температуру, пузырьки увеличиваются в объеме в соответствии с законом Бойля-Мариотта, так как внешнее давление по мере всплытия уменьшается.
Всплывшие пузырьки начинают лопаться, когда давление насыщенного пара, которым они наполнены, будет превосходить атмосферное давление:
pнп > pa
Температура кипения – температура, при которой давление насыщенного пара жидкости превосходит внешнее давление на жидкость.
Температура кипения зависит от внешнего давления на жидкость.
Температура кипения жидкости остается постоянной в процессе кипения
Это происходит потому, что вся подводимая к жидкости энергия расходуется на превращение ее в пар. (Каждый лопнувший пузырек охлаждает жидкость)
Зависимость давления насыщенного пара от температуры объясняет, почему температура кипения жидкости зависти от давления на ее поверхность. Кипение начинается при температуре, при которой давление насыщенного пара в пузырьках сравнивается с давлением в жидкости.
Чем больше внешнее давление, тем выше температура кипения.
Кипение начинается при температуре, при которой давление насыщенного пара в пузырьках сравнивается с давлением в жидкости. Чем больше внешнее давление, тем выше температура кипения.
У каждой жидкости своя температура кипения, которая зависит от давления насыщенного пара. Чем выше давление насыщенного пара, тем ниже температура кипения.
При увеличении температуры жидкости увеличивается давление насыщенного пара и одновременно растет его плотность. Плотность жидкости, находящейся в равновесии со своим паром, уменьшается вследствие расширения жидкости при нагревании.
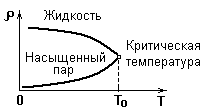
Зависимость плотностей жидкости и ее насыщенного пара от температуры при постоянном объеме.
При некоторой температуре, называемой критической, плотности жидкости и пара сравняются.
Критическая температура – это температура, при которой исчезают различия в физических свойствах между жидкостью и ее насыщенным паром.
При критической температуре плотность и давление насыщенного пара становятся максимальными, а плотность жидкости , находящейся в равновесии с паром, - минимальной.
Особое значение критической температуры состоит в том, что при температуре выше критической ни при каких давлениях газ нельзя обратить в жидкость. Газ, имеющий температуру ниже критической, представляет собой ненасыщенный пар.
Понижение температуры кипения при понижении давления используется в опреснительных установках.
Жидкость, не содержащая газа и находящаяся в сосуде, со стенок которого удален газ, не кипит.
Жидкость, нагретая до температуры, превышающей температуру кипения при нормальном давлении, называется перегретой.
