
- •Содержание
- •Введение
- •Порядок выполнения лабораторной работы
- •По технике безопасности
- •Некоторые свойства вероятностей
- •Введение в математическую статистку
- •Эмпирическая функция распределения
- •Гистограмма распределения
- •Числовые характеристики
- •Нормальное распределение
- •Свойства нормального распределения:
- •Правило 3 сигма
- •Задание
- •Контрольные вопросы
- •Свободные электроны в металлах
- •В ычисление анодного тока при задерживающем напряжении
- •Измерения и их обработка Приборы и принадлежности
- •Выполнение работы
- •Контрольные вопросы
- •Потенциал межмолекулярного взаимодействия
- •Соотношения между кинетической и потенциальной энергиями в агрегатных состояниях
- •Поверхностное натяжение
- •Механизм возникновения поверхностного натяжения
- •Капиллярные явления
- •Приборы и принадлежности
- •Вывод рабочей формулы
- •Порядок выполнения работы
- •Приборы и принадлежности
- •Вывод рабочей формулы
- •Порядок выполнения работы
- •Приборы и принадлежности
- •Описание установки
- •Вывод рабочей формулы
- •Порядок выполнения работы
- •Приборы и принадлежности
- •Описание установки и вывод рабочей формулы метода
- •Порядок выполнения работы
- •Контрольные вопросы
- •Объяснение эффекта Зеебека Объемная термоЭдс или различная зависимость средней энергии электронов от температуры в различных веществах
- •Контактная термоЭдс или различная зависимость от температуры контактной разности потенциалов в различных веществах
- •Объяснение эффекта Пельтье
- •Термоэлектрический модуль (элемент) Пельтье
- •Описание экспериментальной установки
- •Порядок выполнения работы Задача 1 - изучение эффекта Пельтье
- •Задача 2 - изучение эффекта Зеебека
- •Контрольные вопросы
- •Вывод формулы Пуазелля, коэффициент вязкости
- •Описание экспериментальной установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Постановка задачи
- •I. Метод вискозиметрии
- •Обоснование метода
- •Приборы и принадлежности
- •Описание вискозиметра
- •Порядок выполнения работы
- •II. Метод Стокса Обоснование метода
- •Приборы и принадлежности
- •Описание прибора
- •Порядок проведения работы
- •Контрольные вопросы
- •Оборудование
- •Вывод рабочей формулы
- •Порядок выполнения работы:
- •Порядок выполнения работы:
- •Контрольные вопросы
- •Постановка задачи
- •Описание установки
- •Вывод рабочей формулы
- •Порядок выполнения работы
- •Обработка результатов
- •Контрольные вопросы
- •Описание установки
- •Вывод рабочей формулы
- •Порядок выполнения работы
- •Контрольные вопросы
- •Классическая теория теплоемкости твердых тел (кристаллов)
- •Несовершенство классической теории теплоемкости
- •Квантовая теория теплоемкости Эйнштейна
- •Понятие о квантовой теории Дебая для теплоемкости твердых тел
- •Экспериментальная задача Приборы и принадлежности
- •Измерение теплоемкости методом охлаждения
- •Описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Постановка задачи
- •Описание установки
- •Величина χ при различных температурах
- •Контрольные вопросы
- •Основные понятия комбинаторики
- •1. Размещения с повторениями
- •2. Размещения без повторений
- •3. Перестановки без повторений
- •4. Перестановки с повторениями
- •5. Сочетания без повторений
- •Задача о картах и вероятности
- •Обработка результатов по методу наименьших квадратов
- •Обработка результатов измерений.
- •Очень нужно всем студентам знать!!!
- •При обработке результатов прямых измерений предлагается следующий порядок операций:
- •Ошибки величин являющихся функциями нескольких измеряемых величин
- •Изменение концентрации частиц при прохождении через потенциальный барьер
- •Вычисление относительной скорости
- •Условия применимости классической статистики
- •Границы применимости закона Максвелла распределения молекул газа по скоростям
- •Понятие о квантовой статистике Бозе — Эйнштейна и Ферми — Дирака. Переход к статистике Максвелла-Больцмана.
- •Литература
Потенциал межмолекулярного взаимодействия
В
Рис.1. Сила
межмолекулярного
взаимодействия
Рис.2. Потенциальная
энергия
межмолекулярного
взаимодействия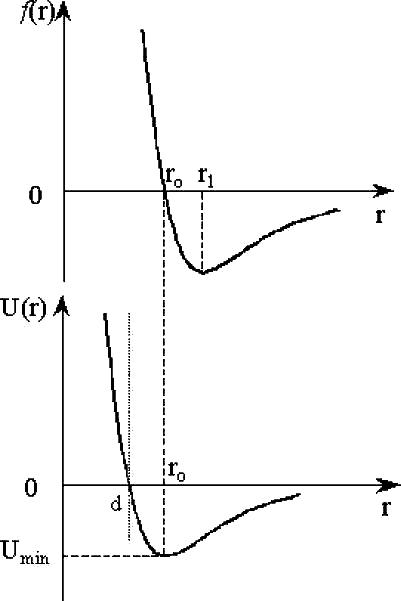
При построении этих кривых учитывают, что сила взаимодействия и потенциальная энергия молекул, находящихся на бесконечно большом расстоянии друг от друга положены равными нулю. На расстояниях r>r0 (рис.1) между молекулами действуют силы взаимного притяжения (отрицательный знак силы), а при r<r0 силы отталкивания (положительный знак силы). Из рис.1 видно, что по абсолютному значению сила притяжения растет с уменьшением r вплоть до некоторого значения r1. Затем сила уменьшается и при расстоянии r0 между атомами становится равной нулю. При дальнейшем уменьшении r сила вновь появляется, но уже сила отталкивания, быстро растущая с уменьшением расстояния между молекулами и стремясь к бесконечности при r → 0.
Кривой f(r) соответствует похожая на нее кривая U(r) (рис.2), поскольку они связаны соотношением:
![]()
При расстоянии между атомами r0, когда сила взаимодействия равна нулю (рисунок 1), потенциальная энергия проходит через минимум. О молекуле в таком положении принято говорить, что она находится на дне “потенциальной ямы”. Это положение равновесия, т. е. силы притяжения уравновешиваются силами отталкивания.
Какой–либо универсальной формулы U(r) пригодной для всех молекул не существует. Для многих задач описания свойств жидкостей к хорошим результатам приводит следующая аппроксимация функции U(r):
![]() , (1)
, (1)
в которой постоянные a1, a2, n, m подбираются из требований наилучшей аппроксимации реального потенциала для конкретного вещества. Как показало исследование потенциалов, в большинстве случаев хорошим приближением являются n=12, m=6. Функция U(r) описываемая уравнением (1), называется потенциалом Леннарда–Джонса, широко используется в теории жидкостей и газов. Первый член (1) соответствует силам отталкивания, второй – силам притяжения, которые называются силами Ван-дер-Ваальса.
В теории уравнения состояния Ван–дер–Ваальса применяется более грубая аппроксимация. Крутой участок кривой U(r) заменяется вертикальной прямой, как это изображено на рис.2 пунктиром. Если d – расстояние этой прямой от начала координат, то центры взаимодействующих частиц не могут сблизиться на расстояние, меньше d. Расстояние d играет роль эффективного диаметра молекулы. Приближение Ван-дер-Ваальса соответствует модели твердых упругих шаров, между которыми действуют только силы притяжения; а силы отталкивания учитываются тем, что существуют размеры шаров.
Соотношения между кинетической и потенциальной энергиями в агрегатных состояниях
Кинетическая энергия может быть только положительной, а потенциальная энергия как положительной, так и отрицательной. Если кинетическая энергия велика, так что сумма кинетической и потенциальной энергий рассматриваемой системы молекул всегда положительна, тогда молекулы, представленные самим себе, стремятся разойтись на бесконечно большое расстояние. Такое состояние системы – газ и он стремится к расширению.
При сжатии газа его плотность увеличивается, и среднее расстояние между молекулами уменьшается. При этом, как видно из рисунка 2, потенциальная энергия по модулю увеличивается. Если средняя кинетическая энергия молекул не слишком велика, то наступает такой момент, когда сумма кинетической и потенциальной энергий будет отрицательной. Такая система молекул уже не может самопроизвольно рассеяться в большем объеме f, молекулы удерживаются друг около друга в конечном объеме. Такое состояние системы молекул является либо жидким (кинетическая и потенциальная величины одного порядка), либо твердым (потенциальная по модулю много больше кинетической). Чаще всего при сжатии газа образуется жидкое состояние. Однако ударное сжатие может перевести систему сразу из газообразного в твердое состояние.
