
- •1.Перетворення білків в процесі технологічнї обробки
- •2.Біохімічна роль води в життєдіяльності людини.Джерела надходження
- •3.Вуглеводи:будова,класифікація
- •3.Вуглеводи:фізико-хімічні особливості
- •3. Вітамін в1: його хімічна роль. Харчові продукти, що містять в1.
- •5. Обчислити масову частку Сульфуру в цистеїні.
- •1. Повноцінні та неповноцінні білки.
- •2. Класифікація ліпідів.
- •3. Ферменти: будова, механізм дії.
- •5. Скільки (г) фруктози утвориться внаслідок гідролітичного розщеплення 200 г цукрози.
- •1. Специфічність ферментів.
- •2. Перетворення вуглеводів в процесі травлення.
- •3. Амінокислотний склад білків.
- •4. Якісна реакція на визначення аніону и03". Токсична дія нітратів.
- •5. Скільки (г) магнію міститься в 20 г магній сульфату?
- •1. Фактори, що впливають на активність ферментів.
- •2. Функції білків в організмі людини.
- •3. Перетворення ліпідів в процесі технологічної обробки.
- •4. Наявність якої функціональної групи доводить «реакцію срібного дзеркала».
- •5. В результаті окислення глюкози виділилось 44,8 л (н.У.) вуглекислого газу. Визначити масу глюкози, яку окиснено.
- •1. Пектинові речовини. Їх застосування в харчовій промисловості.
- •2. Функції ліпідів в організмі людини. Добова потреба.
- •3. Денатурація білка.
- •4. Якісна реакція на виявлення молочної кислоти.
- •5. Скільки (г) лугу ИаОн необхідно для приготування 200мл 0,5 м розчину?
- •1. Глікоген: будова, фізико-хімічні властивості, біологічна роль.
- •2. Поняття про ліпіди. Вміст жирів в харчових продуктах.
- •3. Перетворення білків в процесі травлення.
- •4. Якісна реакція на оцтову кислоту.
- •5. Скільки (г) №с1 та який об'єм води необхідно для приготування 500 г 5%-го розчину?
- •1. Вітамін в12: фізико-хімічні властивості, біологічна роль. Харчові продукти, що містять в12
- •2. Целюлоза: будова, властивості, вміст в харчових продуктах, перетворення в процесі травлення.
- •3. Фізико-хімічні властивості білків.
- •5. Обчислити вміст Нітрогену в глютаміновій кислоті.
- •5. Скільки (г) нс1 міститься в 800 г розчину, якщо масова частка розчиненої речовини складає 0,5%?
- •2.Застосування ферментів в харчовій промисловості.
- •2Функції вуглеводів в організмі людини
- •4.Скласти електронну формулу будови катіону Na. Біохімічна роль. Вміст в харчових продуктах.
- •1.Білки. Вміст білків в харчових продуктах.
- •2.Функції ліпідів о оргаізмі людини.
- •4. Скласти електронну формулу будови катіону Mg. Біохімічна роль. Вміст в харчових продуктах.
- •2.Функції білків а організмі людини.
- •3.Механізм дії ферментів
- •4. . Скласти електронну формулу будови катіону Zn. Біохімічна роль. Вміст в харчових продуктах.
- •1.Вітамін е:фізико-хімічні властивості, біохімічна роль, джерела надходження в організмі людини.
- •3.Повноцінні та неповноцінні білки.
- •1.Класифікація біогенних елементів.
- •2.Порівняльна характеристика глюкози і фруктози: будова, властивості.
- •1.Розчини. Способи вмісту розчиненої речовини в розчині.
- •4.Скласти електронну формулу будови катіону Na. Біохімічна роль. Вміст в харчових продуктах.
- •1.Вплив рН середовища на активність ферментів в біологічних рідинах
- •2.Функції вуглеводів в організмі людини
- •1.Способи очищення питної води
- •3.Фізико-хімічні властивості білка
- •2.Сучасні уявлення про структуру білка
- •3.Функції вуглеводів в організмі людини.
- •1.Предмет харчової хімії. Проблема та завдання харчової хімії.
- •1.Основні положення вчення Вернадського та правила Виноградова про біогенні хімічні елементи.
- •2.. Білки – це природні полімери, макромолекули які складаються з залишків амінокислот.
- •2.Функції білків а організмі людини.
- •3.Перетворення ліпідів в процесі травлення
- •4.Скласти електронну формулу будови катіону Fe. Біохімічна роль. Вміст в харчових продуктах.
- •2.Класифікація ферментів
- •2.. Вміст білків в харчових продуктах(%):
3. Денатурація білка.
Денатурація - втрата білком своїх нативних (природних) властивостей під впливом деяких факторів (температури, тиску, зміни рН-середовища, ультразвуку, йонізуючого випромінювання, органічних і неорганічних кислот, лугів, солей важких металів тощо). При денатурації руйнується четвертинна, третинна і вторинна структури, первинна структура залишається незмінною
4. Якісна реакція на виявлення молочної кислоти.
5. Скільки (г) лугу ИаОн необхідно для приготування 200мл 0,5 м розчину?
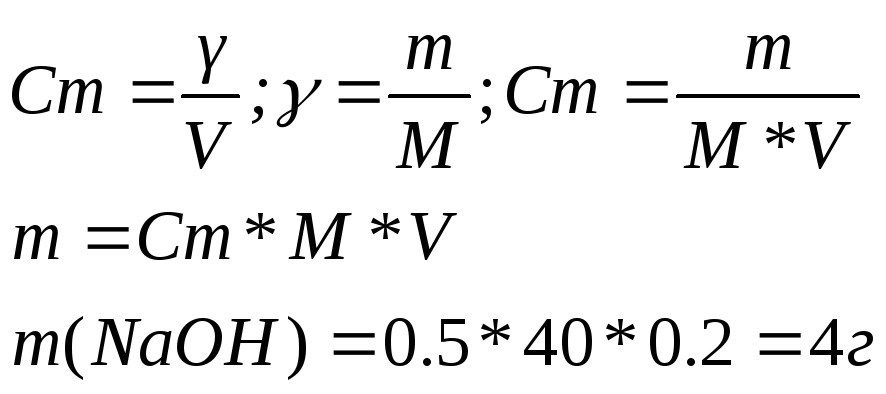
Білет8
1. Глікоген: будова, фізико-хімічні властивості, біологічна роль.
Глікоген, або тваринний крохмаль. Глікоген, як і крохмаль, побудований із залишків глюкози і має таку саму загальну формулу (СвН10О6)„. В організмах людини і тварин він відіграє роль резервного полісахариду. Всі процеси життєдіяльності, і в першу чергу робота м'язів, проходять одночасно з розщепленням глікогену.
Глікоген є в усіх тканинах організму людини. Особливо багато його в печінці (2—5 %) і м'язах (0,5—2 %). Глікоген — білий аморфний порошок, добре розчиняється навіть у холодній воді. При розчиненні він утворює колоїдні розчини.
За хімічною структурою глікоген схожий з амілопектином. Від амілопектину він відрізняється тільки більшою розгалуженістю молекули, більшою молекулярною масою, яка досягає кількох мільйонів. З розчином йоду глікоген дає забарвлення від винно-червоного до червоно-бурого, залежі: і від виду тварин, з яких його було виділено. Глікоген в організмах людини і тварин синтезується з глюкози і нагромаджується в органах і тканинах, а в періоди між прийманням їжі він розщеплюється і постачає організм глюкозою.
2. Поняття про ліпіди. Вміст жирів в харчових продуктах.
Ліпіди — це низькомолекулярні речовини з гідрофобними властивостями. Разом з білками і вуглеводами це основні компоненти всіх видів клітин. У різних органах і тканинах вміст ліпідів неоднаковий. Особливо багато їх у нервовій тканині, серці, печінці, нирках, крові, насінні і плодах деяких рослин. Яловичина 3,8-25Свинина 6,3-41,3Баранина 5,8-33,6Риба 0,4-20, Молоко коров’яче 3,2-4,5Вершкове 61-83,5Яйця 12,1Насіння соняшникове 15-35Арахіс 40-55Грецький 58-74Хліб житній 1,2 Олія 98
3. Перетворення білків в процесі травлення.
Розщеплення білків у шлунку - до пептидів. Фермети - пепсин, гастриксин, хімозин (у дітей). Розщеплення білків у тонкій кишці - до амінокислот. Фермети - ферменти підшлункової залози: трипсин, хімотрипсин, слизової оболонки кишок: ентерокіназа, карбоксипептидази, амінопептидази. Продукти гідролізу білка амінокислоти всмоктуються в кінцевій частині дванадцятипалої і на початку тонкої клубової кишок і попадають у кров, а звідти до клітин різних органів і насамперед до печінки. Амінокислоти, які не всмокталися в тонкій кишці, а потрапили у товсту кишку, піддаються різним перетворенням під дією ферментів мікроорганізмів. Цей процес дістав назву гниття білків. При цьому найбільш поширене декарбоксилування та деякі інші види перетворень, що призводять до утворення з амінокислот токсичних речовин: амінів, індолу, скатолу, фенолу, крезолу.
