
- •Химия и технология гомогенного катализа Конспект лекций Москва 2012
- •Предисловие
- •Общие проблемы катализа
- •1.1 Краткая история открытия каталитических реакций и теории катализа
- •Краткая история открытия каталитических реакций
- •1.2 Теории катализа
- •1.3 Классификации каталитических процессов и катализаторов
- •1.3.1 Классификация каталитических процессов
- •1.3.2 Классификации катализаторов
- •2. Выбор катализаторов
- •2.1 Современное содержание термина «активация»
- •2.1.1 Классификация комплексов
- •Карбеновые комплексы:
- •Карбиновые комплексы
- •2.2 Активация молекул
- •2.2.1 Молекула водорода
- •2.2.2 Молекула монооксида углерода
- •2.2.3 Активация алкенов и алкинов
- •2.2.3.1 Реакции координированных алкенов
- •2.2.3.2 Реакции координированных алкинов
- •2.2.4 Активация полярных молекул
- •2.3 Проблема выбора катализатора и возможные пути ее решения
- •2.3.1 Эмпирический подход.
- •2.3.2 Полуэмпирический метод.
- •2.3.3 Теоретический подход.
- •2.4 Требования к промышленным катализаторам
- •2.4.1 Активность (производительность)
- •2.4.2 Селективность.
- •2.4.3 Стабильность.
- •2.4.4 Наличие методик регенерации и утилизации
- •2.4.5 Воспроизводимость.
- •2.4.6 Экологичность.
- •2.4.7 Экономичность.
- •Технология гомогенного катализа
- •Методы приготовления и исследования гомогенных катализаторов
- •3.1 Приготовление гомогенных катализаторов
- •3.2 Методы исследования гомогенных катализаторов и процессов с их участием
- •3.2.1 Дифракционные методы
- •3.2.2 Электронографический анализ (эга)
- •3.2.3 Спектроскопические методы.
- •3.2.4 Масс-спектрометрия
- •Технология синтеза и разделения реакционных систем на основе гомогенных катализаторов
- •4.1 Выбор реактора
- •4.2 Методы разделения катализаторов и продуктов, используемые для гомогенно-каталитических реакционных систем
- •4.2.1. Выделение наиболее ценных компонентов каталитической системы (чаще всего благородных металлов).
- •4.2.2 Выделение продуктов гомогенно-каталитической реакции.
- •4.3 Гидроформилирование алкенов (Оксосинтез)
- •4.3.1 Схемы с термической декобальтизацией (выделение кобальта в виде металла на поверхности твердой фазы носителя)
- •4.3.2 Солевые схемы (выделение металла в виде соли за счет экстракции)
- •4.3.3 Испарительные схемы (отделение продуктов за счет отгонки )
- •Оксосинтез в двухфазных системах вода-органический растворитель
- •4.4 Технология производства ацетальдегида
- •4.4.1 Механизм и кинетика Вакер-процесса.
- •4.4.2 Технология получения ацетальдегида
- •4.5 Технология производства уксусной кислоты.
- •4.6 Технология производства высших олефинов фирмы Шелл (shop process)
- •4.6.1 Олигомеризация
- •4.6.2 Гидроформилирование
- •4.6.3 Изомеризация
- •4.6.4 Метатезис
- •4.6.5 Технология shop процесса
Оксосинтез в двухфазных системах вода-органический растворитель
Гидроформилирование алкенов можно проводить в системах, содержащих воду и несмешивающийся с ней органический растворитель, служащий экстрагентом для продуктов процесса. В таких случаях обычно используют каталитические системы, включающие комплексы родия с водорастворимыми фосфиновыми лигандами. Хорошая растворимость комплексов родия в воде и нерастворимость в органическом растворителе достигается за счёт использования сульфированных фосфинов. Гомогенно-каталитический процесс протекает в водной фазе, а продукты экстрагируются в органическую фазу. В качестве промышленного процесса такого типа можно привести вариант технологии, разработанный фирмами Рурхеми и Рон Пуленк (Ruhrchemie - Rȏne Poulenc), в котором применяют в качестве лиганда натриевую соль трифенилфосфин-три-метасульфоната P(PhSO3Na)3 (TPPTS). Растворимость TPPTS в воде составляет 1200 г/л.
Упрощенная технологическая схема процесса Рурхеми – Рон Пуленк, используемого для получения масляных альдегидов, включает реактор (1), фазовый сепаратор для разделения жидких фаз (2), холодильник (3), подсистему разделения (4, 5) (рис. 18). Водная фаза, содержащая комплекс родия, из сепаратора (2) через холодильник (3) возвращается в реактор (1). Органический слой, содержащий н-масляный и изомасляный альдегиды, отделяют в сепараторе и подают на разделение.
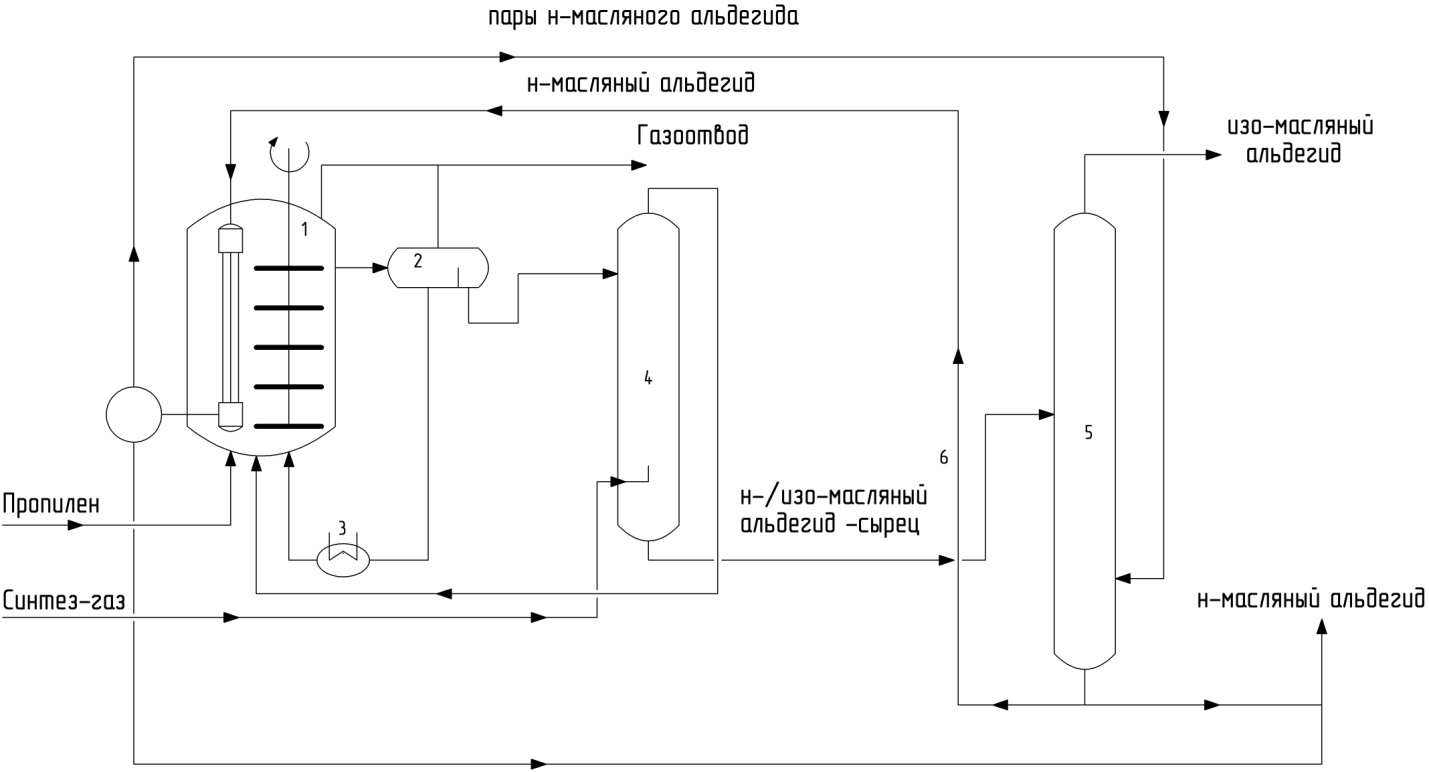
Рис. 18. Схема оксо-процесса в двухфазной системе фирм Рурхеми и Рон-Пуленк
В промышленности процесс гидроформилирования с использованием водорастворимого катализатора Rh-TPPTS применяется c 1984 г. до настоящего времени фирмой Рурхеми для производства бутиловых и 2-этилгексилового спиртов с суммарной мощностью 620000 т/г, а также амиловых и 2-пропилгексиловых спиртов (12000 т/г).
К преимуществам процесса с использованием катализатора Rh-TPPTS по сравнению с системой Rh-PPh3 относятся простота технологии разделения катализатора и продуктов (потери катализатора с продуктами менее 1 ppm), низкое соотношение лиганд: родий (~10), обеспечивающее более высокую региоселективность. К недостаткам этого процесса относят высокие скорости потока раствора катализатора через реактор, повышенные концентрации родия и несколько более жесткие условия реакции. Кроме того, применимость этого варианта технологии имеет ограничения по сырью, а именно, низкая растворимость в воде алкенов с длиной углеродной цепи более 4 не позволяет достигать практически приемлемых скоростей гидроформилирования.
4.4 Технология производства ацетальдегида
Уксусный альдегид и уксусная кислота – продукты, используемые людьми тысячи лет. В допромышленную эпоху эти продукты получали с помощью ферментативного катализа при брожении растительных продуктов. Первый промышленный способ получения ацетальдегида основан на реакции гидратации ацетилена, открытой Кучеровым в 1881 г.
Hg2+
С2Н2 + Н2О —→ CH3CHO
Производство ацетальдегида этим способом началось в 1916 г. в Германии. Основной недостаток этого процесса – токсичность катализатора.
Кроме этого ацетальдегид получали дегидрированием и окислительным дегидрированием этилового спирта на оксидных ( ZnO, CuO, FeO) и металлических катализаторах (Ag, Cu, Au), соответственно.
Более эффективный способ – окислением этилена был разработан в конце 50-х почти одновременно группой Смидта, Хафнера и др. (Консорциум электрохимической промышленности) и И.И. Моисеевым, М.Н. Варгафтиком и Я.К. Сыркиным (МИТХТ им. М.В. Ломоносова). Метод был основан на трех стехиометрических реакциях, которые в совокупности складывались в каталитический цикл. Cложение этих реакций приводит к итоговому уравнению каталитического процесса.
C2H4 + H2O + PdCl2 → CH3CHO + Pd(0) + 2 HCl
Pd(0) + 2 CuCl2 → PdCl2 + 2 CuCl
2 CuCl + 2 HCl + 0,5 O2 → 2 CuCl2 + H2O
С2Н4 + 0,5 O2 → CН3СНО
Это полифункциональная каталитическая система, в которой каждый из трех катализаторов (PdCl2, CuCl2, H2O) выполняет свою кинетическую функцию. Палладий (II) и нуклеофильный катализатор – вода – участвуют в стадиях окисления этилена в ацетальдегид (механизм приведен ниже). Медь (II) катализирует окисление восстановленного палладия кислородом.
Процесс может проводиться с различными алкенами. Продуктами являются альдегиды и кетоны. Показатели зависят от природы используемого алкена. В случае этилена селективность – до 95%, побочные продукты – уксусная кислота – 2%, СО2 – 1%, хлорпроизводные – 1% (хлористый метил, хлористый этил, хлоруксусный альдегид). В случае окисления пропилена основным продуктом является ацетон. Селективность его образования достигает 90%. Пропионовый альдегид является побочным продуктом.
