
- •Химия и технология гомогенного катализа Конспект лекций Москва 2012
- •Предисловие
- •Общие проблемы катализа
- •1.1 Краткая история открытия каталитических реакций и теории катализа
- •Краткая история открытия каталитических реакций
- •1.2 Теории катализа
- •1.3 Классификации каталитических процессов и катализаторов
- •1.3.1 Классификация каталитических процессов
- •1.3.2 Классификации катализаторов
- •2. Выбор катализаторов
- •2.1 Современное содержание термина «активация»
- •2.1.1 Классификация комплексов
- •Карбеновые комплексы:
- •Карбиновые комплексы
- •2.2 Активация молекул
- •2.2.1 Молекула водорода
- •2.2.2 Молекула монооксида углерода
- •2.2.3 Активация алкенов и алкинов
- •2.2.3.1 Реакции координированных алкенов
- •2.2.3.2 Реакции координированных алкинов
- •2.2.4 Активация полярных молекул
- •2.3 Проблема выбора катализатора и возможные пути ее решения
- •2.3.1 Эмпирический подход.
- •2.3.2 Полуэмпирический метод.
- •2.3.3 Теоретический подход.
- •2.4 Требования к промышленным катализаторам
- •2.4.1 Активность (производительность)
- •2.4.2 Селективность.
- •2.4.3 Стабильность.
- •2.4.4 Наличие методик регенерации и утилизации
- •2.4.5 Воспроизводимость.
- •2.4.6 Экологичность.
- •2.4.7 Экономичность.
- •Технология гомогенного катализа
- •Методы приготовления и исследования гомогенных катализаторов
- •3.1 Приготовление гомогенных катализаторов
- •3.2 Методы исследования гомогенных катализаторов и процессов с их участием
- •3.2.1 Дифракционные методы
- •3.2.2 Электронографический анализ (эга)
- •3.2.3 Спектроскопические методы.
- •3.2.4 Масс-спектрометрия
- •Технология синтеза и разделения реакционных систем на основе гомогенных катализаторов
- •4.1 Выбор реактора
- •4.2 Методы разделения катализаторов и продуктов, используемые для гомогенно-каталитических реакционных систем
- •4.2.1. Выделение наиболее ценных компонентов каталитической системы (чаще всего благородных металлов).
- •4.2.2 Выделение продуктов гомогенно-каталитической реакции.
- •4.3 Гидроформилирование алкенов (Оксосинтез)
- •4.3.1 Схемы с термической декобальтизацией (выделение кобальта в виде металла на поверхности твердой фазы носителя)
- •4.3.2 Солевые схемы (выделение металла в виде соли за счет экстракции)
- •4.3.3 Испарительные схемы (отделение продуктов за счет отгонки )
- •Оксосинтез в двухфазных системах вода-органический растворитель
- •4.4 Технология производства ацетальдегида
- •4.4.1 Механизм и кинетика Вакер-процесса.
- •4.4.2 Технология получения ацетальдегида
- •4.5 Технология производства уксусной кислоты.
- •4.6 Технология производства высших олефинов фирмы Шелл (shop process)
- •4.6.1 Олигомеризация
- •4.6.2 Гидроформилирование
- •4.6.3 Изомеризация
- •4.6.4 Метатезис
- •4.6.5 Технология shop процесса
4.3.2 Солевые схемы (выделение металла в виде соли за счет экстракции)
Схемы декобальтизации, основанные на экстракции, называют солевыми. Лучшим экстрагентом для извлечения солей кобальта (см. вышеприведенные требования) оказалась вода. Для экстракции соединений кобальта водой и уменьшения его растворимости в органическом растворе нужно перевести карбонилы кобальта в соль. Это достигается действием окислителя в присутствии кислоты. В качестве окислителей используют кислород воздуха, пероксид водорода, азотную кислоту. В качестве кислот - муравьиную, уксусную и азотную кислоту. Образующаяся соль кобальта(II) переходит в водную фазу и в виде водного раствора подается на стадию карбонилообразования.
Со2(СО)8 + О2 + 4НХ 2CоХ2 + 8СО + 2Н2О
3Со2(СО)8 + 16НNО3 6Cо(NО3)2 + 4NО + 8Н2О + 24СО
На стадии карбонилообразования происходит взаимодействие соли кобальта(II) c синтез-газом с восстановлением кобальта в карбонильные соединения.
2СоХ2 + 8СО + 2Н2 Со2(СО)8 + 4НХ
2СоХ2 + 8СО + 3Н2 2НСо(СО)4 + 4НХ
Если воду на стадии декобальтизации не добавляют, то соль кобальта может образовать суспензию и отделяться от органических продуктов фильтрованием или центрифугированием. В этом случае соль кобальта возвращают на стадию карбонилообразования в виде суспензии в инертном растворителе, используемом в процессе (рис. 13).

Рис. 13. Солевая схема оксосинтеза
К солевым схемам можно отнести и так называемую кульмановскую схему, в которой не используется окислитель, а главную роль играют кислотные свойства гидрокарбонила кобальта (рис. 14). Процесс протекает в реакторе 1 в обычных для этого катализатора условиях: 110-180о и давлении синтез-газа 20-25 МПа. После необходимого времени пребывания в реакторе (1 – 2 ч) контактный раствор попадает в колонну 2, в которой контактирует с водным раствором соды. При этом происходит реакция нейтрализации гидрокарбонила кобальта и экстракция образовавшегося солеобразного карбонила в водную фазу.
НСо(СО)4 + Nа2СО3 NаСо(СО)4 + NaHСО3
Продукты из колонны 2 поступают в фазовый сепаратор 3, в котором удаляются остаточные газы и разделяются органическая и водная фазы. Органическая фаза поступает в следующую экстракционную колонну 2, где отмывается водой от остатков катализатора и следует в систему разделения (на рис. не показана). Водные фазы смешиваются и поступают в колонну 4, в которой подкисляются серной кислотой. Снизу в колонну 4 подают синтез-газ. В колонне 4 регенерируется летучий и умеренно растворимый в кислоте гидрокарбонил кобаль-
2 NаСо(СО)4 + Н2SО4 2 НСо(СО)4 + Nа2SО4
та и в токе синтез-газа возгоняется в колонну 5. Туда же подают алкен и растворитель, в растворе которых гидрокарбонил кобальта поступает в реактор 1 для проведения гидроформилирования (рис. 14).
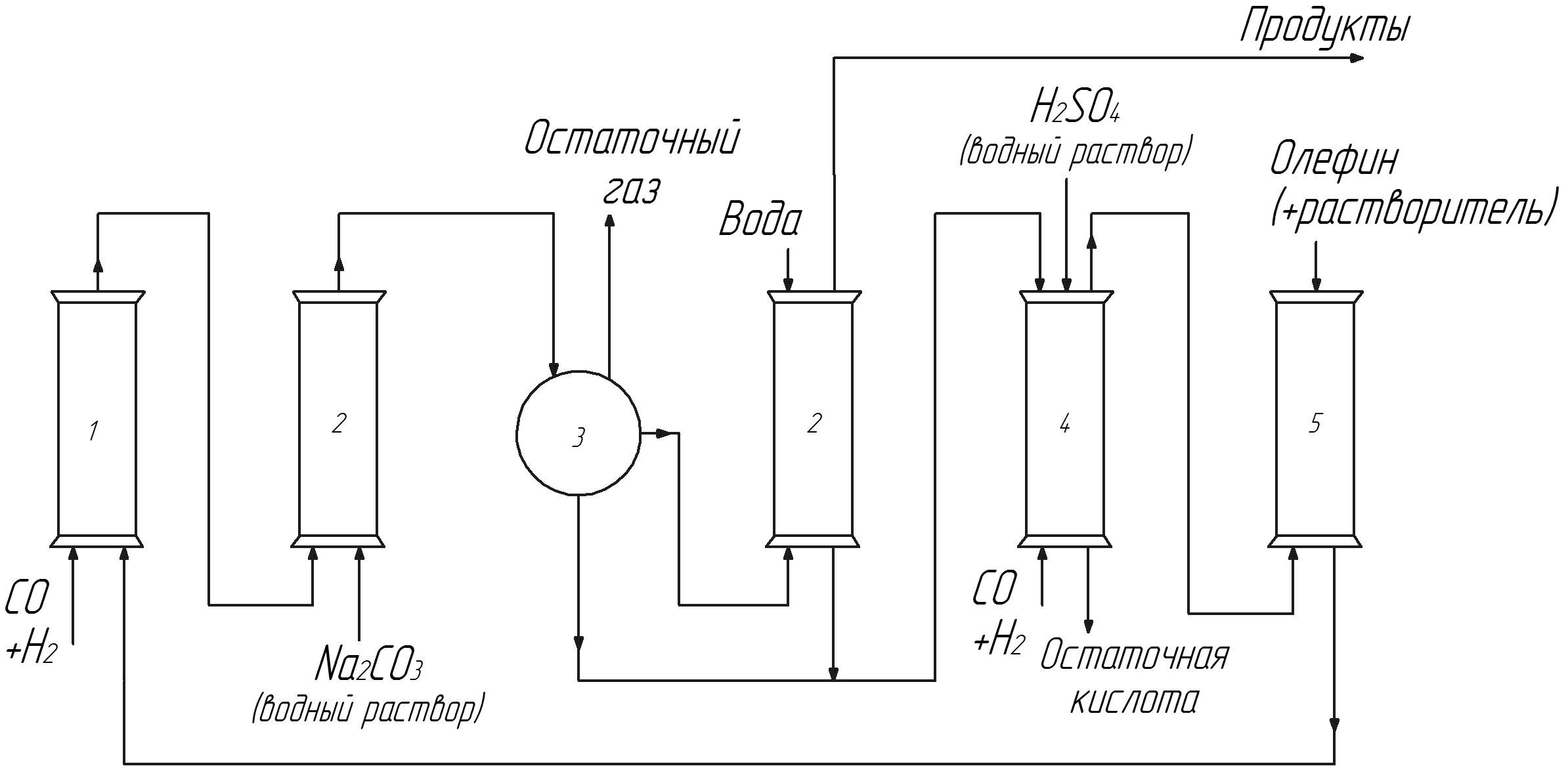
Рис. 14. Кульмановская схема оксосинтеза
Достоинством солевых схем является отсутствие необходимости использовать реактор высокого давления на стадии декобальтизации, а также сохранение альдегидов в качестве основных продуктов оксосинтеза. Более эффективны эти схемы в применении к гидроформилированию высших алкенов в альдегиды. Недостатки этих схем связаны с применением дополнительных реагентов, появлением сточных вод и усилением коррозии оборудования.
