
- •Предмет, содержание, задачи токсикологической химии.
- •Краткий исторический очерк развития токсикологической химии.
- •Связь токсикологической химии с другими химическими, фармацевтическими и биологическими науками.
- •Вклад отечественных учёных в развитие токсикологической химии.
- •Организация судебно-медицинской и химико-токсикологической (судебно-химической) экспертизы в России.
- •Объекты химико-токсикологического исследования и вопросы, решаемые химико-токсикологическим анализом. Понятие «яд», «ядовитое вещество». Классификация ядов и отравлений.
- •Специфические особенности химико-токсикологического анализа.
- •Пути поступления чужеродных соединений в организм. Основные факторы, оказывающие влияние на всасываемость и распределение веществ в тканях и биологических средах организма.
- •Превращение и выделение чужеродных веществ из организма. Общая характеристика.
- •Общая характеристика методов исследования, применяемых в токсикологической химии (методы изолирования, очистки, качественного и количественного анализа).
- •11. Судебная химия – основной раздел токсикологической химии.
- •Документация химико-токсикологических экспертиз и правила её
- •Источники ошибок на основных этапах химико-токсикологического анализа.
- •Правила приёма вещественных (химических) доказательств на экспертизу.
- •Значение данных дознания, истории болезни и результатов судебно-медицинского исследования трупов для судебно-химической экспертизы.
- •Микрокристаллоскопия и кристаллооптика в токсикологической химии.
- •Методы количественного определения. Значение этих определений для оценки результатов исследования (показать на примере «металлических ядов»).
- •Реакции отрицательного судебно-химического значения.
- •Классификация ядовитых и сильнодействующих веществ в токсикологической химии.
- •Охрана окружающей среды и перспективы развития токсикологической химии на современном этапе.
- •Классификация наркотических и психотропных веществ. Основные особенности их химико-токсикологического анализа.
- •Современные физико-химические методы, применяемые в анализе наркотических и психотропных веществ. Основные требования к ним.
- •Фармакокинетика, метаболизм, особенности химико-токсикологического анализа опиатов.
- •Фармакокинетика, метаболизм, особенности химико-токсикологического анализа каннабиноидов.
- •Перспективы развития и совершенствования методов судебно-химических исследований вещественных доказательств.
- •26. Теоретические основы изолирования ядовитых и сильнодействующих веществ из биологического материала дистилляцией водяным паром.
- •27.Синильная кислота. Качественное обнаружение и количественное определение.
- •28. Химико-токсикологическое значение синильной кислоты и её производных.
- •29. Ядовитые галогенпроизводные (хлороформ, хлоралгидрат). Изолирование.
- •30. Ядовитые галогенпроизводные (четыреххлористый углерод, 1,2-дихлорэтан).
- •31. Альдегиды (формалин, формальдегид). Изолирование, качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •32. Ацетон. Изолирование, качественное обнаружение и количественное
- •33. Метиловый спирт. Изолирование, качественное обнаружение и количественное
- •34. Этиловый спирт. Изолирование. Качественное обнаружение и количественное
- •35. Физико-химические методы количественного определения этилового спирта, применение в судебно-химическом анализе.
- •36. Значение этапа количественного определения этилового спирта при химико-токсикологическом исследовании биологических объектов.
- •37. Реакции отличия метилового и этилового спирта. Методы экспресс-анализа спирта. Пробы Раппопорта и Шинкаренко.
- •38.Спирты (амиловый, этиленгликоль). Качественное обнаружение. Токсикологическое значение. Метаболизм.
- •39. Уксусная кислота. Изолирование. Качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •40. Нитробензол в химико-токсикологическом отношении.
- •41. Фенолы (фенол, трикрезол) в химико-токсикологическом отношении.
- •42. Анилин в химико-токсикологическом отношении.
- •43. Метод изолирования подкисленным спиртом. Его достоинства и недостатки.
- •44. Метод изолирования подкисленной водой. Вклад отечественных учёных в разработку этого метода, его достоинства и недостатки.
- •45. Частный метод изолирования подкисленной водой в.Ф. Крамаренко. Влияние рН среды и др. Факторов на изолирование и экстрагирование алкалоидов.
- •46. Метод изолирования подщелоченной водой, его достоинства и недостатки.
- •47. Салициловая кислота. Изолирование, качественное обнаружение и количественное обнаружение. Токсикологическое значение и метаболизм.
- •48. Химико-токсикологическое значение производных барбитуровой кислоты. Методы изолирования, очистки барбитуратов.
- •49. Качественное обнаружение барбитуратов в судебно-химическом анализе.
- •50. Количественное определение барбитуратов в судебно-химическом анализе.
- •51. Спектрофотометрическое определение производных барбитуровой кислоты в химико-токсикологическом анализе.
- •52. Токсикологическое значение и метаболизм барбитуратов.
- •53. Фенацетин. Качественное обнаружение и количественное определение.
- •54. Предварительные химико-токсикологические исследования при наличии алкалоидов (общеалкалоидные реакции).
- •55. Методы изолирования, очистки и обнаружение алкалоидов.
- •56. Алкалоиды, производные пиридина и пиперидина (кониин, ареколин). Изолирование, качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •57. Алкалоиды, производные пиридина и пиперидина (никотин, анабазин) в химико-токсикологическом отношении.
- •58. Пахикарпин в химико-токсикологическом отношении.
- •59. Алкалоиды, производные тропана (атропин, гиосциамин) в химико-токсикологическом отношении.
- •60. Алкалоиды, производные тропана (кокаин) в химико-токсикологическом отношении.
- •61. Производные аминокислот ароматического ряда (новокаин, дикаин) в химико-токсикологическом отношении.
- •62. Алкалоиды, производные хинолина (хинин и его соли). Изолирование, качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •63. Алкалоиды, производные изохинолина (морфин). Изолирование. Качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •64. Заменители морфина (кодеин, этилморфина гидрохлорид, апоморфин) в химико-токсикологическом отношении.
- •65. Доказательства отравления опием.
- •66. Алкалоиды, производные бензилизохинолина (папаверин, наркотин) в химико-токсикологическом отношении.
- •67. Алкалоиды, производные индола (резерпин, секуренин) в химико-токсикологическом отношении.
- •69. Алкалоиды, производные пирролизидина (платифиллин) в химико-токсикологическом отношении.
- •70. Алкалоиды, производные пиримидина (кофеин, теобромин, теофиллин) в химико-токсикологическом отношении.
- •71. Ациклические алкалоиды (эфедрин). Изолирование, обнаружение, определение, значение, метаболизм.
- •72. Производные пиразола (антипирин, амидопирин) в химико-токсикологическом отношении.
- •73. Производные 1,4 - бензодиазепина в химико-токсикологическом отношении.
- •74. Производные фенотиазина в химико-токсикологическом отношении.
- •75. Общая характеристика пестицидов (ядохимикатов) в химико-токсикологическом отношении. Классификация.
- •76. Пестициды из группы галогенпроизводных (ддт, гхцг, гептахлор) в химико-токсикологическом отношении.
- •77. Пестициды из класса фенолов (днок, диносеб, зоокумарин). Качественное обнаружение и количественное определение. Токсикологическое значение и метаболизм.
- •78. Пестициды класса фосфорорганических соединений (хлорофос, карбофос) в химико-токсикологическом отношении.
- •79. Пестициды, производные карбаминовой кислоты (севин) в химико-токсикологическом отношении.
- •80. Пестициды, производные тиокарбаминовой, дитиокарбаминовой кислот (крысид, тмтд) в химико-токсикологическом отношении.
- •81. Металлоорганические пестициды (гранозан, меркуран, меркургексан) в химико-токсикологическом отношении.
- •82. Неорганические ядохимикаты (фосфид цинка, фторид натрия) в химико-токсикологическом отношении.
- •83. Общая характеристика сероводородного и дробного методов анализа «металлических» ядов.
- •84. Вклад отечественных учёных в разработку химико-токсикологического анализа «металлических ядов».
- •85. Теоретические и методологические основы дробного метода анализа «металлических» ядов, разработанные а.Н. Крыловой.
- •86. Органические реагенты, предложенные а.Н. Крыловой для анализа «металлических» ядов дробным методом.
- •87. Последовательность проведения дробного метода анализа на «металлические» яды.
- •88. Частые методы минерализации органических веществ.
- •89. Минерализация серной и азотной кислотами органических веществ. Достоинства и недостатки.
- •90. Минерализация органических веществ азотной, серной, хлорной кислотами. Достоинства и недостатки метода.
- •91. Методы удаления окислителей из минерализата.
- •92. Исследование осадка после минерализации азотной, серной кислотами (свинец, барий).
- •93. Свинец и тетраэтилсвинец. Качественное обнаружение и количественное определение. Токсикологическое значение.
- •94. Барий в химико-токсикологическом отношении.
- •95. Марганец в химико-токсикологическом отношении.
- •96. Хром в химико-токсикологическом отношении.
- •97. Серебро. Изолирование, качественное обнаружение и количественное определение, поступление, распределение, выведение из организма, токсикологическое значение.
- •98. Медь в химико-токсикологическом отношении.
- •99. Висмут в химико-токсикологическом отношении.
- •100. Сурьма и таллий в химико-токсикологическом отношении.
- •101. Кадмий в химико-токсикологическом отношении.
- •102. Цинк в химико-токсикологическом отношении.
- •103. Ртуть, деструктивные методы изолирования. Качественное и количественное значение. Органические препараты ртути (этилмеркурхлорид).
- •104. Мышьяк в химико-токсикологическом отношении. Общая схема анализа.
- •105. Определение мышьяка в аппарате Марша.
- •106. Определение мышьяка в аппарате Зангер-Блека.
- •107. Изолирование веществ из биологического материала диализом (серная, азотная, соляная кислоты). Качественное обнаружение и количественное определение, токсикологическое значение.
- •108. Изолирование веществ из биологического материала диализом (аммиак, едкий натр, щелочные соли). Качественное обнаружение и количественное определение, токсикологическое значение.
42. Анилин в химико-токсикологическом отношении.
Анилин – маслянистая жидкость, почти бесцветная в чистом состоянии, но быстро темнеющая на воздухе в результате окисления кислородом воздуха на свету. Анилин хорошо растворим в сероуглероде, жирах, эфире, этаноле. Нерастворим в воде.
Отравление анилином наступает при вдыхании паров анилина, всасывается даже через неповреждённую кожу. После приёма алкоголя чувствительность к анилину повышается. Анилин оказывает парализующее действие на сосудистую и нервную систему. В крови увеличивается содержание метгемоглобина. При смертельном отравлении в агональном состоянии появляются симптомы поражения ЦНС: клонические и тетанические судороги, наступает паралич дыхательного центра. Патологоанатомически: серые трупные пятна. Канальцы почек забиты метгемоглобином. Кровь не свёртывается. Дегенеративные изменения в паренхиматозных органах, главным образом, в почках.
Качественное обнаружение: часть дистиллята смешивают с насыщенным раствором бромной воды – в воде белый осадок 2, 4, 6-триброманилина.

Реакция высокочувствительная и лежит в основе количественного определения анилина. Как качественная реакция для анилина она неспецифична. Для реакции придаётся отрицательное химико-токсикологическое значение.
Взаимодействие с хлорамином и фенолом анилин и его производное образует индофенол, щелочная соль которого имеет синий цвет.
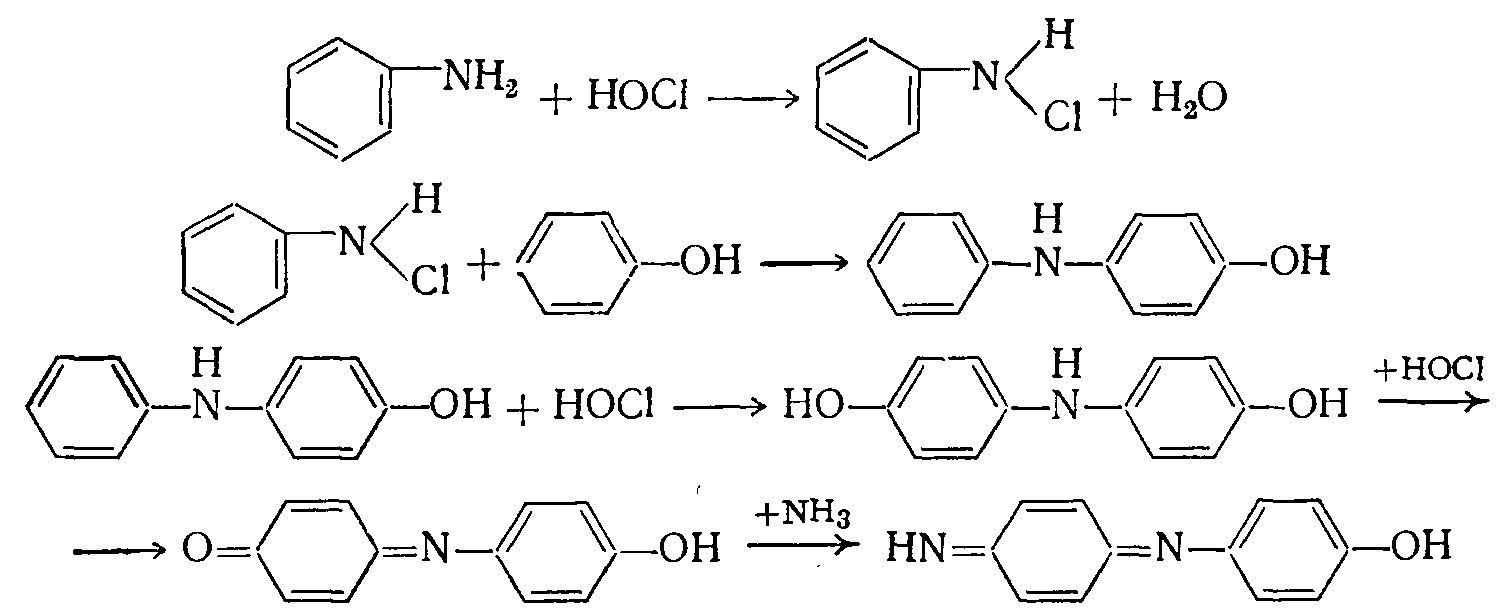
Реакция высокочувствительная и используется для определения анилина в воздухе промышленных предприятий.
Количественное определение
Анилин переводят в 2, 4, 6-триброманилин или анилин переводят в азокраситель красно-оранжевого цвета по первичной ароматической аминогруппе анилина. Определяют фотоэлектроколориметрически или спектрофотометрически со стандартным образцом или по калибровочному графику.
43. Метод изолирования подкисленным спиртом. Его достоинства и недостатки.
Изолирование этанолом, подкисленным щавелевой кислотой (метод Стаса-Отто)
В 1851 году во Франции произошло насильственное отравление Гюстава Фугни никотином. Он стал жертвой собственной сестры Лидии Фугни и ее мужа - графа Бокарме, которые совершили это преступление в погоне за наследством. Исследование внутренних органов погибшего было поручено бельгийскому химику Ж.С. Стасу, который применил для изолирования яда этанол, подкисленный щавелевой кислотой. Последующее извлечение алкалоида из водной фазы (после добавления гидроксида аммония для переведения его соли в основание) проводилось эфиром. В 1856 году братья Юлий и Роберт Ф. Отто ввели в метод Стаса еще одну операцию - очистку извлечения, исследуемого на алкалоиды путем экстрагирования примесей эфиром из кислой водной вытяжки. В дальнейшем метод изолирования подкисленным спиртом, названный по имени авторов методом Стаса-Отто претерпел серьезные изменения и стал применяться не только для алкалоидов, но и для многих других ядовитых и сильнодействующих веществ, имеющих токсикологическое значение.
Современная модификация метода состоит из этапов:
• Настаивание измельченного объекта с этиловым спиртом, подкисленным щавелевой кислотой до рН2-3 в течение суток. Спирт берется в количестве, необходимом для покрытия объекта. Спиртовое извлечение сливается, и вся операция повторяется трехкратно;
• Упаривание объединенных спиртовых извлечений при температуре 40-50°С до густого остатка, в который по каплям добавляют абсолютный этанол для коагуляции белков. Осадок отфильтровывают и всю операцию осаждения повторяют по мере необходимости до полного удаления белковых соединений;
• Упаривание фильтрата при той же температуре до густого остатка и разбавление горячей водой для удаления смолистых веществ жиров и пигментов. Осадок отфильтровывают;
• Экстрагирование веществ кислого, нейтрального и слабоосновного характера из водного фильтрата хлороформом при рН=2 (трехкратная экстракция), отделение органической фазы и концентрирование полученного извлечения упариванием (фракция А, «кислое» извлечение);
• Подщелачивание оставшегося после разделения фаз водного слоя до рН 9-10, экстрагирование веществ сильноосновного и нейтрального характера (трехкратная экстракция) хлороформом, отделение органической фазы и концентрирование упаривание (фракция Б, «щелочное» извлечение);
Изолирование «нелетучих» ядов из биологического материала подкисленным спиртом (метод Стаса-Отто) проводится по следующей схеме:

Достоинства метода заключаются в следующем:
1) Метод универсален, т. к. этанол является хорошим растворителем для многих веществ этой группы (как ионизированных так и молекулярных форм);
2) Метод предусматривает очистку извлечения от балластных веществ, в результате чего получаются чистые хлороформные извлечения, не дающие эмульсий при экстрагировании веществ из водной фазы хлороформом. Метод дает возможность изолировать до 30% барбитуратов и 20-25% алкалоидов;
К недостаткам метода следует отнести:
1) Длительность (8-10 рабочих дней) и многостадийность;
2) Большое количеств операций, связанных с осаждением белков и
фильтрованием ведет к значительным потерям искомых веществ (алкалоиды
теряются на 25-50%);
3) Сравнительная дороговизна метода ( на 1 исследование тратится до 500 мл этанола);
Все это приводит к тому, что классический метод Стаса-Отто теряет свое былое значение и постепенно заменяется более быстрыми эффективными и экономными методами извлечения подкисленной водой.
В настоящее время метод применяется главным образом для исследования гнилостно измененного биологического материала.
