
- •Общие закономерности реакций полимеризации
- •Полимеры непредельных ароматических ув
- •Производство аминоальдегидных полимеров.
- •Анилиноформальдегидные полимеры
- •Общие закономерности реакции поликонденсации
- •Полиэтилен высокого давления (низкой плотности)
- •Производство полиакрилонитрила в водных р-рах минеральных солей
- •3 Билет
- •2. Производство пэнд (вп). Особенности структуры и свойств.
- •3. Технология получения пан в дмфа.
- •4 Билет
- •1. Полипропилен и полиизобутилен. Производство, свойства, применение.
- •2. Пв карбазол, пв пиридин.
- •3. Фенопласты, получение полимерных материалов из новолачных и резольных пресс-порошков.
- •Поливинилхлорид. Свойства. Применение.
- •Технология производства пэнд (вп) в жидкой фазе.
- •Особенности процессов синтеза фенолоальдегидных полимеров.
- •Билет№6
- •Сополимеры винилхлорида. Получение и свойства винипласта, пластиката, вспененного поливинилхлорида.
- •Производство суспензионного полистирола.
- •Пресс материалы с волокнистыми наполнителями.
- •Вопрос 1: птфэ.
- •Вопрос2: Полик-ция в кислой и щелочной среде фенола с формальдегидом, получение новолачных и резольных олигомеров на основе фенола и альдегидов.
- •Вопрос 3: Пресс-материалы с листовым наполнителем.
- •Вопрос 1: Акриловые полимеры: получение, свойства.
- •Вопрос 2: Производство пвх (суспенз., эмульсионным способом и в р-ре).
- •Вопрос 3: Полимеры на основе формальдегида и гомологов фенола.
- •Вопрос 1: пан
- •Вопрос 2: Ионно-координационная полим-ция
- •Вопрос 3: Производство полиэтилена высокого давления в автоклаве с мешалкой
- •Вопрос 2: Пластмассы и лакокрасочные мат-лы на основе меламиноформальдегидных олигомеров (МлФо)
- •1. Простые полиэфиры, полиформальдегид, сополимеры фа.
- •2. Способы проведения поликонденсации
- •3. Технология производства пс суспензионным способом.
- •1. Полиакриленоксиды, пентомпласт.
- •2. Равновесная и неравновесная поликонденсация.
- •3. Полиуретан.
- •Вопрос 1: Способы проведения поликонденсации
- •Вопрос 2: Акриловые полимеры: получение, свойства.
- •3. Технология получения новолачных ффо (рис. 23, 24)
- •Вопрос 1. Общие закономерности реакций поликонденсации
- •Вопрос 2: пс. Получение, свойства
- •Вопрос 3: Технология получения пэвд в трубчатом реакторе (рис.1)
- •Вопрос 1: Поликонденсация фенола с фа.
- •Вопрос 2: Сополимеры вх
- •Вопрос 3: Производство полиэтилена высокого давления в автоклаве с мешалкой
- •Вопрос 1: Ионно-координационная полим-ция
- •Вопрос 2: Технология получения пвх
- •Вопрос 3: Пентапласт [поли-3,3-бис(хлорметил)оксациклобутан]
- •Вопрос 1: Кумароно-инденовые полимеры
- •Вопрос 2: Технология производства пэвд в автоклаве с мешалкой
- •3. Поликонденсация в кислой среде
- •Вопрос 3: Отверждение ффо
- •Вопрос 1: пэСрД
- •Вопрос 2: Сополимеры тфэ
- •Вопрос 3: Получение резольных олигомеров на основе фенола и формальдегида
- •Вопрос 1: птфэ.
- •2. Производство эмульсионного пвх.
- •3. Карбамидоформальдегидные полимеры
- •Вопрос 1: Способы проведения полимеризации
- •Вопрос 2: Меламиноформальдегидные олигомеры
- •Вопрос 3: пмма: технология получения, свойства, применение
Особенности процессов синтеза фенолоальдегидных полимеров.
В результате взаимодействия фенола с альдегидами образуются олигомеры и полимеры, строение которых зависит от функциональности использованного фенола, типа альдегида, мольного соотношения реагентов и рН реакционной среды. При этом образуются либо линейные (или слабо разветвленные) термопластичные продукты, которые называются новолаками либо сильно разветвленные термореактивные олигомеры, названные резолами.
В фенолах реакционноспособными являются атомы водорода, находящиеся в орто- и пара-положениях к гидроксильной группе. Поэтому из одноатомных фенолов трифункциональными являются фенол, м-крезол и 3,5-ксиленол, а из двухатомных — резорцин:
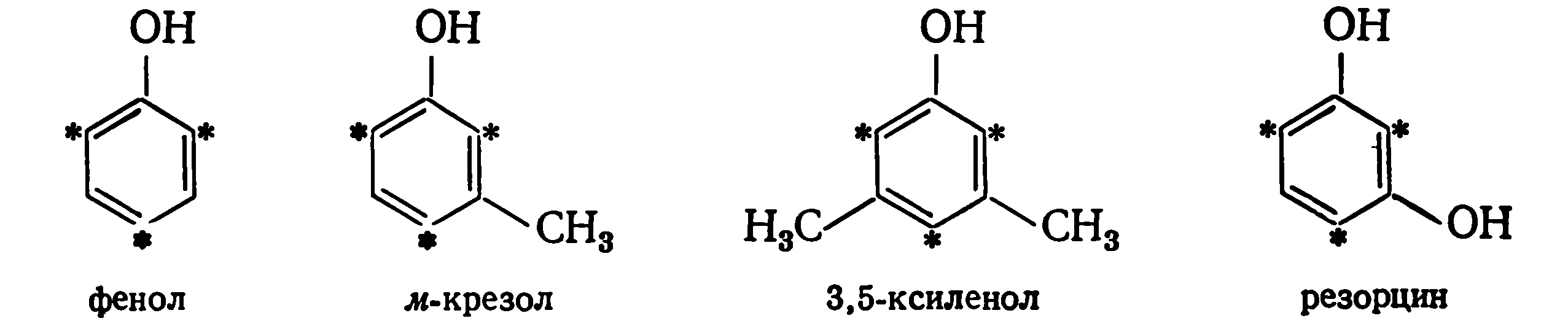
К бифункциональным относятся фенолы с заместителем в орто-. или пара-положении — о- и п-крезолы 2,3-, 2,5- и 3,4-ксиленолы:
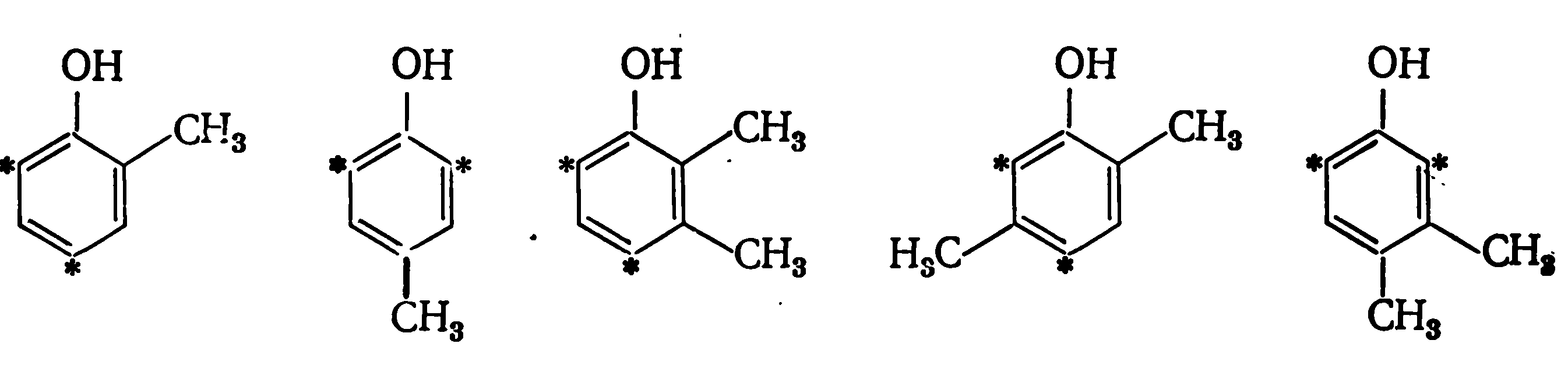
2,6- и 2,4-Ксиленолы — монофункциональны.
При поликонденсации формальдегида и фурфурола с трифункциональными фенолами могут получаться как термопластичные, так и термореактивные олигомеры. Бифункциональные фенолы образуют только термопластичные олигомеры.
Из альдегидов лишь формальдегид и фурфурол способны образовывать термореактивные олигомеры при поликонденсации с трифункциональными фенолами. Другие альдегиды (уксусный, масляный и т. д.) вследствие пониженной химической активности и пространственных затруднений не образуют термореактивных олигомеров.
Термопластичные (новолачные) олигомеры образуются в следующих случаях:
а) при избытке фенола (соотношение фенол : формальдегид 1:0,78—0,86) в присутствии кислотных катализаторов; при отсутствии избытка фенола образуются резольные олигомеры;
б) при большом избытке формальдегида (соотношение фенол: формальдегид 1 :2—2,5) в присутствии сильных кислот в качестве катализатора; получаемые в этом случае олигомеры не отверждаются при нагревании, но при добавлении к ним небольшого количества оснований переходят в неплавкое и нерастворимое состояние.
Термореактивные (резольные) олигомеры образуются в следующих случаях:
а) при поликонденсации избытка трифункционального фенола с формальдегидом в присутствии основных катализаторов (в щелочной среде термореактивные олигомеры получаются даже при очень большом избытке фенола, который в этом случае остается растворенным в продукте реакции);
б) при небольшом избытке формальдегида в присутствии как основных, так и кислотных катализаторов.
Особенностью взаимодействия фенолов с формальдегидом является использование формальдегида главным образом в виде водных растворов. Такой раствор имеет сложный состав вследствие протекания следующих обратимых реакций:
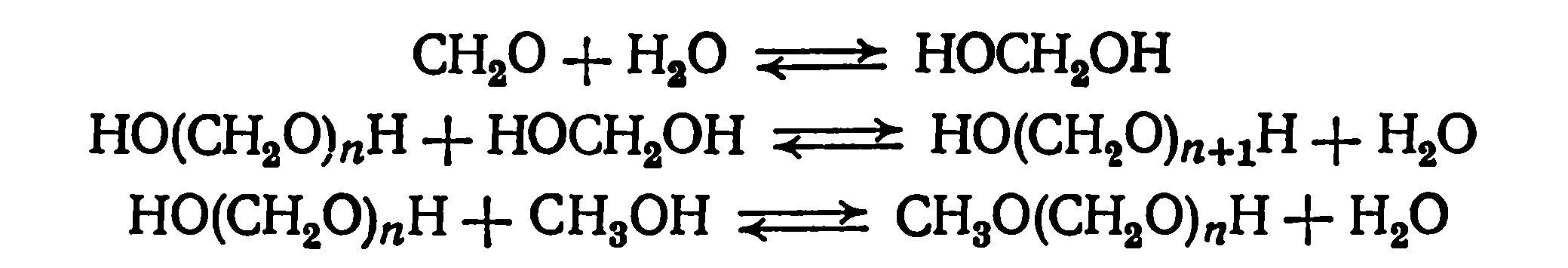
Кинетика и механизм процесса образования фенолоформальдегидных олигомеров определяются типом используемого катализатора. В присутствии кислот реакция протекает следующим образом:
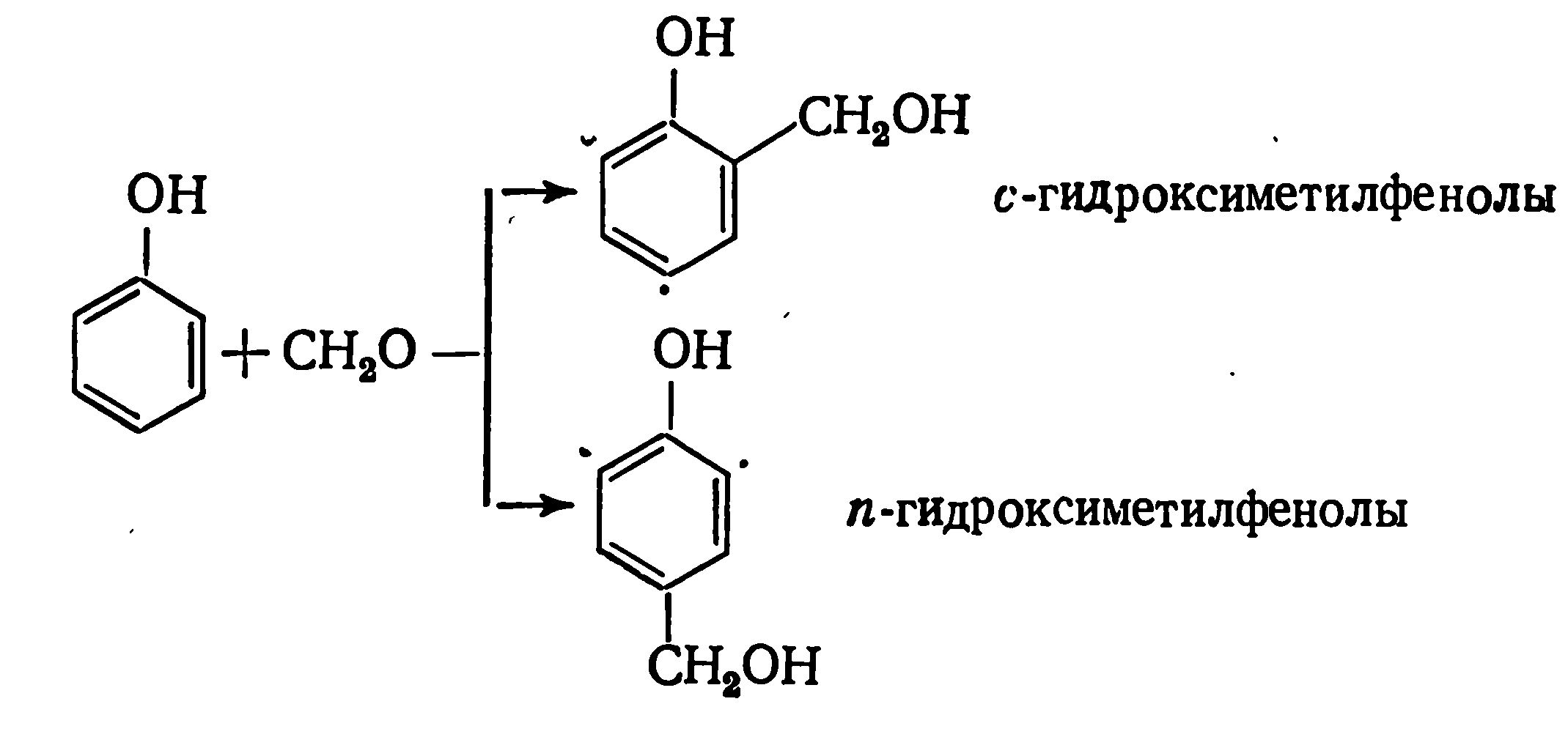
Вначале
эти соединения образуются примерно, в
равных количествах, затем вследствие
более высокой реакционной способности
доля пара-изомера
становится
меньше.По мере протекания конденсации
образуются 4,4'- и 2,4'-дигидроксидифенилметаны,
а затем в меньшем количестве
2,2'-ди-гидроксидифенилметан.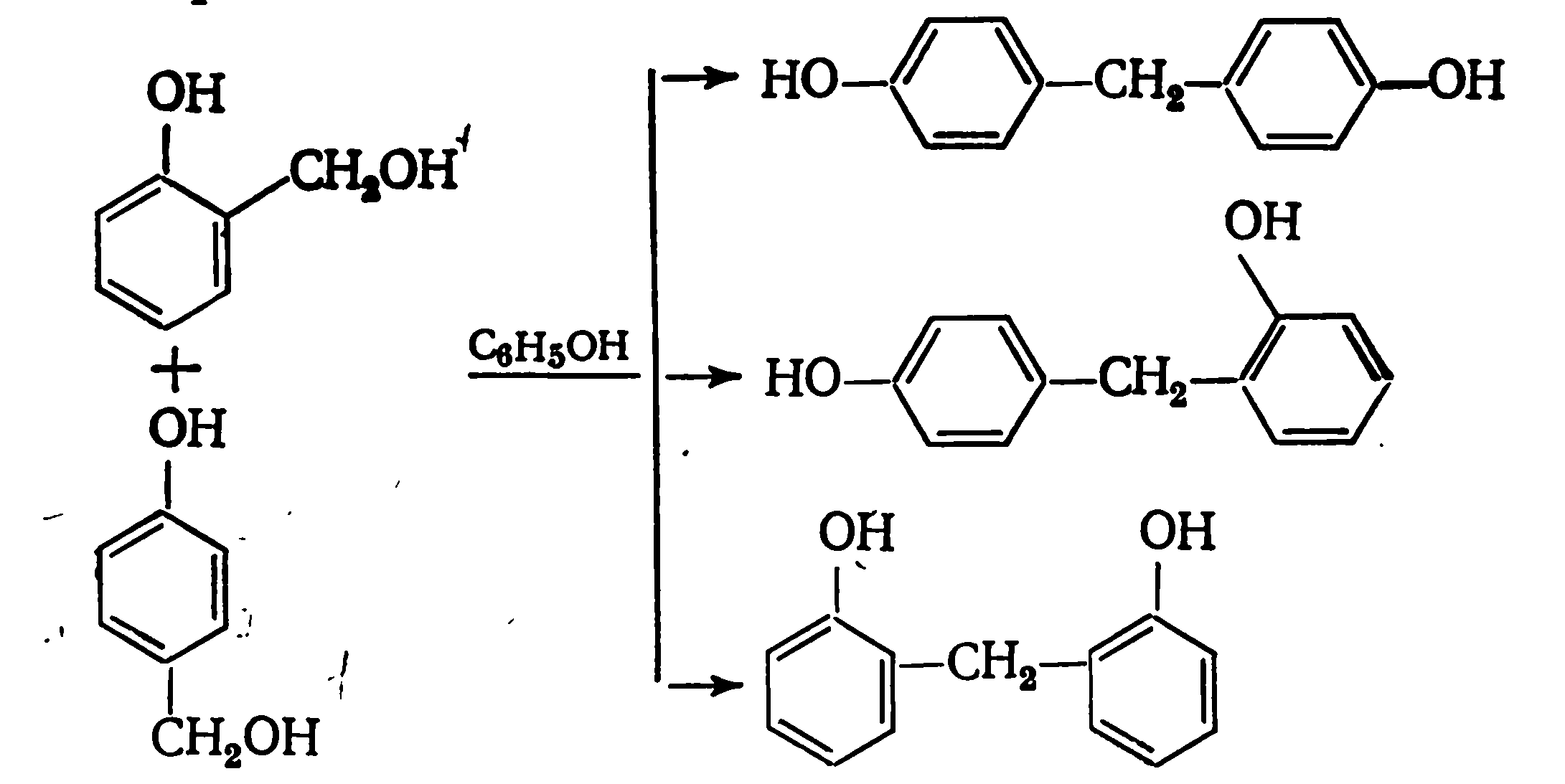
При
этом в продуктах поликонденсации почти
отсутствуют ди- и тригидроксиметилфенолы
и дигидроксидибензиловые эфиры.
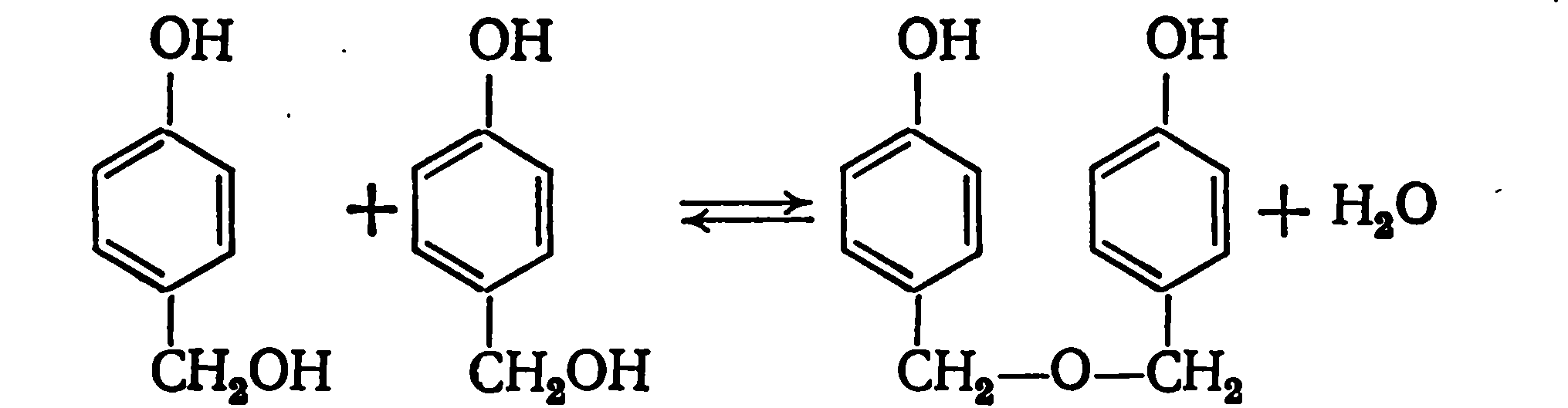
Последние образуются при взаимодействии гидроксиметильных производных фенола друг с другом. Малая конц-ция этих соединений в реакционной массе объясняется их низкой стойкостью. Дигидроксидибензиловые эфиры разлагаются с выделением формальдегида:
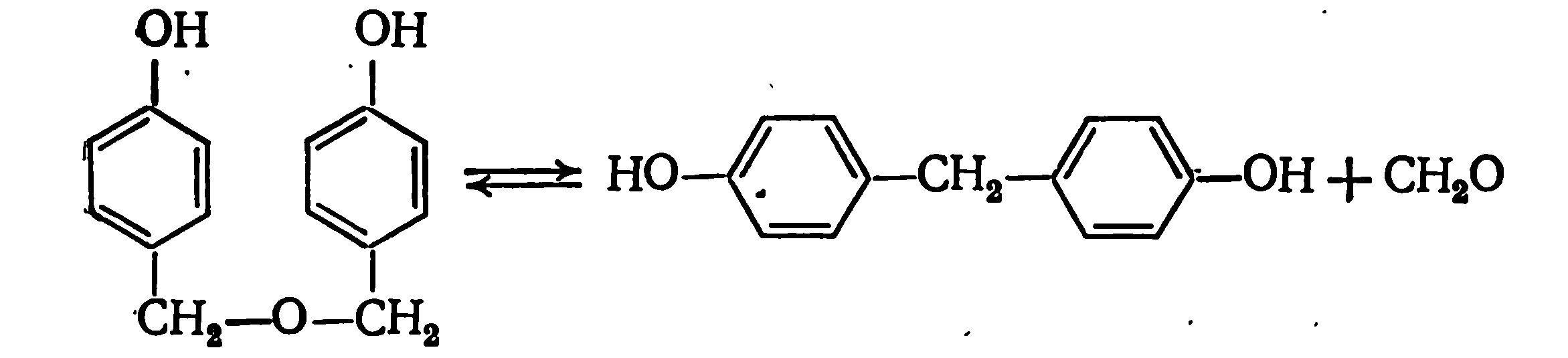
Кроме того возможен фенолиз дигидроксидибензиловых эфиров (К=2-1010 при 25°С), в результате которого образуется смесь продуктов, содержащая о-гидроксиметилфенол, 2,2'- и 2,4'-ди- гидроксидифенилметаны, а также трех- и четырехядерные мономеры с метиленовыми связями.
Как видно из значений констант равновесия, образование метиленового мостика между фенильными ядрами термодинамически намного выгоднее, чем мостика —СН2ОСН2—. В обычных условиях синтеза фенолоформальдегидных олигомеров, при использовании формальдегида в виде водных растворов, образование дигидроксидибензиловых эфиров практически невозможно.
При использовании орто-замещенных производных фенола соответствующие ортоизомеры дополнительно стабилизируются за счет образования внутримолекулярной водородной связи:
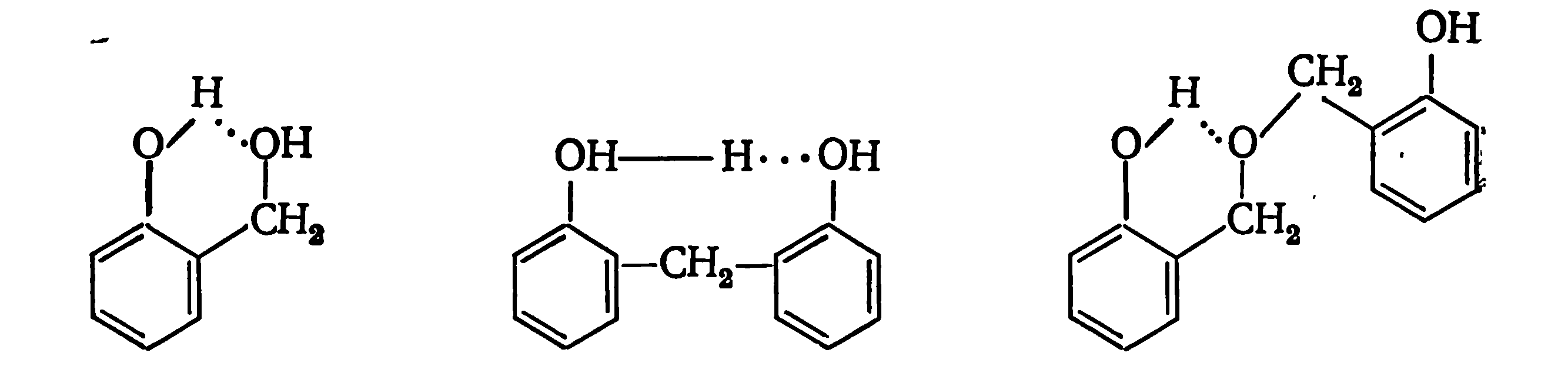
На последующих стадиях химического процесса, происходит взаимодействие моногидроксиметильных производных фенола с дигидроксидифенилметанами. Скорость реакций присоединения и конденсации по незамещенным орто- положениям новолачного олигомера мало зависит от молекулярной массы, т. е. все свободные орто-положения имеют равную реакционную способность. Увеличение конверсии мономеров приводит к разделению реакционной массы на два слоя: водный и олигомерный, после чего реакция продолжается в гетерогенной системе. Наличие в феноле трех реакционноспособных групп создает предпосылки для изомерии фенолормальдегидных олигомеров. Реакционная способность этих положений зависит от природы катализатора и температуры. В условиях обычных для получения новолачных олигомеров (катализатор — кислота, рН= 0—2, 37%-ный раствор формалина, температур а около 100 °С) незамещённые пара-положения фенольных звеньев и пара-гидроксиметильные группы значительно активнее соответствующих орто-положений и орто-гидроксиметильных групп.
Скорость реакций по орто-положениям возрастает с увеличением рН и температуры. Изомерный состав продуктов поликонденсации в водном растворе мало зависит от природы кислоты. В случае проведения поликонденсации в органических растворителях (этиловый спирт, толуол, тетрахлорэтан) доля орто-замещения снижается в ряду кислот: уксусная > щавелевая > бензолсульфокислота > соляная. В процессе получения фенольных олигомеров образуются линейные и разветвленные продукты.
