
- •1. Методи отримання полімерних матеріалів.
- •4.2. Технологія отримання карбамидоформальдегидных олигомеров.
- •4.3. Поліконденсация карбаміду і формальдегіду в кислій середі.
- •4.3.1.Структура і властивості полиметиленкарбамида.
- •4.3.3. Закономірності утворення твердої фази полиметиленкарбамида.
- •4.3.4.Модифікація полиметиленкарбамида.
- •4. 3.5. Морфологія полиметиленкарбамида.
- •4.3.6. Деякі основні сфери застосування пмм.
- •5.2. Будова карбамидоформальдегидных смол.
- •5. 3. Вплив технологічних чинників на будову кфс.
- •5.4. Вплив технологічних чинників на зміст вільного f.
- •Зниження змісту вільного формальдегіду в кфс шляхом використання акцепторів формальдегіду.
- •5.5.1. Зниження токсичності кфс за рахунок введення в її склад
- •Зниження токсичності кфс за рахунок використання амінів і амидов карбонових кислот як акцептори формальдегіду.
- •Екологічно чистий спосіб отримання карбамидоформальдегидных олигомеров.
- •6.1. Отримання карбамідів олигомеров з диметилолмочевины.
- •6.2. Отримання карбамидоформальдегидных олигомеров з концентрату карбмидо-формальдегидного (форконденсата).
- •7. Модифіковані мочевиноформальдегидные полімери і матеріали на їх основі
- •8. Очищення стічних вод виробництва карбамидоформальдегидных смол.
- •8.1. Біохімічні методи очищення стічних вод від формальдегіду.
- •8. 2. Физико-хімічні методи очищення стічних вод.
- •8.3. Хімічні методи очищення стічних вод, що містять формальдегід.
- •9. Полімери меламино-формальдегидные
- •10. Полімери анилино-формальдегидные
- •11.Техніка безпеки при виробництві амино-альдегидных олигомеров і пластичних мас на їх основі
- •12. Феноло-альдегидные полімери
- •12. 1. Сировина для отримання фенолоальдегидных полімерів
- •12. 2. Особливості процесів синтезу фенолоальдегидных полімерів
- •12. 3. Каталізатори процесів отримання фенолформальдегидных олигомеров.
- •12. 4. Технологія отримання новолачных олигомеров
- •12.4.1 Властивості новолачных олигомеров і полімерів
- •12.5. Виробництво резольних олигомеров
- •12.5.1. Властивості резольних олигомеров і полімерів
- •12.6. Полімери на основі гомологов фенолу і формальдегіду
- •12.6.1. Феноло-фурфурольниє полімери
- •12.6.2. Полімери Феноло-лигниновые
- •12.7. Модифіковані полімери феноло-формальдегидные
- •12.7.1. Маслорастворімиє полімери феноло-формальдегидные
- •12.7.2. Поєднані полімери
- •12.8. Полімери резорцино-формальдегидные
- •12.8.1. Обесфеноліваніє водної фази
12. 2. Особливості процесів синтезу фенолоальдегидных полімерів
При поликонденсации фенолу і його гомологов з альдегідами можуть утворюватися як термопластичные, так і термореактивные продукти. Стосовно фенолоальдегидным полімерів термопластичные продукти називають новолачными (або новолаками), а термореактивные — резольними (або резолами).
Основними чинниками, що визначають будову і властивості фенолоальдегидных полімерів, є функціональність фенолу, молярне співвідношення фенол: альдегід і рН реакційної середи.
Залежно від хімічної будови феноли володіють різною функціональністю, під якою розуміють число атомів водню у фенолі або його гомологах, здатних взаємодіяти з альдегідами. У фенолах реакционноспособными є атоми водню, що знаходяться в орто- і пара-положении до гідроксильної групи. Тому з одноатомних фенолів трифункциональными є фенол, л-крезол і 3,5-ксиленол, а з двоатомних — резорцин:
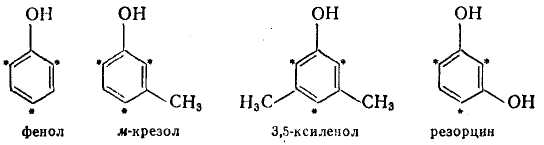
До біфункціональних відносяться феноли із заступником в орто-или пара-положении: о- і п-крезолы; 2,3-, 2,5- і 3,4-ксиленолы:
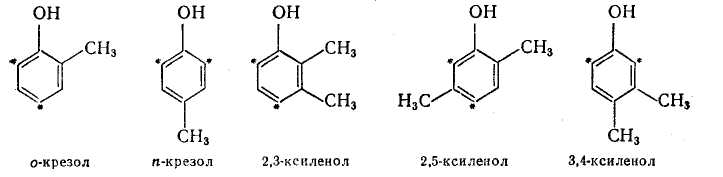
Інші ксиленолы (2,6- і 2,4-) монофункциональны.
При поликонденсации формальдегіду або фурфурола з три-функциональными фенолами можуть бути отримані як термопластичные, так і термореактивные олигомеры. Біфункціональні феноли утворюють тільки термопластичные олигомеры.
З альдегідів лише формальдегід і фурфурол здатні утворювати термореактивные олигомеры при поликонденсации з трифункциональными фенолами. Інші альдегіди (оцетовий, масляний і т. д.) унаслідок зниженої хімічної активності і просторових утруднень термореактивных олигомеров не утворюють.
При взаємодії трифункциональных фенолів з формальдегідом термопластичные (новолачные) олигомеры утворюються а наступних випадках:
а) при надлишку фенолу (співвідношення фенол: формальдегід 1: 0,78—0,86) у присутності кислотних каталізаторів; за відсутності надлишку фенолу утворюються резольні олигомеры;
б) при великому надлишку формальдегіду (співвідношення фенол : формальдегід 1 : 2—2,5) у присутності сильних кислот як каталізатор; отримувані в цьому випадку олигомеры не отверждаются при нагріванні, але при додаванні до них невеликої кількості підстав швидко переходять в неплавкий і нерозчинний стан.
Термореактівниє (резольні) олигомеры утворюються в наступних випадках:
а) при поликонденсации надлишку трифункционального фенолу з формальдегідом у присутності основних каталізаторів. У лужній середі термореактивные олигомеры виходять навіть при дуже великому надлишку фенолу, який в цьому випадку залишається розчиненим в продукті реакції;
б) при невеликому надлишку формальдегіду у присутності як основних, так і кислотних каталізаторів.
Реакції отримання новолачных і резольних олигомеров дуже складні і до цих пір вивчені не повністю. Вони протікають з утворенням великого числа ізомерних проміжних продуктів, які, як правило, є нестійкими і зазнають I подальші перетворення.
Початковими продуктами при синтезі як новолачных, так і резольних олигомеров є фенолоспирты, приєднання формальдегіду, що утворюються в результаті, у вільні орто- і пару-положення молекули фенолу (реакція оксиметилирования).
При отриманні новолаков (зазвичай поликонденсацией надлишку фенолу з формальдегідом у присутності кислотного каталізатора) такими початковими продуктами є переважно одноатомні фенолоспирты (монометилолфенолы), головним чином о-оксибензиловый спирт (салигенин) і у меншій мірі п-оксибензиловый:
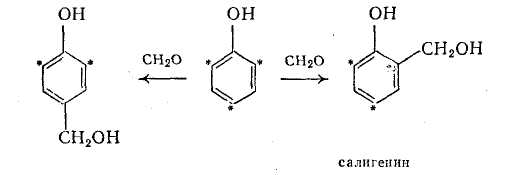

Метілольная група Сн2 ВІН, що міститься в молекулі окси-бензилового спирту, здатна вступати в реакцію з активним атомом водню іншої молекули оксибензилового спирту або фенолу. В результаті реакції конденсації, що протікає з відщеплюванням води, утворюються складніші молекули, в яких фенолові ядра зв'язані метиленовыми містками. При цьому в результаті поликонденсации молекул оксибензилового спирту утворюються новолачные олигомеры лінійної будови — салигниновые олигомеры, а при конденсації з фенолом – ізомерні диоксидифенилметаны:
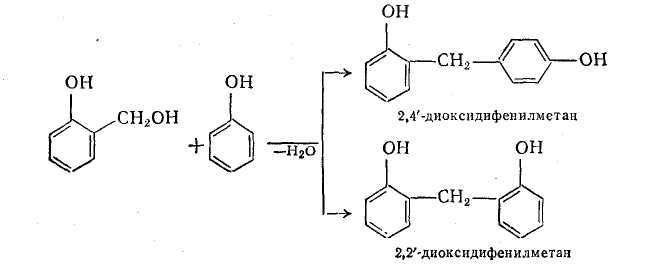
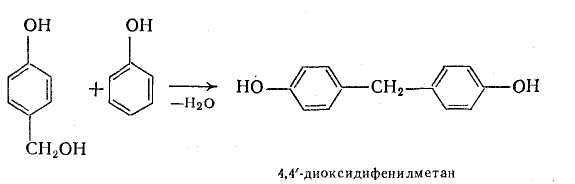
В результаті їх подальшої реакції з формальдегідом і фенолом виходять новолачные олигомеры розгалуженої будови, в яких метиленовые містки знаходяться в орто- і пара-положении до фенолових гидроксилам:
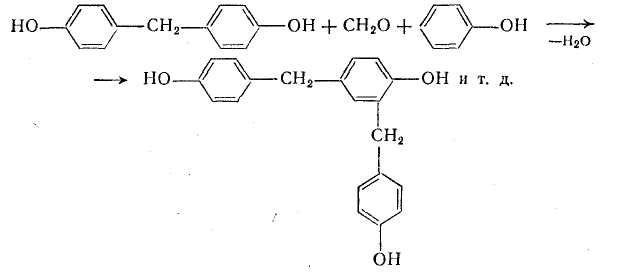
Фенолові гидроксилы не беруть участь в реакції поликонденсации, а ефірні групи Сн2—о—сн2, які утворюються при взаємодії два метилольных груп, майже відсутні в молекулах олигомеров.
У спільному вигляді синтез новолака може бути представлений наступною схемою:
![]()
Новолаки є сумішшю полимергомологов з великим розкидом молекулярних вагів окремих фракцій. Середня молекулярна вага новолачных олигомеров порівняно невелика (зазвичай від 600 до 1300) і залежить від тривалості поликонденсации і молярного співвідношення фенол: формальдегід. При зменшенні молярної частки фенолу в суміші компонентів молекулярна вага олигомера збільшується.
У молекулах новолаков, отриманих з трифункционального фенолу або суміші фенолів, що містить хоч би один трифункциональный фенол, ще залишаються активні атоми водню в орто- і пара-положениях до фенолових гидроксилам. Тому при обробці їх формальдегідом із заміною кислотного каталізатора основним можна отримати резол або неплавкий
і нерозчинний полімер — резит. Резіт виходить також при дії на новолак полімерів формальдегіду (параформ, а-полиоксиметилен, р-полиоксиметилен) або гексаметилентетрамина. У останньому випадку, мабуть, в процесі отверждения беруть участь ди- і триметиламины, що утворюються при розкладанні гексаметилентетрамина, а аміак, що виділяється, грає роль каталізатора.
Новолаки, отримані з біфункціональних фенолів (о- і п-крезолов), при обробці формальдегідом не переходять в неплавкий і нерозчинний стан. Проте, якщо такі олигомеры нагрівати вище 180 °С, вони здатні переходити, хоча і повільно, в неплавкий і нерозчинний стан. То ж спостерігається при 250—280 °С і для новолаков, що отримуються поликонденсацией 1 міль фенолу з 0,8 міль формальдегіду, що можна пояснити активацией атомів водню в мета-положении до фенолових гидроксилам або взаємодією останніх з освітою ефірних зв'язків.
При синтезі резолів на початку реакції разом з о- і п-оксибензиловыми спиртами утворюються ди- і триметилолфенолы:

Освіті їх сприяють надлишок формальдегіду і лужна середа, в якій переважає реакція оксиметилирования, а конденсація відбувається у меншій мірі. Але навіть при эквимолярном співвідношенні фенол: формальдегід в лужній середі на 1 міль фенолу, що прореагував, зв'язується до 1,5 міль формальдегіду і утворюється суміш фенолоспиртов.
При підвищеній температурі фенолоспирты вступають в реакцію конденсації один з одним з утворенням резольних олигомеров, тобто метилольных похідних полиметиленфенолов:
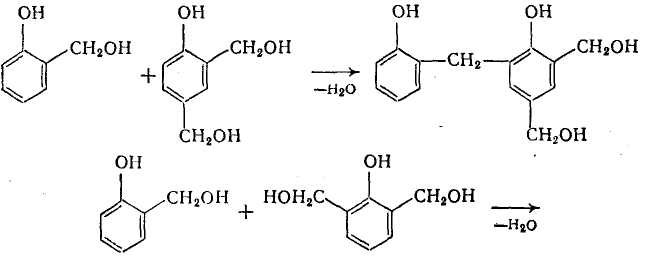
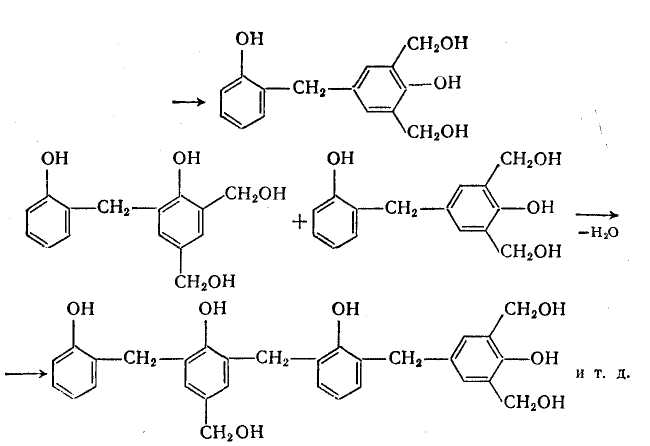
Молекулярна вага резолів (від 400 до 800—1000) нижча, ніж новолачных олигомеров, оскільки для запобігання гелеобразования поликонденсацию проводять швидко. При нагріванні резоли поступово отверждаются, тобто перетворюються на полімери просторової будови. В процесі отверждения резольних олигомеров розрізняють три стадії.
У стадії А, званою також резольною, олигомер по своїх фізичних властивостях аналогічний новолачному олигомеру, оскільки так само, як і новолак, він плавиться і розчиняється в лугах, спирті і ацетоні. Але на відміну від новолака резолом є нестійкий продукт.
Резоли є сумішшю лінійних і розгалужених продуктів спільної формули:
![]()
У стадії В полімер, званий резитолом, лише частково розчиняється в спирті і ацетоні, не плавиться, але ще зберігає здатність при нагріванні переходити у високоеластичне, каучукоподобное стан (здатність розм'якшуватися) і набухати в розчинниках.
У стадії З — кінцевій стадії отверждения — полімер, званий резитом, є неплавкий і нерозчинний продукт, що не розм'якшується при нагріванні і не набухає в розчинниках.
Перехід полімеру в неплавкий і нерозчинний стан є наслідком утворення просторової сітки за рахунок скріплення полімерних ланцюгів метиленовыми містками.
Будову резита можна представити таким чином:
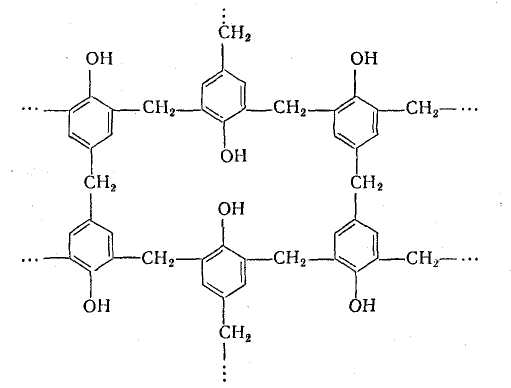
У отвержденном полімері ще залишається деяка кількість вільних метилольных груп, які при подальшій тривалій термообробці реагують з утворенням хімічних зв'язків.
Метілольниє групи, що знаходяться в орто- і пара-положениях до фенолового гидроксилу, володіють різною стабільністю. По теорії Хулче, найбільш стабільні групи в орто-положении, що пояснюється утворенням шестичленних кілець за рахунок водневого зв'язку:
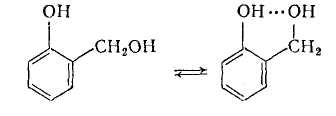
При нагріванні цей зв'язок руйнується. Метілольниє групи, що знаходяться в пара-положении, не беруть участь в утворенні водневих зв'язків, тому вони менш стабільні і при підвищенні температури насамперед вступають в реакцію поликонденсации.
