
- •1. Методи отримання полімерних матеріалів.
- •4.2. Технологія отримання карбамидоформальдегидных олигомеров.
- •4.3. Поліконденсация карбаміду і формальдегіду в кислій середі.
- •4.3.1.Структура і властивості полиметиленкарбамида.
- •4.3.3. Закономірності утворення твердої фази полиметиленкарбамида.
- •4.3.4.Модифікація полиметиленкарбамида.
- •4. 3.5. Морфологія полиметиленкарбамида.
- •4.3.6. Деякі основні сфери застосування пмм.
- •5.2. Будова карбамидоформальдегидных смол.
- •5. 3. Вплив технологічних чинників на будову кфс.
- •5.4. Вплив технологічних чинників на зміст вільного f.
- •Зниження змісту вільного формальдегіду в кфс шляхом використання акцепторів формальдегіду.
- •5.5.1. Зниження токсичності кфс за рахунок введення в її склад
- •Зниження токсичності кфс за рахунок використання амінів і амидов карбонових кислот як акцептори формальдегіду.
- •Екологічно чистий спосіб отримання карбамидоформальдегидных олигомеров.
- •6.1. Отримання карбамідів олигомеров з диметилолмочевины.
- •6.2. Отримання карбамидоформальдегидных олигомеров з концентрату карбмидо-формальдегидного (форконденсата).
- •7. Модифіковані мочевиноформальдегидные полімери і матеріали на їх основі
- •8. Очищення стічних вод виробництва карбамидоформальдегидных смол.
- •8.1. Біохімічні методи очищення стічних вод від формальдегіду.
- •8. 2. Физико-хімічні методи очищення стічних вод.
- •8.3. Хімічні методи очищення стічних вод, що містять формальдегід.
- •9. Полімери меламино-формальдегидные
- •10. Полімери анилино-формальдегидные
- •11.Техніка безпеки при виробництві амино-альдегидных олигомеров і пластичних мас на їх основі
- •12. Феноло-альдегидные полімери
- •12. 1. Сировина для отримання фенолоальдегидных полімерів
- •12. 2. Особливості процесів синтезу фенолоальдегидных полімерів
- •12. 3. Каталізатори процесів отримання фенолформальдегидных олигомеров.
- •12. 4. Технологія отримання новолачных олигомеров
- •12.4.1 Властивості новолачных олигомеров і полімерів
- •12.5. Виробництво резольних олигомеров
- •12.5.1. Властивості резольних олигомеров і полімерів
- •12.6. Полімери на основі гомологов фенолу і формальдегіду
- •12.6.1. Феноло-фурфурольниє полімери
- •12.6.2. Полімери Феноло-лигниновые
- •12.7. Модифіковані полімери феноло-формальдегидные
- •12.7.1. Маслорастворімиє полімери феноло-формальдегидные
- •12.7.2. Поєднані полімери
- •12.8. Полімери резорцино-формальдегидные
- •12.8.1. Обесфеноліваніє водної фази
Зниження змісту вільного формальдегіду в кфс шляхом використання акцепторів формальдегіду.
З літературних джерел відомо, що F вступає в реакції з багатьма органічними і неорганічними сполуками. Теоретично більшість відомих реакцій F можуть бути використані для зниження його змісту в КФС. При виборі акцепторів F необхідно враховувати оборотність реакцій і стійкість продуктів, що утворюються. Акцептори повинні реагувати з (F) швидко і необоротно, у відсутності сильних кислот, підстав і окислювачів, які здатні руйнувати КФС або викликати передчасне їх отверждение. Крім того, добавки і продукти їх взаємодії з (F) повинні добре поєднуватися з КФС.
5.5.1. Зниження токсичності кфс за рахунок введення в її склад
ацетилацетона і аміаку.
Реакція ацетилацетона з формальдегідом описана в літературі і відома під назвою реакції Ганча [211, 212].
O O O O
 || || || ||
|| || || ||
2 Сн3 – З – Сн2 – З + CH2O + NH3 ( H3C – C C – CH3
| (28)
CH3 H3C NH CH3
Встановлено, що введення до складу смоли КФ-МТ – 15 із змістом вільного формальдегіду до 0,25 мас %, ацетилацетона і аміаку при їх молярному співвідношенні 2: 1 до 1 молю формальдегіду з розрахунку на вміст його в смолі, викликає повне скріплення останнє. Спостереження за зразками смоли з додаванням ацетилацетона і аміаку протягом 9 діб показали, що формальдегід у вільному стані у складі смоли був відсутній. У контрольних зразках зміст вільного формальдегіду коливався в межах 0,12 – 0,3 мас %.
Дослідження показали, що після додавання ацетилацетона і аміаку смола зазнавала наступні зовнішні зміни: протягом 30 мін після введення добавок з'явилося оранжево-жовте забарвлення, характерне для 2,6, – диацетил – 3,5 – диметил – 4- гидропиридина.. Впродовж 9 діб зберігання смоли відбувалося досить швидке наростання в'язкості до 150 з (мал. 4.1, крива I). Подальше використання смоли такої в'язкості було б неможливе, в той час, коли в'язкість контрольного зразка за цей же час залишалася практично незмінною (мал. 4.1, крива IV). Введення в смолу аміаку в кількості об 1,5 міль на 1 міль ацетилацетона Така концентрація аміаку підвищує життєздатність смоли до 29 діб (мал. 4.1, крива II, III). При цьому впродовж всього вказаного часу зміст вільного (F) у складі КФС не виявлено (таблиця. 2.3, приклади 5, 17).
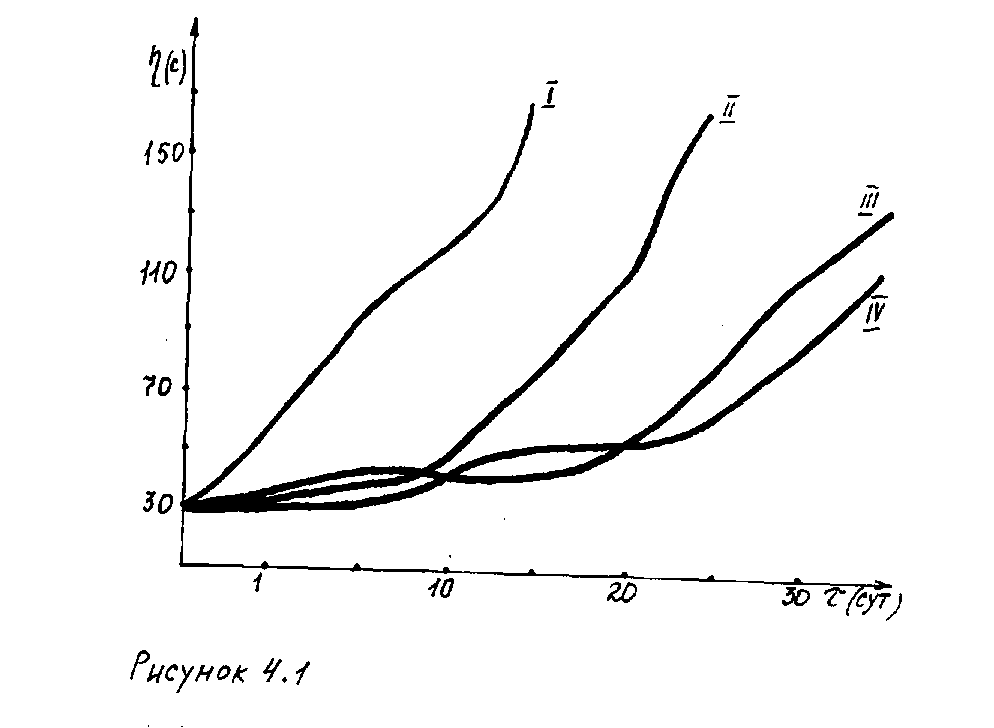
Малюнок 4.1 Залежність в'язкості ( (с) карбамидоформальдегидной смоли від тривалості зберігання ( (сут.). Співвідношення ацетилацетон: аміак (міль : міль) : I – 1 : 0,5, II – 1 : 1, III – 1 : 1,5, IV – контрольний зразок без добавок.
Проте, роль ацетилацетона, ймовірно, не обмежується освітою 2,6–диацетил–3,5–диметил–4 – гидропиридина (( max=410). Наростання в'язкості при введенні добавок може свідчити про взаємодію ацетилацетона з реакційно здатними групами смоли з подальшим впровадженням в полімерний ланцюг. Найбільш вірогідним маршрутом реакції ацетилацетона може бути взаємодія останнього з кінцевими групами смоли по реакції Манніха [213]:
H3C
\
O O O O С= O
|| || || | /
С–nh – CH2OH + CH3 – C – CH2 – C – CH3 ( (C – NH – CH2 – CH+H2O (29)
\
З = O
/
H3C
Ацетілацетон – вельми реакционноспособное речовина в реакціях Манніха [214]. Володіючи декількома активними атомами водню метиленовой і метильных груп, ацетилацетон може вступати в реакції з реакционноспособными групами смоли як поліфункціональний мономер. 2,6-Диацетил-3,5-диметил - 4 - гидропиридин також здатний вступати в реакцію як поліфункціональний мономер по метильным групах, пов'язаних з гетерокольцом і карбонільним атомом вуглецю:
O O O
 || ||
||
|| ||
||
H3C – C – – C – CH3 + 2 (C – NH – CH2OH ( H3C –NH – CH3
O O O O
|| || || |
- C – NH–CH2 – CH2 – C – C – CH2 – CH2 – NH – C - ( + 2 H2O (30)
H3C– NH – H3C
Крім того, згідно реакції Манніха, можливе протікання і інших реакцій 2,6 – диацетил – 3,5 – диметил – 4 – гидропиридина, наприклад, з амино – або иминогруппой заміщеного карбаміду, що міститься у складі КФС, з утворенням продуктів реакції вторинного або третинного аміну.
Тому швидке наростання в'язкості смоли можна пояснити як зростанням молекулярної маси смоли, так і появою у складі смоли поліфункціональних мономерів, здібних до утворення щільнішої сітки фізичних зв'язків.
Підтвердженням припущень є той факт, що, дійсно, при нагріванні смоли з добавками до 1000С у відсутності кислотних каталізаторів протягом декількох хвилин (2–3) відбувається утворення твердого неплавкого полімеру, тоді як контрольний зразок у відсутності кислотних каталізаторів не отверждается.
Отримані результати відкривають можливість отримання КФС, що не містять вільного Сн2о, за допомогою введення в їх склад добавок з достатньо високою реакційною здатністю, зокрема, на основі ацетилацетона і аміаку.
