
- •1. Методи отримання полімерних матеріалів.
- •4.2. Технологія отримання карбамидоформальдегидных олигомеров.
- •4.3. Поліконденсация карбаміду і формальдегіду в кислій середі.
- •4.3.1.Структура і властивості полиметиленкарбамида.
- •4.3.3. Закономірності утворення твердої фази полиметиленкарбамида.
- •4.3.4.Модифікація полиметиленкарбамида.
- •4. 3.5. Морфологія полиметиленкарбамида.
- •4.3.6. Деякі основні сфери застосування пмм.
- •5.2. Будова карбамидоформальдегидных смол.
- •5. 3. Вплив технологічних чинників на будову кфс.
- •5.4. Вплив технологічних чинників на зміст вільного f.
- •Зниження змісту вільного формальдегіду в кфс шляхом використання акцепторів формальдегіду.
- •5.5.1. Зниження токсичності кфс за рахунок введення в її склад
- •Зниження токсичності кфс за рахунок використання амінів і амидов карбонових кислот як акцептори формальдегіду.
- •Екологічно чистий спосіб отримання карбамидоформальдегидных олигомеров.
- •6.1. Отримання карбамідів олигомеров з диметилолмочевины.
- •6.2. Отримання карбамидоформальдегидных олигомеров з концентрату карбмидо-формальдегидного (форконденсата).
- •7. Модифіковані мочевиноформальдегидные полімери і матеріали на їх основі
- •8. Очищення стічних вод виробництва карбамидоформальдегидных смол.
- •8.1. Біохімічні методи очищення стічних вод від формальдегіду.
- •8. 2. Физико-хімічні методи очищення стічних вод.
- •8.3. Хімічні методи очищення стічних вод, що містять формальдегід.
- •9. Полімери меламино-формальдегидные
- •10. Полімери анилино-формальдегидные
- •11.Техніка безпеки при виробництві амино-альдегидных олигомеров і пластичних мас на їх основі
- •12. Феноло-альдегидные полімери
- •12. 1. Сировина для отримання фенолоальдегидных полімерів
- •12. 2. Особливості процесів синтезу фенолоальдегидных полімерів
- •12. 3. Каталізатори процесів отримання фенолформальдегидных олигомеров.
- •12. 4. Технологія отримання новолачных олигомеров
- •12.4.1 Властивості новолачных олигомеров і полімерів
- •12.5. Виробництво резольних олигомеров
- •12.5.1. Властивості резольних олигомеров і полімерів
- •12.6. Полімери на основі гомологов фенолу і формальдегіду
- •12.6.1. Феноло-фурфурольниє полімери
- •12.6.2. Полімери Феноло-лигниновые
- •12.7. Модифіковані полімери феноло-формальдегидные
- •12.7.1. Маслорастворімиє полімери феноло-формальдегидные
- •12.7.2. Поєднані полімери
- •12.8. Полімери резорцино-формальдегидные
- •12.8.1. Обесфеноліваніє водної фази
Зміст
Введення
|
2 |
1. Методи отримання полімерних матеріалів
|
2 |
2. Класифікація полыконденсацыйних полімерів і олігомерів, що отримуються по реакціях рівноважної поліконденсации
|
3 |
3. Аміноальдегидні олігомери
|
3 |
4. Карбамідоформальдегідні олігомери
|
3 |
4.1. Основні реакції процесу отримання карбамідоформальдегидних олігомерів
|
3 |
4.2. Технологія отримання карбамідоформальдегидныих олігомерів
|
11 |
4.3. Поліконденсация карбаміду і формальдегіду в кислому середовищі
|
11 |
4.3.1. Структура і властивості поліметиленкарбаміда
|
11 |
4.3.2. Вплив технологічних чинників на властивості поліметиленкарбаміда
|
16 |
4.3.3. Закономірності утворення твердої фази поліметиленкарбаміду
|
20 |
4.3.4. Модифікація поліметиленкарбаміду
|
22 |
4.3.5. Морфологія поліметиленкарбамиду
|
26 |
4.3.6. Деякі основні сфери застосування поліметиленкарбамиду
|
29 |
5. Отримання карбамідоформальдегідних олігомерів при перемінному рН
|
30 |
5.1. Технологія отримання карбамідоформальдегідної смоли КФ-МТ-15
|
30 |
5.2. Будова карбамідоформальдегидних смол
|
32 |
5.3. Вплив технологічних чинників на будову карбамідоформальдегидних смол
|
34 |
5.4. Вплив технологічних чинників на зміст вільного формальдегіду
|
39 |
5.5. Зниження вільного формальдегіду в карбамідоформаль-дегидних смолах шляхом використання акцепторів формальдегіду
|
42 |
5.5.1. Зниження токсичності КФС за рахунок введення в її склад ацетилацетона і аміаку
|
42 |
5.5.2. Зниження токсичності КФС за рахунок використання амінів і амидов карбонових кислот як акцепторів формальдегіду
|
45 |
6. Екологічно чистий спосіб отримання карбамідоформальдегидних олігомерів
|
48 |
6.1. Отримання карбамідоформальдегидних олигомерів з диметилолкарбаміду
|
51 |
6.2. Отримання карбамідоформальдегидних олігомерів з карбамідоформальдегідного концентрату
|
55 |
7. Модифіковані карбамідоформальдегідные олігомери і матеріали на їх основі
|
62 |
8. Очищення стічних вод виробництва карбамідоформальдегидних смол.
|
67 |
8.1. Біохімічні методи очищення стічних вод від формальдегіду
|
67 |
8.2. Физико-хімічні методи очищення стічних вод
|
68 |
8.3. Хімічні методи очищення стічних вод, що містять формальдегід
|
69 |
9. Меламіноформальдегідні олігомери
|
70 |
10. Аніліно-формальдегідні олігомери
|
71 |
11. Техніка безпеки при виробництві аміно-альдегидних олігомерів і пластичних мас на їх основі
|
75 |
12. Феноло-альдегідні олігомери
|
76 |
12.1 Сировина для отримання фенолоальдегідних олігомерів
|
77 |
12.2. Особливості процесів синтезу фенолоальдегідних олігомерів
|
80 |
12.3. Каталізатори процесів отримання фенолформальдегідних олігомерів
|
87 |
12.4. Технологія отримання новолачных олігомерів
|
94 |
12.4.1. Властивості новолачных олігомеров і полімерів
|
100 |
12.5. Виробництво резольних олігомерів
|
101 |
12.5.1. Властивості резольних олігомерів і полімерів
|
104 |
12.6. Полімери на основі гомологов фенолу і формальдегіду
|
105 |
12.6.1. Феноло-фурфурольні олігомери
|
106 |
12.6.2. Феноло-лігнінові олігомери
|
107 |
12.7. Модифіковані фенолоформальдегідні олігомери
|
108 |
12.7.1. Маслорозчинні фенолоформальдегідні олігомери
|
109 |
12.7.2. Поєднані олігомери
|
112 |
12.8. Резорцино-формальдегідні олігомери
|
115 |
12.8.1. Обесфенолювання водної фази
|
116 |
|
|
Вступ
Полімери - це високомолекулярні сполуки, молекули яких складаються з великого числа однакових угрупувань, що регулярно повторюються, сполучених між собою хімічним зв'язком. Регулярність повторення угрупувань не є обов'язковою ознакою полімерів, оскільки і висока молекулярна маса не є основним критерієм віднесення речовини до полімерів. Полімери мають істотні відзнаки від простих речовин.
Прості речовини можуть мати будь-яку молекулярну масу, але при цьому вони володіють постійними константами властивостей, які не залежать від способу їх отримання. У них постійна температура топлення (кипіння), певна молекулярна маса, постійний коефіцієнт заломлення і ін. Ці дані є константами для певної речовини і не залежать від способу їх отримання. На відміну від простих речовин, властивості високомолекулярних з'єднань залежать від способу їх отримання. Маючи однаковий елементний склад, навіть одну і ту ж молекулярну масу, полімери можуть істотно відрізнятися за своїми механічними властивостями, конфігурацією макромолекул і ін. Полімери однією брутто формули можуть мати різні фізичні константи.
Олігомери – це низькомолекулярні речовини, проміжні між простими речовинами і полімерами. Вони набувають властивостей полімерів в процесі їх переробки, збільшуючи свою молекулярну вагу за рахунок реакцій, що протікають при переробці, – подовження макромолекулярної цінуй, утворення зшитих просторових структур і ін. Олігомери – це особливий клас продуктів полімерної хімії, що має велике практичне застосування.
Технологія – це наука про виробництво, яка визначає якість початкових матеріалів, кількість і порядок їх використання, тимчасові і якісні режими їх переробки, якість готового виробу. Технологія тоді вважається за відпрацьовану, коли відомий вплив всіх параметрів технологічного процесу на якість і вихід кінцевого продукту. Ідеальний варіант хорошої технології – людський чинник при дотриманні основних параметрів не може вплинути на кінцевий результат.
1. Методи отримання полімерних матеріалів.
Не дивлячись на численність полімерних матеріалів, всі методи їх отримання можна описати одній з трьох реакцій
- полімеризації;
- поликонденсации;
- реакції полімер аналогічних перетворень.
Реакцію полімеризації можна представити схемою nА > An, т. е певна кількість мономера взаємодіють один з одним з утворенням макромолекули полімеру, при цьому не спостерігається утворення простих речовин. При поликонденсации мономер А реагує з мономером В з утворенням полімеру і простої речовини
nА + nВ > (АВ) n + nС
Поліконденсация буває рівноважною і нерівноважною. При рівноважній поликонденсации елементарна ланка макромолекули утворюється по рівноважній реакції, при нерівноважній - по нерівноважній реакції. Рівноважна реакція може стати не рівноважною, якщо в процесі поликонденсации видаляти просту речовину.
При полімер аналогічних перетвореннях основний ланцюг макромолекули не бере участь в реакції, а реагують бічні функціональні груп, при цьому утворюються нові функціональні групи і зберігається основний ланцюг макромолекули.
2. Класифікація поликонденсационных полімерів і олигомеров
отримуваних по реакціях нерівноважної поликонденсации..
Всі поликонденсационные полімери і олигомеры, що отримуються по реакціях нерівноважної поликонденсации, підрозділяються на наступні класи:
1. аминоальдегидные олигомеры;
2. фенолформальдегидные олигомеры;
3. полиэфирные полімери;
4. алкидные смоли;
5. епоксидні смоли;
3. Аміноальдегидниє олигомеры.
До аминоальдегидным олигомерам відносяться продукти, що отримуються по реакціях взаємодії формальдегіду і амінів. Як аміни найчастіше використовують карбамід, меламин і анілін і відповідно по використовуваних амінах олигомеры носять назву карбамидоформальдегидных, меламиноформальдегидных або анилиноформальдегидных.
4. Карбамідоформальдегидниє олигомеры.
4.1. Основні реакції, процесу отримання
карбамидоформальдегидных смол
Вперше реакція поликонденсации формальдегіду з сечовиною була відкрита в 1884г Толленсом і Хальцером. А практичне значення продуктам цієї реакції знайшов Джон в 1918г.
Поліконденсация карбаміду і формальдегіду приводить до утворення КФС, склад, властивості і будова, яких знаходяться залежно від співвідношення початкових компонентів, рН середи, часу і температури. При цьому КФС можуть містити в своєму складі продукти як лінійної, так і розгалуженої будови, також не виключені продукти циклічної будови [2 - 7]. Проте, наявні дані в літературних джерелах по будові карбамидоформальдегидных продуктів суперечливі. Це пояснюється складністю процесів, що відбуваються, під час утворення смол зважаючи на високу функціональність карбаміду (4) і формальдегіду (2), які приводять до великого числа можливих структур. Всіма продуктами реакції карбаміду (U) і формальдегіду (F) є гетероцепные з'єднання, що містять групу –N –CHR, – в комбінації з іншими заступниками.
Незалежно від умов проведення реакцій, першими продуктами взаємодії карбаміду і формальдегіду є метилольные похідні. У нейтральній або лужній середі при 400С можуть утворюватися, залежно від молярного співвідношення карбаміду і формальдегіду, монометилолкарбамид (1) і диметилолкарбамид (2):
NH2 CОNH2 + CH2 O ( NH2 CONHCH2 OH ( 1)
NH2 CОNH2 + 2CH2 O ( HOCH2 NHCONHCH2 OH ( 2)
Діметілолкарбаміди (ДМК) можуть також утворюватися в результаті взаємодії монометилолкарбамида (ММК) з (F):
 (
3)
(
3)
При надлишку (F) 3 – 4 міль на 1 міль (U) можливе утворення триметилолкарбамида (ТМК) тетраметилолкарбамида (ТЕМК). Проте, ці продукти украй нестійкі. Можливість утворення ТЕМК при рН 7 і молярному співвідношенні U:F = 1:1- 4 знаходить підтвердження в дослідженнях J. I Jong, J. De Jonge і H. A. K. Eden [9]:
![]() (4)
(4)
![]()
![]() (5)
(5)
Проте, деякі автори [10] вважають за можливе освіту разом з ТЕМК в слаболужній середі пента – і гексапроизводных карбаміду – в сильнощелочной середі при t ( 600С в результаті реакції метилендикарбамида з формальдегідом:
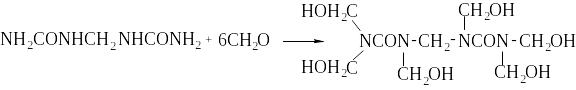 (6)
(6)
Встановлено, що найбільша швидкість реакції відповідає утворенню метилольных груп в результаті реакцій (F) з первинною аміногрупою. При подальшому утворенні метилольных груп реакційна здатність аминной, що залишилася, або иминной групи знижується. Автори приводять співвідношення швидкостей утворення моно-, ди-, триметилолкарбамида відповідно 1: 1/3: 1/9 [9]. Відмічено, що при проведенні реакції навіть при 20 – кратному надлишку (F) по відношенню до (U), в реакцію вступає лише 2,8 міль (F) на 1 міль (U) [10].
Рівноважне полягання продуктів ММК і ДМК у водній середі передбачає протікання реакцій з утворенням початкових з'єднань:
H2 NCONCH2 OH NH2 CONH2 + CH2 O (7)
HOCH2 NHCONHCH2 OH HOCH2 NHCONH2 + CH2 O (8)
Як правило, в лужній середі утворюються, в основному, метилольные похідні, в кислій – відбувається їх конденсація з утворенням продуктів, метиленовые, що містять, і метиленэфирные зв'язки. Так утворення ММК і ДМК в кислій середі супроводиться переходом в монометиленкарбамид при молярному співвідношенні U:F = 1:1 (схема реакції 9) або в диметиленкарбамид, при співвідношенні U: F = 1: 2 (схема 10):
NH2 CONHCH2 OH ( NH2 CON = CH2 (9) -H2O
HOCH2 NHCONHCH2 OH ( HOCH2 NHCON = CH2 ( CH2 = NCON = CH2
-H2O -H2O (10)
Утворення метиленэфирных зв'язків відбувається в результаті реакції метилольных похідних в нейтральній або слабокислой середі:
HOCH2 NHCONHCH2 OH + HOCH2 NHCONHCH2 OH (
HOCH2 NHCONHCH2 – Про – CH2 NHCONHCH2 OH + Н2о (11)
У сильнокислой середі метиленэфирные зв'язки руйнуються [10].
При взаємодії аміногрупи з метилольными групами утворюються з'єднання з метиленовыми зв'язками. Відомо декілька можливих реакцій утворення метиленовых зв'язків, які представлені в роботах J. I Jong, і J. De Jonge [10, 11]:
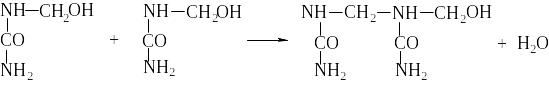 (12)
(12)
NH2CONHCH2 OH + NH2CONH2 ( NH2CONHCH2 NHCONH2 + H2O (13)
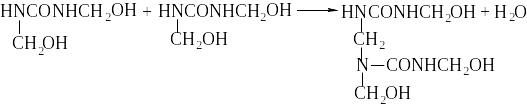 (14)
(14)
![]() (15)
(15)
![]() (16)
(16)
Можливі реакції (F) і ММК також і з метилендикарбамидом з утворенням метиленовых зв'язків [11]:
NH2CONHCH2OH + NH2CONHCH2NHCONH2 (
>NH2CONHCH2NHCONHCH2NHCONH2 + H2O (17)
NH2 CONHCH2 NHCONH2 + CH2 O ( NH2 CONHCH2 NHCONHCH2 OH (18)
Дослідження кінетики реакції утворення метиленовых зв'язків свідчать про те, що швидкості реакції взаємодії (F) з аміногрупою і реакції поликонденсации метилольных груп з аміногрупами в незначній мірі залежать від кількості залишків карбамідів в реагуючій молекулі [10]. У таблиці 1.1 приведені константи швидкості реакцій приєднання і конденсації, розраховані авторами відомих робіт [10–13] відповідно до вище приведених схем реакцій.
З таблиці 1.1 видно, що швидкості утворення метиленовых зв'язків в результаті реакцій (U) і ММК, майже однакові (таблиця. 1.1, схеми реакції № 13, 17). Реакції утворення метиленовых зв'язків є бімолекулярними і каталізують кислотними іонами (Н3о+). Реакції обратимы і у відповідних умовах можуть піддаватися гідролізу. Швидкість гідролізу метиленовых зв'язків назад пропорційна швидкості їх освіти [10].
Оборотними є також реакції приєднання (F) і конденсації метилольных груп, які при молярних концентраціях і тривалому часі реакції протікають до досягнення стану рівноваги. Швидкість таких реакцій залежить від концентрації компонентів, рН і температури.
Так, при високих концентраціях початкових з'єднань рівновага в системі зміщується у бік утворення продуктів реакції, внаслідок чого можуть відбуватися необоротні процеси з виділенням осаду і структурним зшиванням у вигляді полиметиленкарбамида.
Таблиця 1.1 Констант швидкості реакцій (при t =350 З)
№ схеми реакції
|
Значення рН
|
Константа швидкості реакції, моль/л·сек.
|
Літературне джерело
|
|
1 |
2 |
3 |
4 |
|
1 |
7,0 |
0,56·10-4
|
[9,10]
|
|
1 |
5,5 |
1,4·10-4
|
[9,10]
|
|
2 |
7,0 |
0,44·10-4
|
[13]
|
|
3 |
7,0 |
0,38·10-4
|
[8]
|
|
9 |
7,0 |
0,1·10-4
|
[8]
|
|
10 |
7,0 |
0,33·10-4
|
[8]
|
|
11 |
3,96 |
3·10-4
|
[9]
|
|
12 |
3,96 |
0,85·10-4
|
[9]
|
|
13 |
3,96 |
3,3·10-4
|
[9]
|
|
14 |
3,96 |
3·10-4
|
[9]
|
|
15 |
3,96 |
2·10-4
|
[9]
|
|
16 |
3,96 |
0,5·10-4
|
[9]
|
|
17 |
3,96 |
4,3·10-4
|
[10,13]
|
|
18 |
7,0 |
0,6·10-4
|
[9,10]
|
|
18 |
5,5 |
1,5·10-4
|
[9,10]
|
|
.
Встановлено, що в діапазоні значень рН 3,7 – 5,5 лімітуючою стадією реакції метилольных груп з аминными групами з утворенням Сн2 – зв'язків є стадія утворення иминиевых іонів.
Вплив значень рН на швидкість реакцій наочно представлений авторами в роботі [10] на малюнку 1.1. З малюнка 1.1 видно, що швидкості реакцій приєднання і конденсації однакові при рН 4,5. При нижчому значенні рН протікають, більшою мірою, реакції конденсації, при вищому значенні рН – реакції приєднання. При значеннях рН ( 7,0 освіта – Сн2 – зв'язків не відбувається.
Температура також робить вплив на швидкість реакцій
- g
До
g
До
 2
3 4 5 6 7 8 9 10 11 12 (рН)
2
3 4 5 6 7 8 9 10 11 12 (рН)
Малюнок 1.1. Залежність констант швидкості реакції приєднання і конденсації від значень рН при t = 350С:
(1) NH2 CONH2 + CH2 O ( NH2 CONHCH2 OH;
(2) NH2 CONH2 + NH2 CONHCH2 OH ( NH2 CONHCH2 NHCONH2
-H2O
Підвищення температури з 250С до 450С прискорює реакцію утворення метилендикарбамида в 4 рази (схема 13) з до =2,1·10-4 литр/моль·с до до =8,6·10-4 литр/моль·с [12]. При температурі 30-400С утворюються, в основному, низькомолекулярні з'єднання. Подальше нагрівання до 800-900С, незалежно від рН, приводить до зростання ступеня поликонденсации з подальшим утворенням олигомеров і полімерів. Утворення високомолекулярних з'єднань в системі карбамід – формальдегід може відбуватися і без підвищення температури, але у присутності кислотних каталізаторів, як які використовують HCl, H2SO, H3PO4 і інші кислоти. Будова таких продуктів може бути різноманітною. Якщо в системі домінуючим продуктом є ММК, тоді переважно утворюються полімери лінійної будови:
n NH2 CONHCH2 OH ( H –(NHCONHCH2(n– OH + Н2о(n-1) ( 19)
Також можуть утворюватися і продукти наступної будови:
H -(NHCON – CH2 – NHCONH2 (n– OН ( 20)
|
Сн2 ВІН
Спочатку, багато досліджень підтверджували лінійну будову карбамидоформальдегидных продуктів незалежно від способу їх отримання. Проте за допомогою ІК-СПЕКТРОСЬКОПІЇ було виявлено, що за наявності в олигомерном продукті залишків карбаміду більше 5, можуть утворюватися розгалуження за рахунок освіти метиленовых зв'язків в результаті реакцій з иминными групами [15]. Відомо, що утворення полімерів лінійної будови відбувається при молярному співвідношенні U:F = 1: 1. При співвідношенні U: F більш ніж 1 : 1 (наприклад 1 : 1,2 – 1 : 2,5 і більш), можливе утворення продуктів лінійно – розгалуженої будови [7], що містять у складі одночасного метиленэфирные, метиленовые зв'язки і метилольные групи, оскільки з метилольными групами однієї молекули може взаємодіяти рухливий атом водню другої молекули, створюючи тим самим умови для розгалужень:
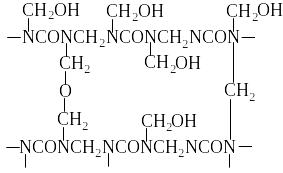 (21)
(21)
Представлений приклад на схемі 21 має спрощену будову і може складатися з різноманітних поєднань приведених фрагментів. Полімер подібної будови, як правило, розчинимо у воді, оскільки велика концентрація метилольных груп додає карбамидоформальдегидным смолам здатність розчинятися у воді [16,17].
Високомолекулярне з'єднання просторової будови утворюється в результаті реакцій конденсації між аминными, иминными і метилольными групами сусідніх макромолекул і які можуть бути представлені схемою:
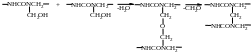 (22)
(22)
З двох типів поперечних зв'язків (див. схема 22) стійкішим є метиленовая зв'язок [8].
У складі карбамидоформальдегидных продуктів можуть також міститися і циклічні з'єднання. Можливість утворення циклічних структур підтверджується багатьма дослідженнями [4 – 6]. Так, Шивананда С. Джада в роботі [4] показав можливість утворення лінійних циклічних структур з ефірними зв'язками незалежно від значень рН і молярних співвідношень початкових з'єднань, оскільки їх освіта, як вважає автор, може бути наслідком реакції конденсації:
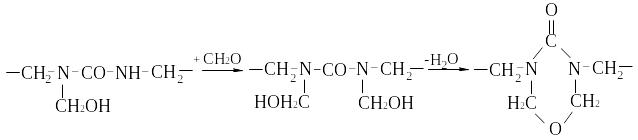 (23)
(23)
Відмічено, що утворення циклічних продуктів реакції, представлених схемою 23, відбувається більшою мірою при рН ( 7,5, чим при рН( 5,0.
Утворення циклічних продуктів у вигляді уроновых циклів у складі КФС знаходить підтвердження в роботах І.Я. Слоніма, Я.Г. Урмана і співробітників [6, 18]. Автори доводять можливість утворення уроновых циклів в результаті внутрішньомолекулярної конденсації метилольных груп похідних карбаміду, як в лужній, так і в кислій середі, але неодмінно при великому надлишку формальдегіду.
Штаудінгер із співробітниками в роботі [19,20] відзначають утворення триазиновых циклів у складі КФС за рахунок взаємодії метилольной групи з NH – групою сусідньої молекули карбаміду в ланцюзі з метиленовыми містками.
Гексагидротріазіновиє (триметилентриаминовые) цикли можуть утворюватися, як вважають Марвелл, Коршак в.В. із співробітниками [21], в результаті тримеризации ненасиченого метиленового похідного карбаміду наступної будови:
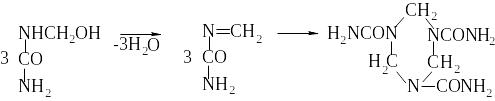 (24)
(24)
Проте утворення продуктів подібної будови (див. схеми реакцій 24) у складі КФС без додавання аміаку або інших амінів ставиться під сумнів авторами роботи [5] Пшеніциной в.П., Молоткової п.Н. і співробітниками, присвяченою вивченню структури карбамидоформальдегидных олигомеров.
