
- •1. Методи отримання полімерних матеріалів.
- •4.2. Технологія отримання карбамидоформальдегидных олигомеров.
- •4.3. Поліконденсация карбаміду і формальдегіду в кислій середі.
- •4.3.1.Структура і властивості полиметиленкарбамида.
- •4.3.3. Закономірності утворення твердої фази полиметиленкарбамида.
- •4.3.4.Модифікація полиметиленкарбамида.
- •4. 3.5. Морфологія полиметиленкарбамида.
- •4.3.6. Деякі основні сфери застосування пмм.
- •5.2. Будова карбамидоформальдегидных смол.
- •5. 3. Вплив технологічних чинників на будову кфс.
- •5.4. Вплив технологічних чинників на зміст вільного f.
- •Зниження змісту вільного формальдегіду в кфс шляхом використання акцепторів формальдегіду.
- •5.5.1. Зниження токсичності кфс за рахунок введення в її склад
- •Зниження токсичності кфс за рахунок використання амінів і амидов карбонових кислот як акцептори формальдегіду.
- •Екологічно чистий спосіб отримання карбамидоформальдегидных олигомеров.
- •6.1. Отримання карбамідів олигомеров з диметилолмочевины.
- •6.2. Отримання карбамидоформальдегидных олигомеров з концентрату карбмидо-формальдегидного (форконденсата).
- •7. Модифіковані мочевиноформальдегидные полімери і матеріали на їх основі
- •8. Очищення стічних вод виробництва карбамидоформальдегидных смол.
- •8.1. Біохімічні методи очищення стічних вод від формальдегіду.
- •8. 2. Физико-хімічні методи очищення стічних вод.
- •8.3. Хімічні методи очищення стічних вод, що містять формальдегід.
- •9. Полімери меламино-формальдегидные
- •10. Полімери анилино-формальдегидные
- •11.Техніка безпеки при виробництві амино-альдегидных олигомеров і пластичних мас на їх основі
- •12. Феноло-альдегидные полімери
- •12. 1. Сировина для отримання фенолоальдегидных полімерів
- •12. 2. Особливості процесів синтезу фенолоальдегидных полімерів
- •12. 3. Каталізатори процесів отримання фенолформальдегидных олигомеров.
- •12. 4. Технологія отримання новолачных олигомеров
- •12.4.1 Властивості новолачных олигомеров і полімерів
- •12.5. Виробництво резольних олигомеров
- •12.5.1. Властивості резольних олигомеров і полімерів
- •12.6. Полімери на основі гомологов фенолу і формальдегіду
- •12.6.1. Феноло-фурфурольниє полімери
- •12.6.2. Полімери Феноло-лигниновые
- •12.7. Модифіковані полімери феноло-формальдегидные
- •12.7.1. Маслорастворімиє полімери феноло-формальдегидные
- •12.7.2. Поєднані полімери
- •12.8. Полімери резорцино-формальдегидные
- •12.8.1. Обесфеноліваніє водної фази
6.1. Отримання карбамідів олигомеров з диметилолмочевины.
Для отримання КФС без надсмольной води як початкову сировину використовують диметилолмочевину – продукт конденсації карбаміду і двох мілі формальдегіду. Діметілолмочевіна є білим порошком, добре розчинним у воді. Її отримують шляхом конденсації карбаміду з формальдегідом і молярному співвідношенні компонентів 1 : 2 при рН 8,0 і температурі 85-90оС. Для отримання карбамідів олигомеров з диметилолмочевины її розчиняють в 2 х мілі технічного формальдегіду (37 %), завантажують 2 міль карбаміду і ведуть поликонденсацию спочатку в лужній середі при рН= 8,8-9,5 при температурі 95оС протягом 1 години, потім в кислій середі при рН 4,5-5,0 протягом 0,5 години, потім знову в лужній середі до завершення поликонденсации до досягнення коефіцієнта рефракції Кр1.4520-1.4560.
Процес поликонденсации диметилолмочевины, карбаміду і формальдегіду по складу реакційної маси істотно відрізняється від процесу поликонденсации карбаміду і формальдегіду .Для порівняння на малюнку 5.6.2. приведений даний по залежності вміст метилольных груп і формальдегіду в обох процесах і F в процесі поликонденсации приведені на мал.
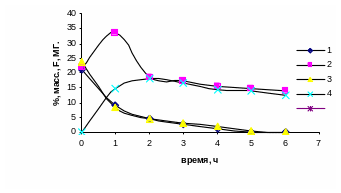
Мал. 5.6.2. Залежність змісту F (крива 1,3) і МІЛІГРАМ (крива 2,4) від часу поликонденсации
На першій стадії поликонденсации карбаміду і формальдегіду досить висока концентрація формальдегіду-23.8% мас.(див. рис 1, крива 1), взаємодія якого з карбамідом приводить до утворення метилольных похідних карбаміду, що супроводиться накопиченням метилольных груп (МІЛІГРАМ) і спадом концентрації формальдегіду (див. мал. 5.6.2 крива 1, 3). Реакційна маса складається в основному з монометилолкарбамида і диметилолкарбамида. При отриманні карбаміду олигомера з диметилолкарбамида початкова реакційна маса містить формальдегід і диметилолкарбамид, при цьому зміст формальдегіду і метилольных груп досить високий –21,1% мас і 21,85% мас відповідно. Взаємодія послід--них супроводиться накопиченням метилольных груп до 33,6% мас. і зменшенням змісту формальдегіду. (см мал. 1, криві 2 і 4). Реакційна маса в цьому випадку повинна істотно відрізнятися від реакційної маси, що утворюється при отриманні промислової КФС.
Якісний склад реакційної маси, визначений за допомогою методу спектроскопії Ямр13с показує наступне.
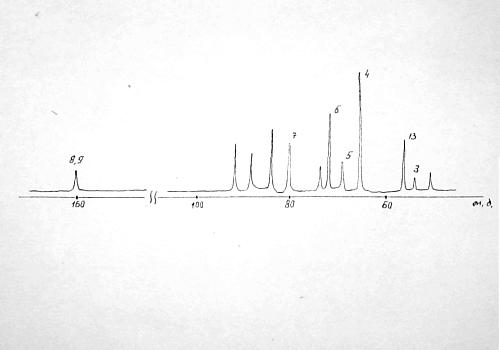
Мал. 5. 1. 2. Спектр Ямр13с реакційної маси. (Віднесення сигналів приведене в тексті)
На стадії I в лужній середі при взаємодії формальдегіду і диметилолкарбамида протягом 60 мін разом з дизамещенными карбамидами (b,d), метиленметоксильными групами біля третинного атома азоту (k), метилольными і метиленэфирными групами переважно біля вторинного атома азоту (p, про) утворюються уро-новые цикли (?=155 м. д.) (рис.2). Із спектрів видно, що на стадії I в лужній середі утворюються продукти як лінійної, так і лінійно-розгалуженої будови із змістом циклічних структур. Метілольниє похідні біля третинного атома азоту є досить нестійкими продуктами і знаходяться в термодинамічній рівновазі з F .
Істотна відмінність реакційних мас при синтезі смоли з диметилолкарбамида в порівнянні з синтезом без нього не позначаються на якісних показниках карбаміду олигомера, що видно з таблиці 5.1.1.
№ п/п
|
Найменування показників
|
КФС промыш- ленна
|
КФС зразок 1
|
КФС зразок 2
|
1. |
Масова частка сухого залишку %.
|
64 - 68 |
65,6 |
66,2 |
2. |
Зміст вільного F % мас.
|
до 0,15
|
0 |
0,06 |
3. |
В'язкість по ВЗ-4, з
|
50-80 |
65-72 |
65-72 |
4. |
Негативний логарифм концентрації водневих іонів, рН
|
7,5-8,5 |
8,2 |
8,2 |
5. |
Час желатинизации пр 100оС, з
|
50-70 |
66,5 |
68 |
6. |
Смешиваємость з водою за об'ємом
|
1 : (2-10) |
1: 8 |
1 : 8 |
7.. |
Коефіцієнт рефракції
|
1,452-1,46 |
1,458 |
1,456 |
Всі якісні показники КФС, синтезованих з ДММ, знаходяться в межах вимог, передбачених стандартами, що діють, до цих смол, а зміст вільного F не перевищує 0.06% мас, що значно нижче, ніж біля промислової КФС. Проте смоли отримані з ДММ істотно відрізняються від КФП, отриманою з F і U по своєму фрагментарному складу. На малюнку 5.1.3 приведені спектри Ямр13с синтезованих смол і промислової КФС.
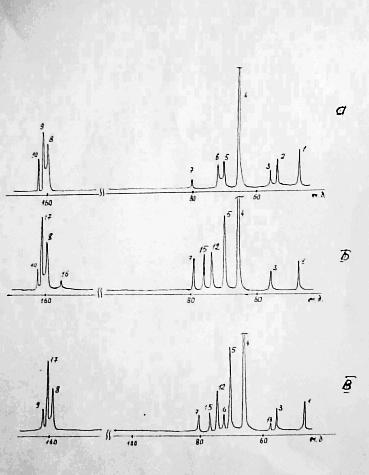
Мал. 5.1.3.
Як видно з приведених даних, всі досліджувані зразки містять метиленовые групи в середньому ланцюзі макромолекули (сигнал 1), метиленовые групи біля атомів азоту, пов'язаного з метиленэфирными групами (сигнал 5), метилольные групи біля первинного атома азоту (сигнал 4), метиленэфирные фрагменти (сигнал 7), метиленовые групи біля сечовини з вільною аміногрупою (сигнал 9). Крім того, промислова КФС містить метиленовые групи біля третинного атома азоту (сигнал 2), метиленовые групи біля азоту з метиленэфирными фрагментами (сигнал 3), метилольные групи біля третинного атома азоту (сигнал 6) і вільну U (сигнал 10).
Отримані дані дають підставу рахувати КФС, отримані з ДММ більш розгалуженої будови і з великим змістом ефірних фрагментів, в порівнянні з промисловою КФС. Наявність останніх пояснює вищий час желатинизации синтезованих смол, в порівнянні з промисловою (див. таблиці. 1, п. 5), бо відомо, що для підвищення стабільності КФС використовують їх ефіризацію спиртами [6].
