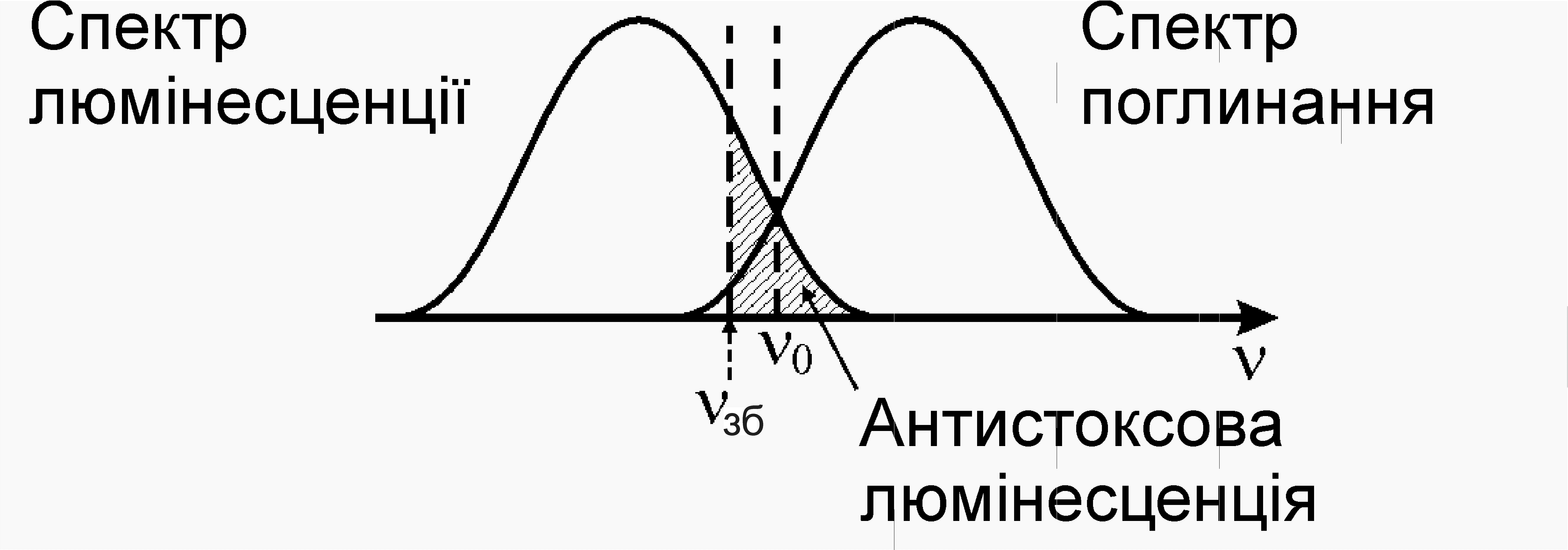- •29.1.2. Закон Кірхгофа
- •29.1.3. Закони випромінювання ачт
- •29.2. Зовнішній фотоефект
- •29.3. Енергія та імпульс світлових квантів
- •29.4. Ефект Комптона
- •29.5. Модель атома Бора - Резерфорда. Досліди Франка і Герца
- •29.6. Спектр атома водню за Бором
- •30. Елементи квантової механіки
- •30.1. Корпускулярно-хвильовий дуалізм
- •30.2. Співвідношення невизначеностей Гейзенберга
- •30.3. Хвильова функція і її статистичний зміст
- •30.4. Рівняння Шредінгера
- •30.5. Розв’язування рівняння Шредінгера для мікрочастинки, що міститься в нескінченно глибокій потенціальній ямі
- •30.6. Квантовий гармонічний осцилятор
- •30.7. Тунельний ефект
- •31. Фізика атомів і молекул
- •31.1. Квантово-механічна модель атома водню
- •31.2. Дослід Штерна і Герлаха. Спін електрона
- •31.3. Принцип Паулі. Періодична система елементів Менделєєва
- •31.4. Рентгенівські спектри
- •31.5. Типи міжатомних зв'язків і утворення молекул
- •31.6. Молекулярні спектри
- •31.7. Комбінаційне розсіювання світла
- •31.8. Люмінесценція
- •32. Елементи квантової статистики
- •32.1. Класична і квантова статистики
- •32.2. Розподіли Фермі-Дірака та Бозе-Ейнштейна
- •33. Фізика твердого тіла
- •33.1. Елементи зонної теорії кристалів
- •33.2. Діелектрики
- •33.3. Метали
- •33.4. Напівпровідники
- •33.5. Домішкова провідність напівпровідників
- •33.7. Напівпровідникові прилади
- •33.8. Фотопровідність
- •34. Макроскопічні квантові ефекти
- •34.1 Явище надпровідності
- •34.2. Ефект Джозефсона
- •34.3. Надтекучість
- •35. Основи квантової електроніки
- •35.1. Взаємодія випромінювання з речовиною
- •35.2. Інверсна заселеність
- •35.3. Лазери
- •36. Фізика атомного ядра
- •36.1. Будова та основні характеристики атомних ядер
- •36.2. Енергія зв'язку ядра. Дефект маси
- •36.3. Властивості ядерних сил
- •36.4. Феноменологічні моделі ядра
- •36.5. Радіоактивні перетворення атомних ядер
- •36.6. Закономірності -розпаду
- •36.7. Закономірності -розпаду
- •36.9. Ядерні реакції
- •36.40. Спонтанний поділ ядер
- •36.11. Вимушений поділ ядер. Ланцюгова реакція поділу
- •36.12. Ядерний реактор
- •36.13. Термоядерні реакції
- •36.14. Дозиметричні одиниці
- •37. Елементарні частинки
- •37.1. Фундаментальні взаємодії
- •37.2. Класи елементарних частинок
- •37.3. Характеристики елементарних частинок
- •37.4. Частинки й античастинки
- •37.5. Лептони
- •37.6. Адрони
- •37.7. Кварки
- •37.8. Переносники фундаментальних взаємодій
- •37.9. Велике об'єднання
- •Висновок
31.8. Люмінесценція
Крім термодинамічно рівноважного теплового випромінювання існують також нерівноважні випромінювання, одним з видів яких є люмінесценція. По визначенню С. І. Вавилова люмінесценцією називається надлишкове над тепловим випромінювання, якщо його тривалість перевищує 10‑ 10 с. Це визначення дозволяє відрізнити люмінесценцію, спектр якої, як правило, розташований у видимому діапазоні, від рівноважного теплового випромінювання, яке при кімнатній температурі у видимій частині спектра практично відсутнє. На відміну від відбитого світла, що зникає практично миттєво після перекриття падаючого променя, люмінесценція характеризується певною «інерційністю», тобто після припинення підведення енергії від зовнішнього джерела люмінесценція триває від 10-10 с до декількох секунд і більше.
По механізму підведення енергії збудження розрізняють такі основні види люмінесценції.
1. Фотолюмінесценція – збудження молекул електромагнітним випромінюванням видимого й ультрафіолетового діапазонів.
2. Корпускулярна люмінесценція – збудження молекул ударами мікрочастинок (найчастіше електронів).
3. Хемілюмінесценція — виникнення світіння в ході хімічних перетворень, у яких енергія хімічної реакції перетворюється безпосередньо у світлову. Надзвичайно цікавий вид хемілюмінесценції — біолюмінесценція (світіння живих об'єктів (бактерій, світлячків, риб тощо).
4. Електролюмінесценція – світіння, що виникає при внесенні деяких напівпровідників в електричне поле, під дією якого електрони переходять на більш високі енергетичні рівні з наступними переходами на нижчі рівні енергії, що супроводжуються висиланням світлових квантів.
За тривалістю світіння люмінесценція підрозділяється на два види: флуоресценція (час загасання ~ 10-8 с) і фосфоресценція ( – до декількох секунд і навіть годин). Поділ люмінесценції на флуоресценцію та фосфоресценцію умовний, оскільки часові інтервали загасання цих видів люмінесценції не мають чітких границь і можуть перекриватися.
Розглянемо основні закономірності флуоресценції, що виникає, як правило, у газах, рідких або твердих розчинах.
Рис. 31.8

![]() ,
,
тобто л < з. Дістали правило Стокса: світло люмінесценції має меншу частоту в порівнянні із частотою світла, що збуджує люмінесценцію.
Рис. 31.9

![]() ,
,
тобто л > з.
Більш
загальним є правило Стокса-Ломмеля:
спектр люмінесценції зсунутий в область
менших частот у порівнянні зі спектром
поглинання (рис. 31.10). Частота 0,
що відповідає точці перетинання спектрів
поглинання й люмінесценції, задовольняє
умові
![]() ,
тобто енергія кванта h0
дорівнює різниці енергії збуджених
,
тобто енергія кванта h0
дорівнює різниці енергії збуджених
![]() і основного
і основного
![]() електронного станів. Ця частота аналогічна
граничній частоті фотоефекта.
електронного станів. Ця частота аналогічна
граничній частоті фотоефекта.
Рис. 31.10