
- •29.1.2. Закон Кірхгофа
- •29.1.3. Закони випромінювання ачт
- •29.2. Зовнішній фотоефект
- •29.3. Енергія та імпульс світлових квантів
- •29.4. Ефект Комптона
- •29.5. Модель атома Бора - Резерфорда. Досліди Франка і Герца
- •29.6. Спектр атома водню за Бором
- •30. Елементи квантової механіки
- •30.1. Корпускулярно-хвильовий дуалізм
- •30.2. Співвідношення невизначеностей Гейзенберга
- •30.3. Хвильова функція і її статистичний зміст
- •30.4. Рівняння Шредінгера
- •30.5. Розв’язування рівняння Шредінгера для мікрочастинки, що міститься в нескінченно глибокій потенціальній ямі
- •30.6. Квантовий гармонічний осцилятор
- •30.7. Тунельний ефект
- •31. Фізика атомів і молекул
- •31.1. Квантово-механічна модель атома водню
- •31.2. Дослід Штерна і Герлаха. Спін електрона
- •31.3. Принцип Паулі. Періодична система елементів Менделєєва
- •31.4. Рентгенівські спектри
- •31.5. Типи міжатомних зв'язків і утворення молекул
- •31.6. Молекулярні спектри
- •31.7. Комбінаційне розсіювання світла
- •31.8. Люмінесценція
- •32. Елементи квантової статистики
- •32.1. Класична і квантова статистики
- •32.2. Розподіли Фермі-Дірака та Бозе-Ейнштейна
- •33. Фізика твердого тіла
- •33.1. Елементи зонної теорії кристалів
- •33.2. Діелектрики
- •33.3. Метали
- •33.4. Напівпровідники
- •33.5. Домішкова провідність напівпровідників
- •33.7. Напівпровідникові прилади
- •33.8. Фотопровідність
- •34. Макроскопічні квантові ефекти
- •34.1 Явище надпровідності
- •34.2. Ефект Джозефсона
- •34.3. Надтекучість
- •35. Основи квантової електроніки
- •35.1. Взаємодія випромінювання з речовиною
- •35.2. Інверсна заселеність
- •35.3. Лазери
- •36. Фізика атомного ядра
- •36.1. Будова та основні характеристики атомних ядер
- •36.2. Енергія зв'язку ядра. Дефект маси
- •36.3. Властивості ядерних сил
- •36.4. Феноменологічні моделі ядра
- •36.5. Радіоактивні перетворення атомних ядер
- •36.6. Закономірності -розпаду
- •36.7. Закономірності -розпаду
- •36.9. Ядерні реакції
- •36.40. Спонтанний поділ ядер
- •36.11. Вимушений поділ ядер. Ланцюгова реакція поділу
- •36.12. Ядерний реактор
- •36.13. Термоядерні реакції
- •36.14. Дозиметричні одиниці
- •37. Елементарні частинки
- •37.1. Фундаментальні взаємодії
- •37.2. Класи елементарних частинок
- •37.3. Характеристики елементарних частинок
- •37.4. Частинки й античастинки
- •37.5. Лептони
- •37.6. Адрони
- •37.7. Кварки
- •37.8. Переносники фундаментальних взаємодій
- •37.9. Велике об'єднання
- •Висновок
31.5. Типи міжатомних зв'язків і утворення молекул
При зближенні молекул між ними виникають сили міжатомної взаємодії, які можуть приводити до утворення молекул.
Розрізняють два види міжатомних (хімічних) зв'язків – іонну та ковалентну.
Природа іонного зв'язку може бути пояснена в рамках класичної фізики як результат кулонівських сил притягання між різнойменно зарядженими іонами. Типовими прикладами молекул з іонним зв'язком є галоген-водні – HCl, HBr тощо. При зближенні атомів водню й галогену електрони атома водню переходять у зовнішню, недобудовану оболонку атома галогену, добудовуючи її до оболонки інертного газу. У результаті цього виникає кулонівське притягання між двома різнойменно зарядженими іонами, що забезпечує стійкість полярної молекули, що утворилася.
Ковалентний зв'язок має універсальний характер і утворюється між будь-якими атомами. У найбільш чистому виді ковалентний зв'язок проявляється в молекулах, що складаються з однотипних атомів, таких як H2, O2 тощо.
Природа ковалентного зв'язку не може бути пояснена в рамках класичної фізики й вимагає використання квантово-механічних уявлень. Як показали теоретичні розрахунки та експерименти, ковалентні зв'язки мають властивість насичення, що виражається в певній валентності атомів і певної спрямованості, що формує просторову структуру молекули. При зближенні атомів їх електронні оболонки починають перекриватися, що приводить до виникнення обмінної взаємодії, відповідальної за утворення ковалентного зв'язку між атомами (див. Додаток. 8).
31.6. Молекулярні спектри
Повна внутрішня енергія W молекули може бути представлена як сума енергій електронів Wел, коливального руху ядер Wкол і обертального руху Wоб молекули як цілого:
![]() .
.
Електронна
частина енергії молекули, як і в атомі,
може набувати дискретного ряду значень:
![]() ,
,
![]() ,
... . Стан з найменшим значенням енергії
,
... . Стан з найменшим значенням енергії
![]() називається основним (незбудженим).
Далі йде перший збуджений стан з енергією
називається основним (незбудженим).
Далі йде перший збуджений стан з енергією
![]() і т.д.
і т.д.
Перейдемо тепер до розгляду енергії коливального руху молекули.
Кожний атом молекули має три ступені свободи, тому якщо молекула складається з N атомів, то загальне число ступенів свободи дорівнює 3N. Із цього числа три ступені свободи доводяться на поступальний і три ступені – на обертальні рухи молекули як цілого. Отже, число коливальних ступенів свободи дорівнює 3N–6 і молекула може виконувати 3N–6 різних коливань. З достатнім наближенням можна вважати, що ці коливання є гармонічними із частотами 1, 2, ..., 3N-6. Енергія i-го гармонічного коливання може бути виражена через частоту гармонічного осцилятора формулою (див. §30.6)
-
 ,
,(31.8)
де i=0, 1, 2, ... - коливальні квантові числа. Таким чином, коливальна частина енергії молекули квантується, тобто може мати ряд дискретних значень.
Обертальну енергію молекули можна представити у вигляді
-
 ,
,(31.9)
де J — момент інерції молекули відносно осі, що проходить через її центр мас; L = J — момент імпульсу. Як і для електрона в атомі (див. § 31.1), момент імпульсу молекули квантується:
-
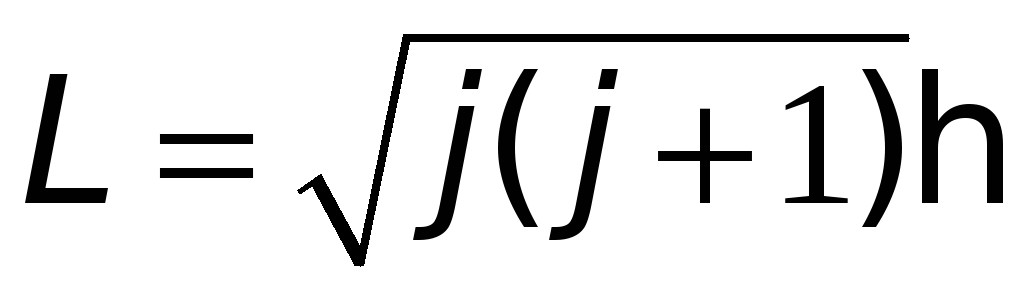 ,
,(31.10)
де j — обертальне квантове число, що приймає значення j=0, 1, 2, ... .
Таким чином, обертальна енергія молекули також квантується, тобто дискретна:
-
 .
.(31.11)
На підставі викладеного можна зробити висновок, що повна енергія молекули

може приймати лише дискретні значення.
Теорія й дослід показують, що відстань між електронними рівнями енергії значно більша відстаней між коливальними рівнями, які, у свою чергу, значно більші відстаней між обертальними рівнями енергії:
![]() .
.
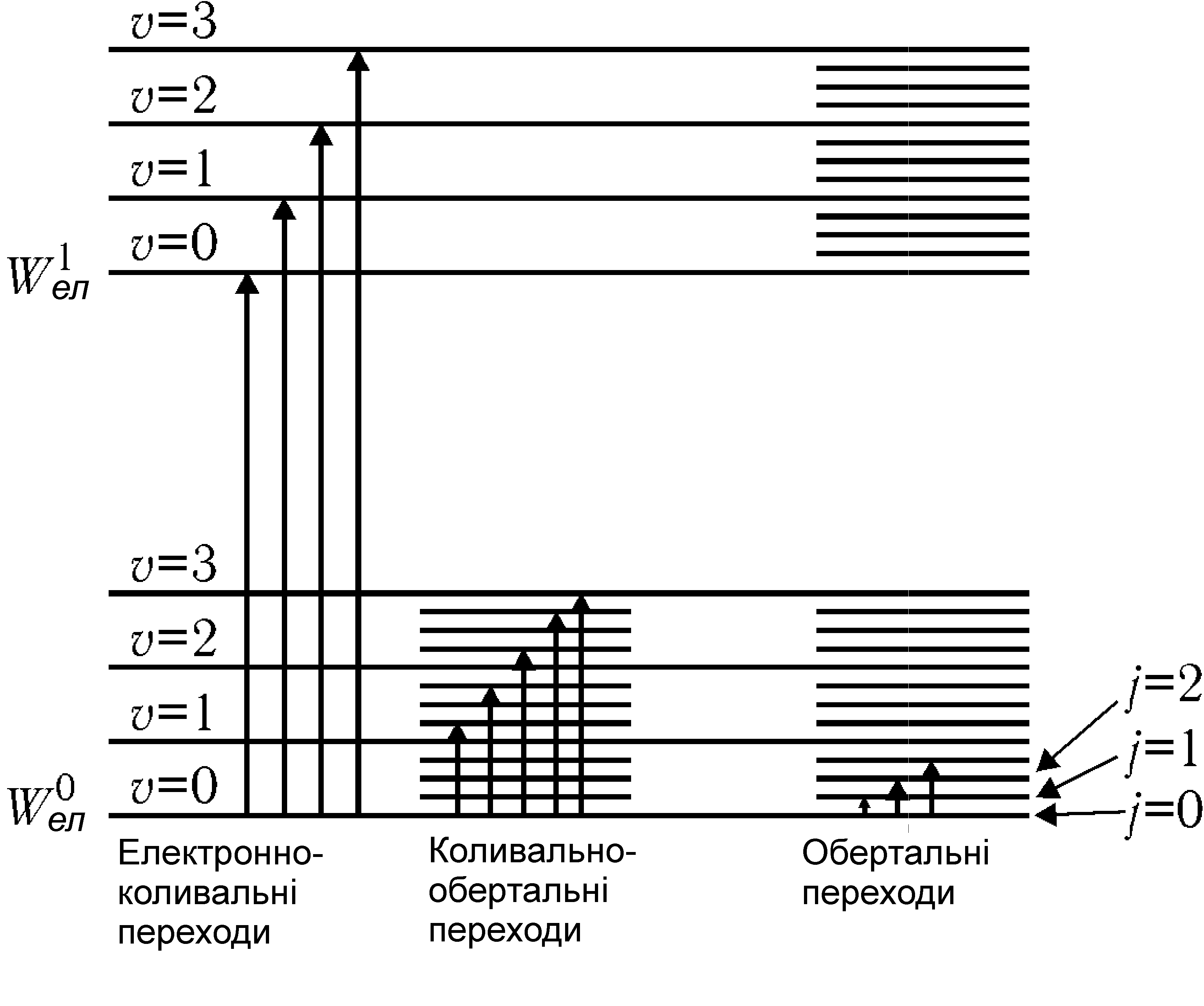
Рис. 31.5
Енергетична
схема рівнів двохатомної молекули
показана на рис. 31.5, де
![]() ,
,
![]() ,
— електронні рівні; v=
0, 1, 2, ... — коливальні квантові числа
(нульовий коливальний рівень суміщений
з електронним); j
= 0, 1, 2, ... -
обертальні квантові числа.
,
— електронні рівні; v=
0, 1, 2, ... — коливальні квантові числа
(нульовий коливальний рівень суміщений
з електронним); j
= 0, 1, 2, ... -
обертальні квантові числа.
У загальному випадку при поглинанні фотона енергії h молекула може перейти в стан зі збудженням обертальних, коливальних і електронних рівнів енергії:
![]() ,
,
де,
наприклад,
![]() — різниця енергій між коливальними
рівнями v
і v'.
— різниця енергій між коливальними
рівнями v
і v'.
У міліметровому діапазоні радіохвиль енергія фотона настільки мала, що її вистачає лише для збудження обертальних рівнів (Wоб ≠ 0, Wкол=0, Wел=0). Виникає обертальний спектр, що складається з ряду близько розташованих ліній. Частоти ліній цього спектра знаходять із умови
 .
.
Для обертальних рівнів діє правило відбору: можливі переходи тільки між сусідніми рівнями, тому j/ = j+1. Тоді
-
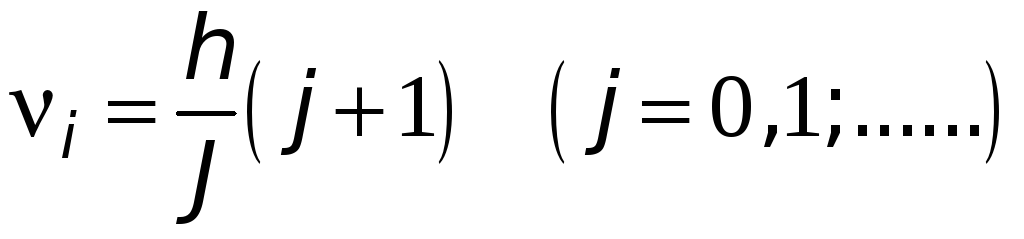 .
.(31.12)
Вимірявши на досліді частоту обертальної лінії спектра, можна за допомогою (31.12) знайти момент інерції і потім – рівноважний стан між ядрами у двохатомній молекулі або розміри більш складних молекул.
Рис. 31.6
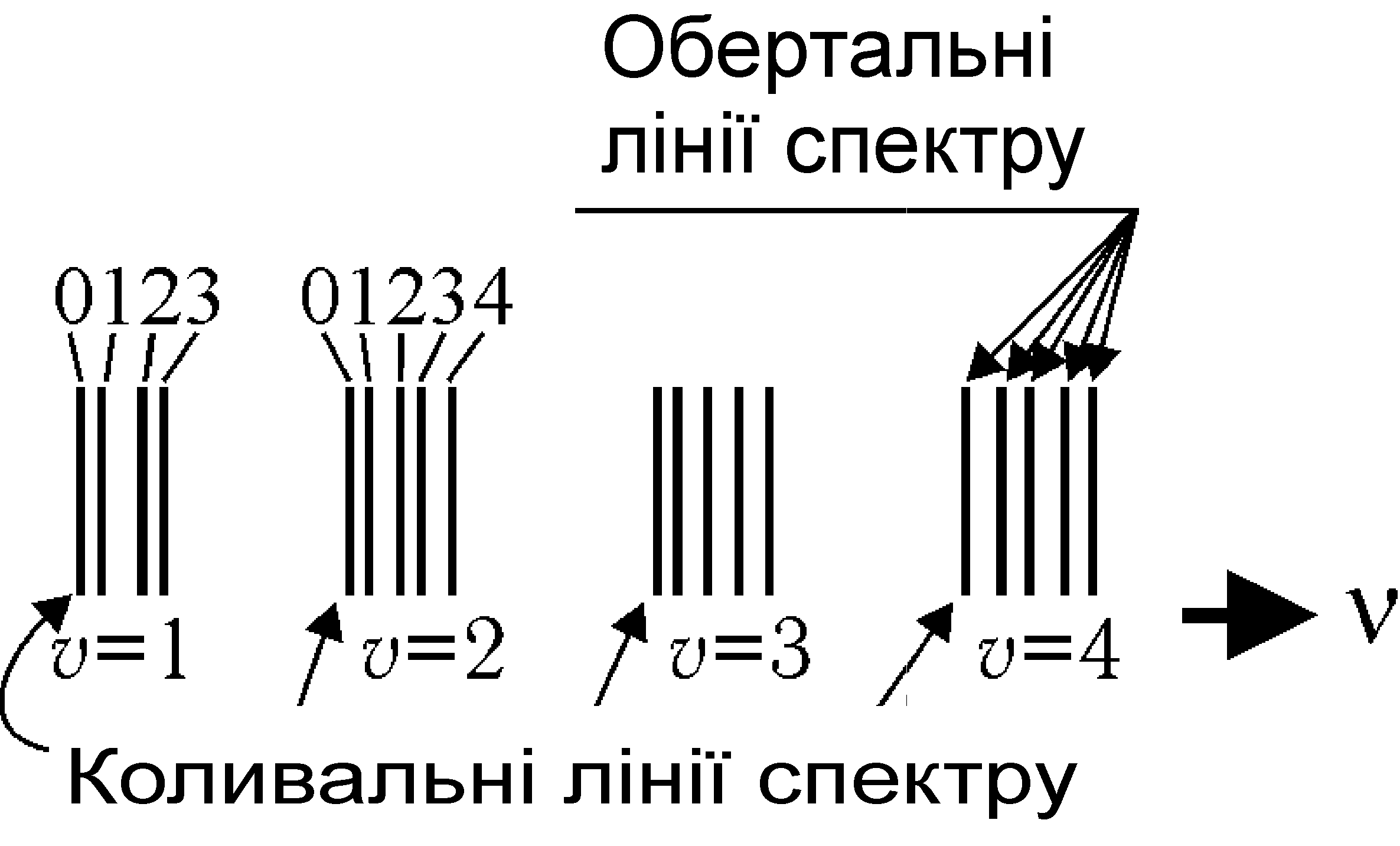
І, нарешті, у видимій і ультрафіолетовій частині електромагнітного діапазону розташовується електронно-коливальний спектр (Wоб ≠ 0, Wкол ≠ 0, Wел≠0). Для його реєстрації застосовують прилади, де обертальна структура спектра не розрізняється: у межах однієї коливальної лінії відбувається злиття всіх обертальних ліній.
Коливальна структура електронно-коливальних спектрів проявляється лише для найпростіших молекул. Складні багатоатомні молекули дають, як правило, суцільні спектри поглинання та випромінювання.
Спектри поглинання молекул у більшості випадків строго індивідуальні: кожна молекула має свій спектр. За видом спектра можна проводити ідентифікацію молекул, а за його інтенсивністю можна визначати концентрацію відповідної речовини. Завдяки цьому можливий спектральний аналіз складних хімічних сумішей.
