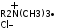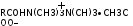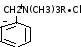- •Розділ 1
- •1.2. Фізико-хімічна механіка як наукова дисципліна, її задачі
- •1.3. Дисперсні системи. Класифікація дисперсних систем з позицій фізико-хімічної механіки композиційних матеріалів
- •1.3.6. Періодичні колоїдні системи.
- •1.4. Особливості властивостей колоїдних систем
- •1.5. Короткий історичний огляд
- •Розділ 2
- •2.2. Змочування і набухання
- •2.3. Спонтанні процеси на межі розділу фаз
- •Розділ 3
- •3.2. Теорія мономолекулярної адсорбції Ленгмюра
- •3.3. Полімолекулярна адсорбція
- •3.4. Рівняння Гіббса. Двомірний тиск
- •3.5. Правило Дюкло-Траубе
- •3.6. Адсорбція на межі тверде тіло – розчин
- •Розділ 4
- •4.2. Класифікація пар за хімічною будовою
- •4.3. Аніоноактивні пар
- •4.4. Катіоноактивні пар
- •4.5. Класифікація пар за механізмом дії
- •4.6. Термодинамічні, поверхневі й об'ємні властивості розчинів пар у зв'язку зі стійкістю дисперсних систем
- •4.7. Використання пар в техніці
- •Розділ 5
- •5.1.1. Будова подвійного електричного шару (пдеш)
- •5.2. Стійкість і коагуляція дисперсних систем
- •5.3. Седиментаційна (кінетична) стійкість
- •5.4. Процеси стабілізації дисперсних систем і їхня роль у техніці
- •Розділ 6
- •6.2. Загальні відомості про структуроутворення в дисперсних системах
- •Розділ 7
- •7.2. Методи реологічного моделювання
- •7.3. Криві течії і в'язкості
- •7.4. Методика побудови реологічних кривих
- •7.5. Моделі і рівняння течії структурованих дисперсних систем
- •7.6. Про реологічні криві течії і в'язкості структурованих рідин на прикладі цементобетонних сумішей
- •Іі частина
- •8.2. Розчинення в'яжучих речовин
- •8.3. Основні закономірності кінетики кристалізації нової фази з пересичених розчинів і фазовий склад цементного каменю
- •8.4. Формування структури цементного каменю
- •Розділ 9
- •9.2. Основні параметри вібраційного ущільнення бетонної суміші
- •9.3. Вібродиспергування та виброперемішування суміші
- •9.4. Основи технології виробництва дорожніх бетонів на основі органічних в'яжучих
- •9.4.2. Принцип та метод визначення температури перемішування сумішей
- •9.4.3. Температурні параметри приготування сумішей
- •9.4.4. Змочування кам'яних матеріалів в'яжучим як фактор якості перемішування
- •9.4.5. Зміст процесу ущільнення асфальтобетону.
- •9.4.6. Шляхи інтенсифікації ущільнення сумішей
- •Розділ 10
- •10.1. Склад, структура і властивості кам'яновугільних дорожніх дьогтів
- •10.2 Склад, структура і властивості нафтових дорожніх бітумів
- •10.3. Бітумні емульсії
- •10.3.2. Бітумні емульсії – мікрогеторогенні дисперсні системи
- •10.3.3. Технологія виробництва
- •Технічна характеристика диспергатора дб – 1
- •Технічна характеристика триступеневого диспергатора
- •10.3.4. Фізико-механічні властивості та технологічні вимоги.
- •10.3.5. Галузі застосування.
- •Бітумополімерні в’яжучі і асфальтобетони на їх основі
- •Розділ 11
- •11.2. Дьогтебетон
- •11.3. Асфальтобетон
- •11.3.1. Утомленісна довговічність асфальтобетонів і роль агресивних середовищ
- •11.4. Дьогтебетони і асфальтобетони з комплексно-модифікованою мікроструктурою
- •Рекомендована література до вивчення теоретичного матеріалу
4.2. Класифікація пар за хімічною будовою
У хімічному відношенні ПАР розділяють на неіоногенні і іоногенні речовини.
Молекули неіоногенних ПАР містять кінцеві групи, що неіонізовані, з високою спорідненістю до дисперсійного середовища. До складу їх звичайно входять атоми кисню, азоту і сірки (емульгатори, мийні речовини).
До групи неіногенних ПАР відносяться продукти оксиетилювання довголанцюгових спиртових кислот, спиртів, амінів, алкілфенолів, наприклад, з’єднання такого складу R·COO(C2H4O) nH; R·CH2O(C2H4O) nH; R·C6H5O(C2H4O)ОH, а також складні ефіри багатоатомних спиртів і жирних кислот, аміди жирних кислот, лігносульфонові кислоти, похідні целюлози. Розчинність неіногенних ПАР у воді обумовлена функціональними групами, що мають спільну спорідненість з нею.
Іоногенні речовини поділяються на два основних класи. Якщо довгий ланцюжок (вуглеводнева частина) молекули з низькою спорідненістю з дисперсійним середовищем входить до складу аніона, що утворюється у водяному розчині, сполуки відносять до аніоноактивних речовин. Типовою аніоактивною ПАР є стеарат натрію, що утворює у водяному розчині іони Na+ і C17Н35СООН- (довгий ланцюжок). Поверхневу активність визначає аніон.
Відповідно катіоноактивні ПАР утворюють у водяних розчинах катіони, що містять довгий ланцюжок – вуглеводневий радикал.
Подальший розподіл аніоноактивних і катіоноактивних речовин може бути проведено залежно від характеру іоногенної групи (табл. 4.1).
Третя група ПАР – амфотерні (амфолітні) електроліти. Амфолітні ПАР утримують дві функціональні групи, одна з яких має кислий, а друга лужний характер, наприклад, карбоксильну і амінну групи. Залежно від середовища амфолітні ПАР мають аніонні або катіонні властивості.
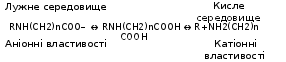
Таблиця 4.1
|
№ з/п |
Тип сполук |
Характерний представник |
Формула |
|
Аніоноактивні ПАР | |||
|
1 |
Мило |
Стеарат натрію |
СН3 (СН2)16СОО–·Nа+ |
|
2 |
Сульфатовані спирти |
Лаурилсульфат натрію |
СН3 (СН2)10СH2O SO3–·Nа+ |
|
3 |
Ефіри |
– |
R (OCH2CH2)n OSO3–·Nа+ |
|
4 |
Сульфатовані карбонові кислоти |
Nа – солі сульфатованої олеїнової кислоти |
|
|
5 |
α- олефінсульфонати |
– |
RСН = СНSO2О–·Nа+ |
|
6 |
Нафтові сульфонати |
– |
Утримують SO3– і Nа+ |
|
7 |
Сульфовані ароматичні вуглеводні |
Лінійні алкіл-бензолсульфанати натрію |
|
|
8 |
Сульфовані ефіри |
Nа – лаурил- сульфоацетат |
СН3(СН2)10СН2ОСОСН2SO3–·Nа+ |
|
9 |
Сульфовані аміди |
–– |
|
|
10 |
Сульфовані оксіетілі-ровані алкілфеноли |
–– |
RC6H4O(CH2CH2O)n·CH2CH2 SO3–·Nа+ |
|
11 |
Ациловані аміно-кислоти |
–– |
|
|
12 |
Металалкілфосфати |
Натрійалкілпол-фосфат |
Nа5R5(P3O10)2 |
|
Катіоноактивні ПАР | |||
|
13 |
Четвертинні амонійні солі |
Первинні аміни |
|
|
Вторинні аміни |
| ||
|
Третинні аміни |
| ||
|
14 |
Ацетиловані аміни |
–– |
|
|
15 |
Солі бензиламонія |
–– |
|
|
Неіоногенні ПАР | |||
|
16 |
Ефіри багатоатомних спиртів та вищих кислот |
Моногліцерин стеарат |
CH2OHCHOHCH2OOC(CH2)16CH3 |
|
17 |
Оксиетиловані аміни |
–– |
|
|
18 |
Оксиетиловані вищі жирні кислоти |
Поліетиленгликольмоностеарат |
СН3(СН2)10 СН2СОО(СН2СН2О)nСН2СН2ОН |
|
19 |
Ефіри поліалкіленгликолей та алкілфенолів |
Поліоксіетиленалкілфенол |
|
|
20 |
Продукти конденсації жирних кислот і алканоламінів |
Діетаноламін стеарат |
|
|
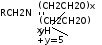
21 |
Третинні ацетиленові гликолі |
4,7-диметил- 5-децин-4,7-діол |
|
|
22 |
Поліоксиетировані алкілфосфати |
–– |
С8Н17OP(О)[(OCH2CH2)n х OCH2CH2OH]2 |
|
Амфолітні ПАР | |||
|
23 |
Бетаїни |
–– |
RCHCOO–∙Na+;
+N(CH3)3∙Cl–
|
|
24 |
Амінокислоти
|
–– |
|
До амфотерних ПАР відносяться білки, що вміщують групи – СОО– і NH+3 . Отримані синтетичні амфоліти - сополімери акрилової кислоти і вінілпіридину, а також сополімери глютамінової кислоти і лізину. Схематично молекулу амфолітного ПАР можна подати у вигляді
HONH3 – R – COOH
Таким чином, ПАР можна згрупувати за наступними класами:
аніоноактивні речовини;
катіоноактивні речовини;
неіоногенні речовини;
амфотерні речовини, що виявляють властивості як аніоноактивних, так і катіоноактивних поверхнево-активних речовин;
емульгатори, нерозчинні у воді, і такі різні речовини, що включають холестерин, стеариновий спирт і ін.;
речовини ПАР в неводних середовищах.