- •Розділ 1
- •1.2. Фізико-хімічна механіка як наукова дисципліна, її задачі
- •1.3. Дисперсні системи. Класифікація дисперсних систем з позицій фізико-хімічної механіки композиційних матеріалів
- •1.3.6. Періодичні колоїдні системи.
- •1.4. Особливості властивостей колоїдних систем
- •1.5. Короткий історичний огляд
- •Розділ 2
- •2.2. Змочування і набухання
- •2.3. Спонтанні процеси на межі розділу фаз
- •Розділ 3
- •3.2. Теорія мономолекулярної адсорбції Ленгмюра
- •3.3. Полімолекулярна адсорбція
- •3.4. Рівняння Гіббса. Двомірний тиск
- •3.5. Правило Дюкло-Траубе
- •3.6. Адсорбція на межі тверде тіло – розчин
- •Розділ 4
- •4.2. Класифікація пар за хімічною будовою
- •4.3. Аніоноактивні пар
- •4.4. Катіоноактивні пар
- •4.5. Класифікація пар за механізмом дії
- •4.6. Термодинамічні, поверхневі й об'ємні властивості розчинів пар у зв'язку зі стійкістю дисперсних систем
- •4.7. Використання пар в техніці
- •Розділ 5
- •5.1.1. Будова подвійного електричного шару (пдеш)
- •5.2. Стійкість і коагуляція дисперсних систем
- •5.3. Седиментаційна (кінетична) стійкість
- •5.4. Процеси стабілізації дисперсних систем і їхня роль у техніці
- •Розділ 6
- •6.2. Загальні відомості про структуроутворення в дисперсних системах
- •Розділ 7
- •7.2. Методи реологічного моделювання
- •7.3. Криві течії і в'язкості
- •7.4. Методика побудови реологічних кривих
- •7.5. Моделі і рівняння течії структурованих дисперсних систем
- •7.6. Про реологічні криві течії і в'язкості структурованих рідин на прикладі цементобетонних сумішей
- •Іі частина
- •8.2. Розчинення в'яжучих речовин
- •8.3. Основні закономірності кінетики кристалізації нової фази з пересичених розчинів і фазовий склад цементного каменю
- •8.4. Формування структури цементного каменю
- •Розділ 9
- •9.2. Основні параметри вібраційного ущільнення бетонної суміші
- •9.3. Вібродиспергування та виброперемішування суміші
- •9.4. Основи технології виробництва дорожніх бетонів на основі органічних в'яжучих
- •9.4.2. Принцип та метод визначення температури перемішування сумішей
- •9.4.3. Температурні параметри приготування сумішей
- •9.4.4. Змочування кам'яних матеріалів в'яжучим як фактор якості перемішування
- •9.4.5. Зміст процесу ущільнення асфальтобетону.
- •9.4.6. Шляхи інтенсифікації ущільнення сумішей
- •Розділ 10
- •10.1. Склад, структура і властивості кам'яновугільних дорожніх дьогтів
- •10.2 Склад, структура і властивості нафтових дорожніх бітумів
- •10.3. Бітумні емульсії
- •10.3.2. Бітумні емульсії – мікрогеторогенні дисперсні системи
- •10.3.3. Технологія виробництва
- •Технічна характеристика диспергатора дб – 1
- •Технічна характеристика триступеневого диспергатора
- •10.3.4. Фізико-механічні властивості та технологічні вимоги.
- •10.3.5. Галузі застосування.
- •Бітумополімерні в’яжучі і асфальтобетони на їх основі
- •Розділ 11
- •11.2. Дьогтебетон
- •11.3. Асфальтобетон
- •11.3.1. Утомленісна довговічність асфальтобетонів і роль агресивних середовищ
- •11.4. Дьогтебетони і асфальтобетони з комплексно-модифікованою мікроструктурою
- •Рекомендована література до вивчення теоретичного матеріалу
5.1.1. Будова подвійного електричного шару (пдеш)
Згідно з Штерном, що об’єднав схеми будови ПДЕШ Гельмгольца-Перрена і Гуі-Чепмена, перший шар (рис. 5.4.) чи навіть декілька перших шарів протиіонів притягаються до поверхні агрегату під впливом як електростатичних, так і адсорбційних сил. У результаті цього частина протиіонів утримується поверхнею на дуже близькій відстані, порядку 1-2 молекули, що утворюють плоский конденсатор товщиною δ. Цей шар, у якому спостерігається різке падіння електричного потенціалу, – адсорбційний шар (гельмгольцівський, штернівський).
Інші протиіони, що потрібні для компенсації потенціалвизначальних іонів, у результаті теплового руху утворюють дифузійну частину подвійного електричного шару.
Зі схеми видно повне падіння потенціалу φδ у дифузійній частині подвійного шару і різницю потенціалів (φ0-φδ) між обкладками конденсатора. Місце границі ковзання в цьому шарі залишається дотепер неясним (на схемі границя ковзання позначена лінією АВ).

Рис. 5.4. Подвійний електричний шар за Штерном і падіння в ньому потенціалу
Зрозуміло, що введення електролітів в систему приведе до того, що дифузійний шар буде стискуватися і все більше протиіонів буде попадати у адсорбційний шар. Подвійний електричний шар, згідно поглядам Штерна, при цьому усе більше наближається до шару, передбаченому у теорії Гельмгольца-Перрена, ξ – потенціал зменшується, поступово наближаючись до нуля. При розріджуванні системи, навпаки, дифузний шар розширюється і ξ – потенціал збільшується.
На розподіл іонів у подвійному електричному шарі за теорією Штерна сильно впливає природа протиіонів. Якщо протиіони мають різну валентність, то товщина дифузійного шару і число протиіонів у адсорбційному шарі визначаються, головним чином, валентністю іонів і, отже, обумовлюються електростатичними силами. Зрозуміло, що дифузійний шар тим тонше і ξ – потенціал тим нижче, чим більше валентність протиіонів.
Якщо протиіони мають однакову валентність, то товщина подвійного електричного шару і кількість протиіонів у дифузійному шарі визначається специфічною адсорбційною спроможністю іонів, обумовленою їх поляризовністю і гідратацією. Ці властивості іонів визначаються за їх дійсним радіусом, розташуванням відповідних елементів у таблиці Д.І. Менделєєва.
Більша поляризовність іону повинна сприяти зменшенню товщини подвійного електричного шару, оскільки при цьому виникають додаткові адсорбційні сили між твердою фазою і індукційним диполем і, крім того, він може більш близько підійти до поверхні. Так як деформованість іону збільшується з його розмірами і оскільки радіуси аніонів взагалі значно більше радіусів катіонів, поляризовність аніонів (α) звичайно більша, ніж катіонів.
|
Катіон |
α ·1024, см3 |
|
Аніон |
α ·1024, см3 |
|
Li+ |
0,03 |
|
F– |
0,96 |
|
Na+ |
0,19 |
|
Cl– |
3,60 |
|
K+ |
0,89 |
|
Br– |
5,00 |
|
Rb+ |
1,50 |
|
I– |
7,60 |
|
Cs+ |
2,60 |
|
|
|
В цьому, між іншим криється пояснення того, чому негативний заряд поверхні зустрічається у природі значно частіше, ніж позитивний.
Гідратація іонів, як відомо, зменшується зі зростанням справжнього радіуса іонів. Зниження гідратації іонів повинно сприяти стисканню подвійного електричного шару, так як гідратна оболонка зменшує електростатичну взаємодію між протиіонами і поверхнею твердої фази.
Із усього наведеного стає зрозумілим, чому здатність стискувати подвійний електричний шар і зменшувати ξ – потенціал зростає у ряду катіонів від Li+ до Cs+, а в ряді аніонів від F– до I–.
Ємність подвійного шару С визначається, як ємність двох послідовно розташованих конденсаторів за формулою (5.4):
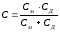 (5.4)
(5.4)
де: См – ємність молекулярного конденсатора; СД – ємність дифузійного шару. Ємність молекулярного шару См дорівнює відношенню заряду стінки σ до різниці потенціалів φ0 – φδ
См = σ / (φ0 – φδ) (5.5)
Величина См майже постійна, а величина Сд сильно залежить від концентрації електроліту, тому характер падіння потенціалу у подвійному електричному шарі також залежить від кількості електроліту, що знаходиться у системі. Таким чином, якщо навіть потенціал φ0 є постійним, то φδ, значення якого визначається станом дифузійного шару, знижується із зменшенням товщини іонної атмосфери (рис. 5.4).
Якщо ємність одного із двох конденсаторів значно більше ємності іншого, то повна ємність практично рівна меншій складовій. Так, у розведених розчинах С ≈ С∂, а у концентрованих С ≈ См .
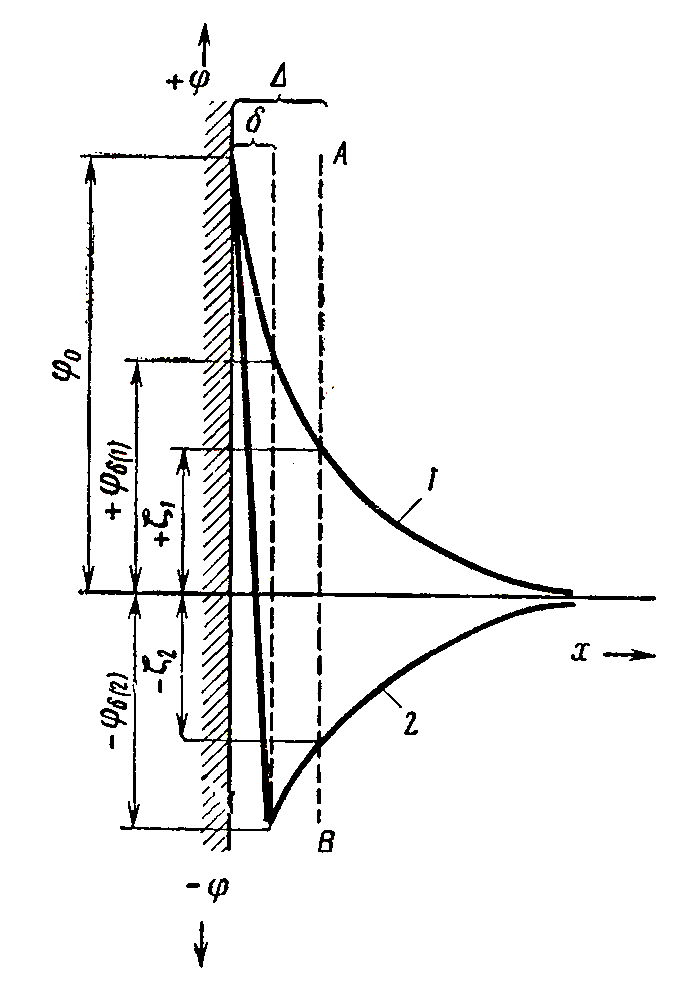
Значення ємності подвійного електричного шару, що розраховано за теорією Штерна з урахуванням радіусів іонів, виявляються близькими до знайдених експериментально. Це може пояснити причину зміни знака електрокінетичного потенціалу при введенні у систему багатовалентних іонів, заряд яких протилежний за знаком заряду дисперсної фази. Такі багатовалентні іони утягуються у адсорбційний шар у результаті як сильних електростатичних взаємодій, так і із-за велику адсорбованість, що пов’язана з поляризованістю таких іонів. Іони можуть адсорбуватися у такій кількості, що не тільки нейтралізують заряд твердої поверхні, але і перезаряджають колоїдну частку. У результаті, як це видно з рис. 5.5, характер падіння потенціалу у подвійному електричному шарі може зміниться корінним чином, а φδ і ξ – потенціали, що мають той же знак, що і φ – потенціал (на схемі φδ(І) і ξІ), міняють знак на протилежний (на схемі φδ(2) і ξ2). При цьому, звичайно, потенціал φ0 остається постійним, так як чужорідні іони не спроможні добудовувати кристалічну решітку твердої фази. Таким чином, утворюється становище, коли φ0 і ξ – потенціали будуть мати різні знаки. Зрозуміло, що подальше підвищення концентрації електроліту у системі повинно приводити до стискання дифузійного шару і падіння ξ – потенціалу.
|
|
Рис. 5.5. Зміна падіння потенціалу подвійного електричного шару при перезарядці за допомогою іонів, що сильно адсорбуються: 1 – падіння потенціалу до перезарядки; 2 – падіння потенціалу після перезарядки
|
Для перезарядки частинок, що мають негативний ξ – потенціал, особливо часто використовують багатовалентні іони алюмінію і торію.