
конспекты / ------------------
.pdf
211
Якщо потрібно тільки зменшити швидкість полімеризації, а не зупинити процес остаточно, застосовують спеціальні речовини - замедлители. Характер дії інгібіторів і замєдлітелів практично однаковий, а розходження між ними скоріше кількісне, чим якісне.
Методом радикальної полімеризації отримані такі відомі полімери, як полівенилхлорід, полістирол, бутадієнстирольні каучуки, поліметилметакрилат і ін. По активності при радикальній полімеризації мономери можна розташувати в такий ряд:
бутадієн > стирол >метилметакрилат>акрилонитрил> винилхлорид
. Іонна полімеризація
Якщо в радикальній полімеризації активним центром є радикал, то в іонної - іони. Полімеризація, при котрої її активний центр - заряд іона - передається послідовно по макромолекулярної ланцюзі при її рості,
називається іонною полімеризацією.
Іонна полімеризація, як і радикальна, - ланцюговий процес. Проте макромолекула , що рості , при іонній полімеризації на відміну від радикальної являє собою (у процесі росту) не вільний радикал, а іон - катіон або аніон. У залежності від цього розрізняють катіонну (карбонієву) і аніонну (карбаніонну) полімеризацію.
Іонна полімеризація протікає при каталізаторів, що сприяють утворенню іонів. Але на противагу ініціаторам смердоти не входять до складу полімеру, тобто не витрачаються в процесі полімеризації. Іонна полімеризація називається також каталітичною полімеризацією.
Особливість іонної полімеризації - її дуже скроні швидкість при низьких температурах (від -50 до —70°С). Ця швидкість залежить від полярності середовища, у якому протікає полімеризація.
Іонна полімеризація, як і радикальна, протікає через трьох основні стадії.
Катіонна (карбонієва) полімеризація. Цей тип полімеризації протікає через утворення катіонів. У цьому випадку використовують каталізатори, що володіють электроноакцепторними властивостями. Приєднуючи молекулу мономера, смердоти утворять катіон - іон карбонія. У якості речовин, що каталізують катіонну полімеризацію, можуть виступати кислота і каталізатори Фриделя—Крафтса (А1С1з, ВFз, ТiСl4 і ін.). Катіонну полімеризацію можна прискорити за допомогою добавок - сокаталізаторів (вода, кислоти й інші речовини, що є донорами протонів). Сокаталізатори істотно впливають на активність каталізатора. При таких добавок катіонну полімеризацію можна уявити у виді таких елементарних реакцій (стадій).
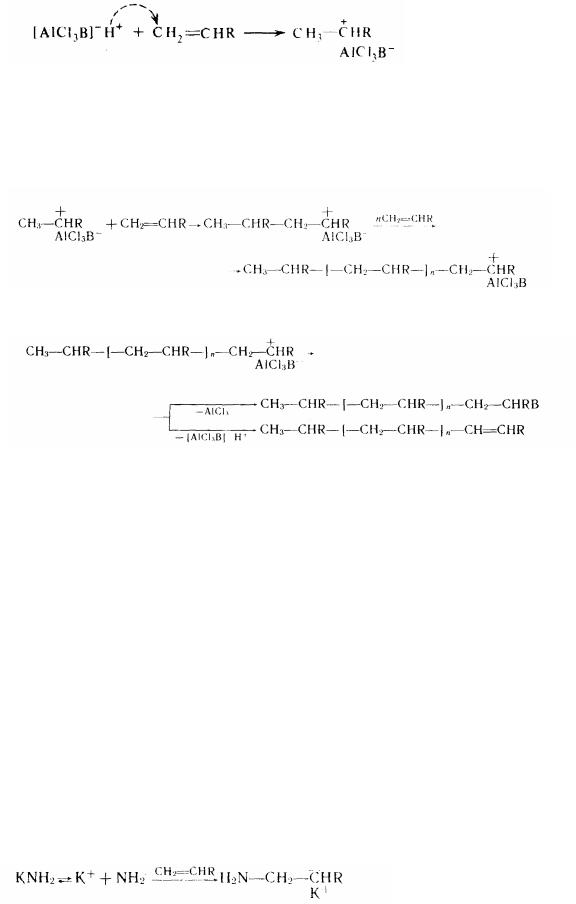
1. ініциюваннє. На цій стадії відбувається взаємодія каталізатора (А1С1з) і сокаталізатоуа (НВ) з утворенням комплексного з'єднання, що виявляє властивості сильної кислоти:
Ця кислота, отдавая протон молекулі мономера, перетворює його в карбонієвий іон, урівноважений комплексним протівоіоном (іонна пару):
212
Слід зазначити, що сокаталізаторами можуть бути тільки ті речовини, що взаємодіють із каталізаторами. Роль сокаталізатора багато в чому залежить від характеру реакційного середовища.
2.Ріст ланцюга. У процесі росту ланцюга поляризовані молекули мономера приєднуються до іона , що рості, «упроваджуючись» між макрокарбкатіоном (із бокові його зарядженої частини) і протівоіоном (А1С1зВ-):
3.Обрив цілі. Ріст ланцюга припиняється в результаті відщеплення
(регенерації) від іона комплексної кислоти, що рості, або каталізатора:
У результаті обриву ланцюга каталізатор знову виділяється у вільному виді. Сумарна швидкість катіонної полімеризації прямо пропорційна концентрації каталізатора, а середній ступінь полімеризації від концентрації каталізатора не залежить, але прямо пропорційна концентрації мономера: υ = κ [ДО]; Р=κ ’[М], де [ДО] -концентрація каталізатора; [М] -концентрація
мономера.
По реакційній спроможності при проведенні атіонної полімеризації деякі мономери можна розташувати в ряд:
ізобутилен > ізопрен > стирол > бутадієн
Аніонна (карбаніонна) полімеризація. Ця полімеризація протікає через стадію утворення карбаніона. Каталізаторами цього типу полімеризації служать электронодонорні речовини - підстави, лужні метали, металлорганічні з'єднання (бутіллітій, бутілнатрій, трифенилметілнатрій, А1(С2Н5)з і його комплекси й ін.), гідриди металів (Li, Nа), амід калію КNН2. Активними каталізаторами є також продукти, що утворяться при пропусканні олефінов через суміш натрійалкіла, алкоголята і галогеніду натрію, - «алфінові каталізатори» (від слів «алкоголят» і «олефін»).
Розглянемо механізм аніонної полімеризації при каталізатора (RNН2) у середовищі рідкого аміаку.
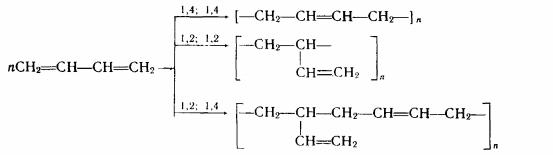
1. ініциювання:
Для металоорганічних сполук (R'—Nа) утворення активного центру відбувається шляхом упровадження мономера по поляризованому зв'язку

213
метав - вуглець:
Электроноакцепторні заступники (R) у молекулі мономера сприяють приєднанню аніона. Оттягівая електронну щільність, смердоти створюють дефіцит електронів на кінці молекули, до якого приєднується негативно заряджена група (NН2 або R'-). Тому в реакції аніонної полімеризації активно беруть долю мономери, що мають поляризовані подвійні зв'язки (стирол, метилметакрилат, акрілонітрил, метакрилонітрил і ін.).
2.Ріст ланцюга:
Упроцесі цієї реакції, як і при каталітичній полімеризації, мономер займає місце між макрокарбаніоном і протівоіоном.
3. Обрив ланцюга. Реакція передачі ланцюга на розчинник або на мономер може викликати припинення росту макромолекулярного ланцюга:
Встановлено, що швидкість аніонної полімеризації пропорційна квадрату концентрації мономера і кореню квадратному з концентрації каталізатора: υ =κ [М2]√[ДО], де [М] -концентрація мономера; [ДО] - концентрація каталізатора. На активність кінця макромолекули, що рості, зарядженої негативно, впливає будівля попередніх йому ланк макроцепи. Активність карбаніона значно знижується зі збільшенням стеричного впливу (наприклад, напруги) в окремих ділянках макромолекули.
У якості каталізатора аніонної полімеризації часто виступають лужні метали. Смердоти сприяють окисно-відбудовним реакціям, що протікають між цими металами і мономерами. Металлорганічні з'єднання, що утворяться, каталізують подальший ріст макромолекулярного ланцюга:
Полімеризація в цьому випадку протікає на поверхні лужного металу (натрію). Мономер (бутадієн), адсорбіруясь на металі, поляризуеться і реагує з карбаніоном. Проте образующієся натрийбутадієновий (і натрийізопреновий) каучук нестереорегулярен.
Вперше синтез каучуку з бутадієну методом аніонної полімеризації з застосуванням металевого натрію в промислових масштабах був здійснений у СРСР.
Мономері, що вступають в аніонну полімеризацію, по реакційній активності
214
можна розташувати в ряд:
акрілонітрил > метакрилонітрил > метилметакрилат > стирол > бутадієн Слід зазначити, що стирол і дієни (наприклад, бутадієн) - мономери, спроможні однаково добрі полімерізоватися під впливом як вільних радикалів
(радикальна полімеризація), так і іонів (іонна полімеризація).
Аніонна-координаційна полімеризація і стереорегулярні полімери
У 1953 р. були відкриті нові каталізатори аніонної полімеризації. Смердоти являють собою комплекси металлорганічних з'єднань із солями перехідних металів. Такі каталізатори, відомі як каталізатори Циглера - Натта, мають надзвичайно високою полімерізаційна активність. Полімеризація, збуджена такими каталізаторами, називається аніонною-координаційною полімеризацією.
Найбільше відомі каталізатори цього класу - комплекси триетілалюмінія із солями титана:
А1(С2Н5)з+ТiСl4 (або ТiС1з). Ці каталізатори дозволили спростити і полегшити технологію одержання багатьох полімерів. Наприклад, для синтезу поліетілену без таких каталізаторів потре буваються жорсткі умови (тиск 150-250 МПа, температура біля 300°С). Застосовуючи каталізатори Циглера—Натта, поліетилен одержують при тиску, що не перевищує 1 МПа, і температурі не вище 60°С. Поліетилен, синтезований без каталізаторів Циглера—Натта, називають
поліетиленом високого тиски на противагу поліетилену низького тиску (із каталізатором).
Властивості поліетилену, отриманого при низькому тиску, відрізняються від властивостей поліетилену, отриманого при високому тиску. Поліетилен високого тиску - більш еластичний і гнучкий, при розтягу він утворить прозору плівку. Поліетилен низького тиску прочнійш і жестче, його щільність вище, чим у поліетилену високого тиску.
Ще більш важливу роль каталізатори Циглера—Натта зіграли в одержанні полімерів із високорегулярним будівлею. Тому їх часто називають
стереоспецифіними каталізаторами.
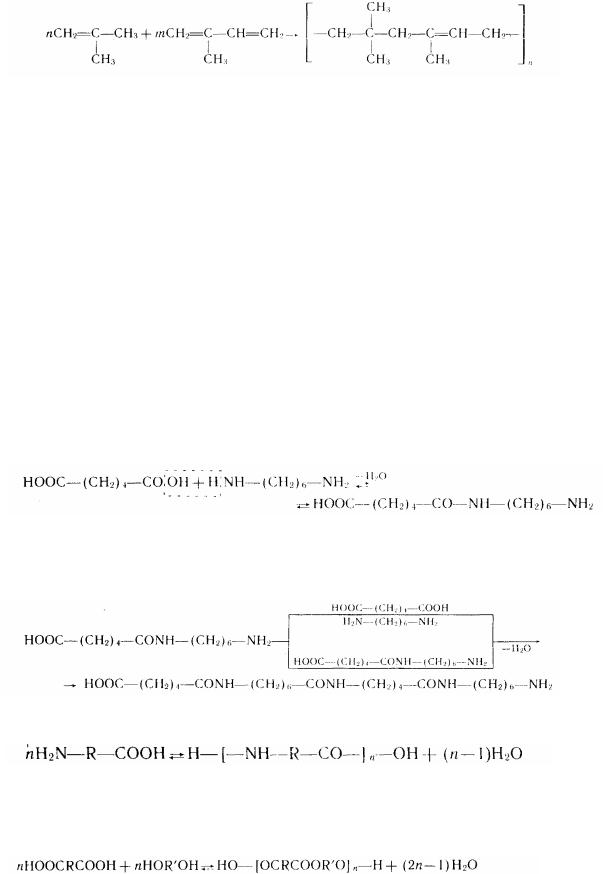
Відомо, наприклад, що при звичайній полімеризації бутадієну приєднання його молекул друг до друга може відбуватися в 1,2-ілі 1,4-положенні. У тієї ж час можливо одночасне приєднання однієї молекули в 1,2-положення, а другой-в 1,4-положення:
Застосування каталізаторів Циглера—Натта дозволяє синтезувати практично 100%-ний стереорегулярній (пространственно упорядкований) полібутадієн із полімеризацією мономерів тільки в 1,4-положенні і створенням цис-конфигураці в кожній елементарній ланкі (1,4-цис-полібутадієн)*. По деяких показниках цей

215
полімер мало відрізняється від натурального каучуку, а по стійкості до старіння навіть перевершує його. Цим же методом можна одержувати ізотактичний поліпропілен, а також поліізопрен (1,4-цис-полиизопрен), що служити синтетичним замінником натурального каучуку.
Крім стереоізомерії великий вплив на властивості полімеру робить ізомерія, пов'язана з формою макроцепи. Наприклад, використовуючи каталізатори Циглера - Натта, можна синтезувати поліетилен строго лінійної будівлі (практично без бічних відгалужень), що має велику щільність, кристалічність і більш скроні температуру плавлення.
Каталізатори Циглера - Натта - гетерогенні каталізатори, поверхня яких впливає на орієнтацію молекул мономера при полімеризації. Так, утворення стереорегулярних полімерів при полімеризації олефінов можливо тільки при гетерогенному каталізі. Правда, деякі стереорегулярні полімери можуть утворитися й у відсутність таких каталізаторів - у гомогенних середовищах, а також при дотриманні визначених розумів (при протіканні реакцій по свободнорадікальному або катіонному механізмі).
Механізм аніонної-координаційної полімеризації можна уявити такою уявою. При взаємодії А1(С2Н5)3 і ТiС14 утвориться активний комплекс:
комплекс що
випас із розчину ТiСl3 адсорбирується поверхнею хлордіетілалюмінія, створюючи центри активації, до яких приєднуються молекули мономера шляхом упровадження між атомом алюмінію і етильної групи. Всі наступні акти приєднання мономерів протікають із подовженням углеводородної ланцюга комплексу:
При розпаді комплексу утвориться суміш високомолекулярних продуктів стереорегулярного будівлі:
Стереорегулярні полімери (наприклад, 1,4-цис-поліізопропен) утворяться і при використанні літійорганичних каталізаторів (бутіллітія, бутілнатрію й ін.). При цьому утворення активного центру можна уявити у виді

216
Ступінчата полімеризація
Цей вид полімеризації відрізняється від ланцюгової полімеризації палимо, що процес протікає шляхом поступового (ступенчата) приєднання молекул мономера друг до друга за рахунок переходові рухливого атома водню (або групи атомів) від мономера до що росте макроцепи. Тому в реакцію східчастої полімеризації вступають такі поліфункціональні мономери, що містять або рухливий атом водню, або групу, спроможну його приєднати. Роздивимося, наприклад, утворення поліуретану:
поліуретан
Проміжні з'єднання, що утворені поступовим приєднанням молекул мономера друг до друга, цілком стійкі. Східчаста полімеризація каталізірується водою, кислотами, луками і солями.
Сополімеризація
Сополімеризація - процес утворення сополімеров спільною полімеризацією двох або декількох різноманітних по природі мономерів. Цим методом одержують високомолекулярні з'єднання із широким діапазоном фізичних і хімічних властивостей. Наприклад, у результаті сополімеризацї бутадієну з акрилонітрилом утвориться бутадієннітрильний каучук (СКН), що володіє високою стійкістю до олій і бензинів. З нього виготовляють уплотнітельні прокладки для деталей, що стикаються з оліями і розчинниками:
Сополімеризацієй ізобутілену з ізопреном утворюється бутилкаучук із високою газонепроникністю:
217
При сополімерізації мономери можуть поводитися декілька інакше, чим при їхній роздільній полімеризації. У цьому випадку виявляється взаємний вплив різноманітних мономерів, у результаті чого реакційна спроможність одного з них сильно залежить від природи іншого. Процес із полімеризації ще більш ускладнюється, якщо в реакції беруть долю декілька мономерів.
ПОЛИКОНДЕНСАЦИЯ
Поліконденсація - процес утворення полімерів шляхом хімічної взаємодії молекул мономерів, що супроводжується виділенням низькомолекулярних речовин (води, хлороводороду, аміаку, спирту й ін.).
У процесі поліконденсації відбувається взаємодія між собою функціональних груп, що утримуються в молекулах мономерів (—ОН,
—СООН, —NН2, галогени, рухливий водень і ін.). Мономері, що вступають у реакцію поліконденсації, повинні бути не менше чим біфункціональними.
Призведемо приклади деяких реакцій поліконденсації. При реакції адіпінової кислоти з гексаметілендіаміном на першій стадії утвориться стійке з'єднання з тієї ж функціональністю (тобто біфункціональне):
При подальшій поліконденсації процес нарощування полімерного ланцюга може йти різноманітними шляхами: або взаємодією дімера , що утворився, з одним або двома різноманітними мономерами, або реакцією між окремими фрагментами майбутнього полімеру:
У результаті реакції утвориться поліамід (поліамід-6,6). Амінокислоти, реагуючи один з одним, також утворять поліаміди:
Реакція між двухосновнимі кислотами і двохатомними спиртами призводить до одержання поліефірів, із яких найбільше значення мають поліефіри на основі духмяних і непредельних двухосновних кислот:
Для прискорення реакції поліконденсації застосовуються каталізатори - органічні і мінеральні кислоти (оцтова, молочна, бензойна, соляна і сірчана).
Основні закономірності і відмінні риси реакції поліконденсації

218
По характері функціональних груп, що взаємодіють між собою при поліконденсації, мономери діляться на:
1.Мономері з взаємодіючими однорідними функціональними групами. Реакція поліконденсації може здійснюватися між молекулами того самого мономера:
2.Мономері, що містять у молекулі взаємодіючі різнорідні функціональні групи:
3.Мономері з однорідними функціональними групами, що не взаємодіють. Реакція поліконденсації протікає лише при взаємодії між собою мономерів, що мають функціональні групи одному типу:
4.Мономері з різнорідними функціональними групами , що не взаємодіють, наприклад Н2N-R-ОН (аміноспирт). Такі мономери для синтезу полімерів застосовуються рідко.
Якщо в поліконденсації беруть долю однотипні мономери, то такий процес називається гомополіконденсацією:
Увипадку різнотипних мономерів має місце гетерополіконденсація:
Відомо, що структура макромолекулярного ланцюга полімерів визначається функціональністю мономерів. У випадку біфункціональних мономерів при поліконденсації утворяться лінійні полімери (лінійна поліконденсація}. Якщо в поліконденсацію вступають мономери з функціональністю, рівної трїм і більш, ті утворяться розгалужені або просторові полімери. Така поліконденсація називається просторової. Чим більше функціональних груп містить мономер, палимо полімер, що більше утвориться, схожий на жорстку просторову сітку з високим щаблем поперечного зшивання. Прикладом такої структури може служити полімер, отриманий із гліцерину і фталевої кислоти.
Для процесу поліконденсації має значення не тільки природа і число функціональних груп у молекулі мономера, але і відстань між ними. Справа в тому, що при взаємодії функціональних груп, відділених друг від друга трьома або чотирма атомами вуглецю, може утворитися (на першій стадії) замість лінійної молекули циклічне з'єднання (пьятиабо шестичленный цикл), стійке відповідно до теорії напруги Байера. Наприклад, із γ -гідроксімасляної кислоти в результаті внутримолекулярної конденсації утвориться замість полімеру циклічний бутіролактон:
γ- гідроксімасляна |
бутіролактон |
кислота |
|
Циклічна структура може виникнути й у результаті межмолекулярної

219
конденсації:
Циклізація утрудняється зі збільшенням відстані між функціональними групами, у результаті чого утворяться малостійкі цикли. Таким чином, спроможність біфункціональних мономерів до циклізації залежить від напруженості утворюючого циклу, що, у свою чергу, визначається відстанню між функціональними групами.
Крім того, на процес поліконденсації і на реакційну спроможність мономерів впливає також і розташування функціональних груп. Наприклад, внутримолекулярна циклізація стає неможливої, якщо дві функціональні групи знаходяться в n-положенні бензольного каблучки, У тієї ж час циклізація відбувається, якщо ці групи знаходяться в о-положенні. Впливають і сферичні чинники. Так, якщо в о-положенні присутні нереакціонноспособний заступник мішаючи або друг другу в просторі функціональні групи, те це позначається і на процесі поліконденсації Наприклад, близькість аміногруп в о-фенілендіаміне сприяє утворенню циклічних продуктів, що призводить іноді до повного припинення лінійної поліконденсації.
Отже, циклізація утрудняє, а часто і взагалі перешкоджає процесу поліконденсації в цілому. Тому при введенні в цю реакцію мономерів необхідно враховувати їхню спроможність до побічних реакцій, зокрема до циклізації.
Поліконденсація також складається з трьох основних стадій.
1. Утворення активних центрів (функціональних груп).
Як правило, при поліконденсації вихідні мономери вже містять активні функціональні групи. Проте буває і так, що ці групи створюються безпосередньо в процесі поліконденсації. Наприклад, при синтезі фенолоформальдегідних полімерів активні центри (метилольні групи) утворяться при взаємодії фенолу з формальдегідом:
Ці групи потім вступають у реакцію піл і конденсації між собою.
2. Ріст ланцюга. У процесі росту ланцюга відбувається виділення низькомолекулярних речовин. Це призводить до тому, що склад елементарних ланк полімер, а не відповідає складу вихідного мономера. У цьому полягає одне з основних відмінностей реакції поліконденсації від реакції полімеризації.
Особливістю стадії росту ланцюга при поліконденсації є незалежність окремих актів росту ланцюга друг від друга. Тому процес поліконденсації можна уявити як суму однотипних реакцій, що відбуваються між молекулами мономера, дімера, тримера і т.д.
3. Припинення росту й обрив ланцюга. Друга характерна рису реакції поліконденсації - її оборотний характер. При досягненні стани рівноваги швидкість утворення полімеру на кожній стадії взаємодії мономерів дорівнює швидкості його руйнації (деструкції). Для одержання полімерів із великою молекулярною масою необхідно порушувати цю рівновагу, удаляя
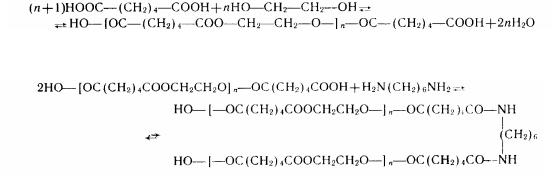
220
виділяющієся в процесі поли конденсації низькомолекулярні продукти. Для цього або підвищують температуру реакційного середовища, або процес ведуть при зниженому тиску. Перше необхідно для зниження грузькості реакційного середовища, що зростає в міру плину реакції поліконденсації, а до зниження тиску в реакторі удають, щоб скроні температура не руйнувала полімер. Таким чином, молекулярна маса полімеру і швидкість поліконденсації залежать від положення рівноваги. Воно, у свою чергу, визначається концентрацією мономера, температурою, каталізатором і т.д.
Процес поліконденсації може припинитися з багатьох причин: унаслідок сталого рівноважного стана, зміни структури і порушення еквівалентності функціональних груп, збільшення грузькості реакційного середовища і пов'язаного з цим зменшення рухливості макромолекул.
Продукти поліконденсації являють собою складну суміш. У її склад можуть входити фракції полімер гомологів, низькомолекулярні з'єднання, деяка кількість мономерів , що вступили не в поліконденсацію , і навіть побічні продукти
.Сополіконденсація і блок-сополіконденсація
Для одержання полімерів із різноманітними і корисними властивостями в реакцію поліконденсації вводять декілька різноманітних по природі мономерів. Така реакція поліконденсації називається з про поліконденсацією або спільною поліконденсацією. У результаті утворяться полімери, макромолекулі яких побудовані з ланк, що подають залишки всіх мономерів, узятих для проведення поліконденсації. До складу макромолекул ці залишки входять звичайно у випадковому сполученні, без визначеного порядку. Для одержання полімерів із регулярним розташуванням таких ланк надходять такою уявою. Спочатку з двох мономерів синтезують порівняно низькомолекулярні гомополімери - блоки. Потім їх з'єднують між собою ланками третього мономера. Такий процес називається блоксополіконденсацієй. Наприклад, реакцію спільної поліконденсації діамінов із стати і еф і рам і починають із попередньої стати і конденсації адіпінової кислоти з етіленгликолем. При цьому необхідний деякий надлишок адіпінової кислоти. У результаті утворяться порівняно низькомолекулярні блоки, що мають на обох кінцях макромолекули карбоксильні групи:
Додаючи потім гексаметилендіамін, «зшивають» ці блоки й одержують блок-сополімер - поліефірамід:
ЛЕКЦІЯ 17
Хімічні перетворення полімерів
Хімічні реакції високомолекулярних з'єднань в основному мало відрізняються
