
конспекты / ------------------
.pdf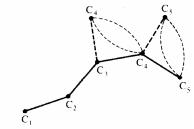
201
своєї скручености.
Малий. 36. Скроні гнучкість макромолекули виникає в результаті обертання атомів вуглецю навколо простої а-связі
Текучість полімерів, грузькість їхніх розчинів і поводження при впливі механічних навантажень залежать від молекулярної маси і гнучкості макромолекул.
Гнучкість ланцюгових макромолекул - відмітна і важлива характеристика високомолекулярних з'єднань, що визначає весь комплекс їхніх особливих властивостей. Завдяки гнучкості макромолекули постійно змінюють свою конфігурацію. Зміна форми макромолекули відбувається звичайно або як результат обертальних коливань її окремих частин біля положень, що відповідають мінімумам енергії, або в результаті стрибкоподібних обертальних переходів від однієї конформації до іншої.
Простий зв'язок, як відомо, припускає обертання однієї частини молекули щодо інший без деформації валентних рогів або хімічних зв'язків. У випадку макромолекул таке обертання призводить до виникнення множини різноманітних конформації нерегулярної форми. Це пояснюється палимо, що таке обертання може відбуватися навколо великого числа послідовно розташованих простих зв'язків у ланцюзі (малий. 36). Якщо уявити, що три атоми вуглецю (С1, С2 і С3) молекули лежати в одній площині, те атом С4 може займати будь-яку точку по краю окружності «конуса», утвореного обертанням біля зв'язку С2—С3 як осі обертання. Ті ж ставитися і до атому С5 при його вільному обертанні навколо простого зв'язку С3—С4. У випадку дуже довгої молекули полімеру в результаті таких довільних поворотів навколо множини простих зв'язків форма макромолекули буде досить складної, із високим щаблем асиметрії. Таку лінійну макромолекулу можна уявити у виді поплутаного клубка шерсті. Проте, як відомо, внутрішнє обертання навколо простих зв'язків не зовсім вільно. Це пов'язано з різноманітними стеричними перешкодами, що виникають унаслідок взаємодії сусідніх атомів, що заміщають, або груп атомів цей або сусідньої макроцепи. Такі перешкоди особливо виявляються у випадку величезних молекул, що займають у просторі різноманітне положення. При внутрішньому обертанні відбувається зміна загальної енергії молекули, тому що енергія взаємодії між атомами або групами атомів визначається відстанню між ними. Тому для високомолекулярних з'єднань ще в більшому ступені, чим для низькомолекулярних, характерно загальмоване внутрішнє обертання.
Молекулярна маса полімерів - цілком нове поняття. Якщо для звичайних
202
з'єднань молекулярна маса - розмір постійна, константа, що строго характеризує індивідуальність хімічної речовини, те для полімерних з'єднань молекулярна маса - розмір середньостатистична. Це пов'язано з палимо, що полімерні з'єднання звичайно складаються із суміші макромолекул, що мають різноманітні розміри і масу, - полімергомологів. Тому для полімерів користуються поняттям середньої молекулярної маси. Проте при однаковій середній молекулярній масі зразки полімеру можуть відрізнятися по співвідношенню наявних в них різноманітних полімер гомологів. Для кількісної оцінки такого співвідношення вводитися поняття щабель полідисперсності, або молекулярно-масового розподілу. Цей розмір визначається значеннями середніх молекулярних мас фракцій полімер гомологів.
Ступінь полідисперсності, як і молекулярна маса, є важливою характеристикою полімеру.
Високомолекулярні з'єднання відрізняються від звичайних речовин особливим характером їхніх хімічних перетворень. Найменшої «часткою» у макромолекулярної ланцюзі, що бере доля в хімічних реакціях, часто виступає не молекула в цілому, як у ряду низькомолекулярних з'єднань, а елементарна ланка, або ділянка ланцюга макромолекули. Внаслідок гнучкості макромолекули деякі її ділянки поводяться як кинетично самостійні одиниці, проявляючи скроні автономність.
Поряд із реакціями елементарних ланк відбуваються і макромолекулярні реакції полімерів, у яких макромолекула поводитися яка єдине ціле.
Властивості полімерів залежать від геометричної форми макромолекул. Так, лінійні полімери, володіючи великою тривкістю, еластичністю, можуть утворювати розчини з високою грузькістю. Це пов'язано з високим щаблем орієнтації лінійних макромолекул друг щодо друга і їх досить щільним упаковуванням. Розгалужені полімери володіють іноді навіть більшою розчинністю в порівнянні з лінійними полімерами. Ступінь розгалуженості визначає їхня тривкість і грузькість розчинів. Наприклад, полімери з високим щаблем розгалуження утворять розчини зі зниженою грузькістю, що пояснюється меншою гнучкістю цих макромолекул, а виходить, і незначною їхньою асиметрією. Розгалуженість макроцепи є ще одним видом нерегулярності макромолекул полімеру, що мішає і навіть перешкоджає кристалізації. Сітчасті полімери по властивостях дуже відрізняються від лінійних і розгалужених полімерів. Смердоти не розчиняються, не плавляться без розкладання, практично не кристалізуються. Ці особливості визначаються щаблем зв'язування макромолекулярніх ланцюгів між собою. Наприклад, із збільшенням числа хімічних зв'язків між макромолекулами збільшується твердість полімеру з одночасним зменшенням можливості його кристалізації. У даному випадку межмолекулярні зв'язки діють аналогічно розгалуженню ланцюгів: шкірний вузол фактично є множинним розгалуженням.
Фізичні стани полімерів
На відміну від низькомолекулярних речовин високомолекулярні з'єднання можуть знаходитися тільки в двох агрегатних станах: твердому і рідкому.
По характері поводження полімерних матеріалів під впливом механічних навантажень (при кімнатній температурі) усі високомолекулярні з'єднання діляться на трьох великі групи.
203
1.Текучі полімери, що мають аморфна будівля, що необратимо змінюють свою форму під дією навіть незначних механічних навантажень (наприклад, низькомолекулярній поліізобутілен, фенолоформальдегідні полімери --резоли).
2.Высокоеластичні полімери (еластомери), що мають у ненапряженому стані аморфна будівля (наприклад, каучуки і гуми) і обратимо що деформуються під впливом щодо небільших. навантажень. При нагріванні багато твердих полімерів стають высокоеластичними (полістирол, полівенилхлорід і ін.).
3.Тверді полімери, що мають аморфна або кристалічна будівля, мало змінюють свою форму навіть при великих механічних навантаженнях. Після усунення дії останніх смердоти спроможні відновлювати свою початкову форму. Тверді аморфні полімери, що не встигнули при охолодженні закрісталізуватися, але що загубили текучість, називаються стеклообразними полімерами.
Таким чином, аморфні полімери можуть перебувати в трьох фізичних станах: твердому, або стеклообразному, високоеластичному і вязкотекучему. Слід зазначити, що высокоеластичне стан характерно тільки для высокополімеров.
При нагріванні або охолодженні тієї самий полімер може переходити з одного фізичного стана в інше. Наприклад, поліізобутілен при кімнатній температурі знаходиться у високоеластичному стані, але при нагріванні може бути переведень у вязкотекуче, а при охолодженні - у стеклообразне. Всі три фізичних стани аморфних полімерів необхідно строго відрізняти від фазових состоянь— кристалічного і рідкого. У залежності від температур й розумів механічного впливу аморфний полімер спроможний переходити з одного фізичного стана в інше без стрибкоподібних змін термодинамічних властивостей. Отже, в усіх
фізичних станах аморфного полімеру його фазовий стан ті саме - рідке. Наявність великого температурного інтервалу між твердий і вязкотекучим
станами (до 150°С) - одна з відмінних рис полімерних матеріалів.
Стосовно впливу тепла високомолекулярні з'єднання поділяють на термопластичні і термореактивні. Термопластичні полімери спроможні розм'якшуватися при нагріванні і знову затвердівати при охолодженні, зберігаючи усі свої властивості: розчинність, плавкість і т.д. Термореактивні полімери при підвищенні температур спочатку стають пластичними, але потім, затвердівая (під впливом каталізаторів або отвердітелей), переходять у неплавкий і нерозчинний стан.
Методи синтезу високомолекулярних з'єднань
Нафтохімічне синтез-джерело мономерів
Мономері служать структурними одиницями, «цеглинками», із яких побудовані високомолекулярні з'єднання. Основним джерелом мономерів є нафтохімічний синтез, задача якого складається в одержанні різноманітних хімічних продуктів із нафти і газів (природних і побіжних): синтетичних миючих засобів, розчинників, присадок, палив, мастильних масел, аміаку, водню і багатьох інших. У промисловості нафтохімічного синтезу використовують у великих масштабах граничні, непредельні, ароматні і, у меншому ступені, нафтенові вуглеводні. При переробці нафтохімічної сировини застосовуються процеси дегидрировання, ізомерізації і циклізації, алкіліровання , полімеризації і
204
конденсації, а також галогенування, нитровання, сульфіровання, окислювання і т.д.
Для одержання нижчих мономерів можуть використовуватися процеси піролізу газоподібних вуглеводнів із С2—С4 (компоненти природних і побіжних газів) і нафтових фракцій - від бензинових (С5—С10) до газойлевих (С18—С25). Основним продуктом піролізу є етилен, що провадиться у величезних кількостях.
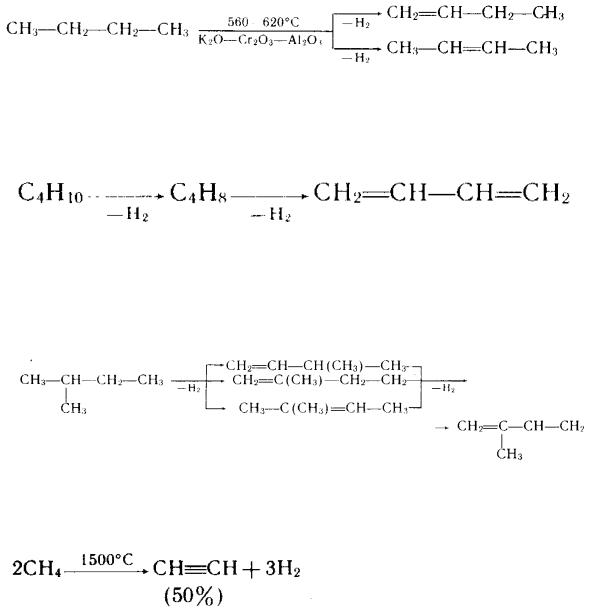
З газів, що утворяться при термічній або термокаталітичної переробці нафтопродуктів, витягають бутилені й амілени. Їх можна також одержувати каталітичним дегідруваннєм бутанів і пентанів:
З дієнових вуглеводнів найбільше значення мають бутадієн і ізопрен. Перший промисловий засіб одержання бутадієну - каталітичне перетворення етилового спирту - був розроблений С.В.Лебедєвим (1928) (див. гл. I, § 16). Зараз бутадієн одержують каталітичним дегідруваннєм н-бутану і н-бутілену, що утримуються в природних газах і газах нафтопереробних заводів:
Бутадієн утвориться також у якості побічного продукту (у невеличкій кількості) при піролізі важких бензинових, гасових і газойлевих фракцій. Високотемпературній піроліз пентано-аміленової фракції нефтепереробки може дати ізопрен.
Наявність значних кількостей пентанів у побіжних газах нафтовидобутки і низька їхня вартість роблять цей метод економічно вигідним:
ізопрен У якості мономера широко використовується ацетилен, що утворюється з
карбіду кальцію, а також электрокрекінгом, термоокислювальним крекінгом і високотемпературнім піролізом метану й інших алканів:
Для синтезу багатьох мономерів духмяного ряду служити бензол, що утвориться при ароматизації циклоалканов або виділяється з кам'яновугільної смоли.
За останні роки поряд із нафтою, газами і рогом для синтезу мономерів вусі ширше використовується рослинна сировина, якою дуже багатий Радянський Спілка. Мова йде насамперед про сировину, що пентозансодержить, і різноманітних отходах сільського господарства, що можуть бути джерелами

205
цінних хімічних продуктів, наприклад фурфурола.
Будівля мономерів і їхня спроможність до утворення полімерів
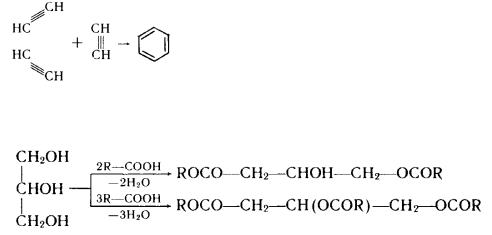
Мономери повинні відповідати декільком вимогам. Головне з них - містити не менше двох функціональних груп, спроможних взаємодіяти принаймні з двома іншими мономерами. У якості таких груп можуть виступати —ОН, —СООН, — СНО, -NH2 і ін. Число цих груп визначає функціональність мономера. Так, оцтова кислота СНзСООН і етиловий спирт С2Н5ОН - монофункціональні з'єднання. При їхній взаємодії утвориться, як відомо, складаний ефір - з'єднання низкомолекулярне , що не має реакційноспособних груп, а отже, не спроможне до подальшої конденсації:
При реакції дікарбонових кислот із двохатомними спиртами (гликолями) - з'єднаннями біфункціональними, утворяться ефіри, що містять у молекулі як і раніше дві функціональні групи, що можуть знову вступати в реакцію конденсації з мономерами:
макромолекули, отримані з біфункціональних мономерів, мають лінійну будівлю. Якщо ж функціональність вихідних мономерів більше двох, то утворяться розгалужені або просторові полімери:
Таким чином, геометрична форма макромолекул полімеру залежить від функціональності вихідних мономерів.
Подвійний або потрійний зв'язок, що утримується в молекулі мономера, також може визначати його функціональність. Молекула етілену, приєднуючи по подвійному зв'язку двох атоми водню або галогену, біфункціональна. Ацетилен приєднує чотири таких атоми, тому він тетрафункціонален. Проте функціональність для багатьох мономерів - розмір непостійна. Наприклад, тієї ж
206
ацетилен при утворенні бензолу має функціональність, рівну не чотирьом, як у випадку реакції приєднання, а двом:
Перемінною функціональністю володіє також і гліцерин. У залежності від розумів реакції і кількості кислоти, що реагує з ним, гліцерин може бути бі- і трифункціональним з'єднанням:
Іноді для синтезу високомолекулярних з'єднань використовують і олігомери. На їхній основі можна одержувати блок-сополімери, що сполучать у собі властивості багатьох полімерів.
Наявність двох або більш функціональних груп у молекулі мономера, використовуваного для синтезу полімеру, - умова необхідне, але недостатнє. Необхідним є також відсутність об'ємних заступників поруч із подвійним зв'язком. У противному випадку при синтезі високомолекулярних з'єднань методом полімеризації виникають просторові (стеричні) утруднення, що перешкоджають утворенню полімеру. Наприклад, 1,1 -діфенил-етілен СН2=С(С6Н5)2 на відміну від стіролу С6Н5—СН=СН2 не спроможний полімерізоватися через вплив великих по обсязі фенільних груп-заступників. По цей же причині не вступають у реакції полімеризації багато хТО 1,2-пронзводні етилену, у молекулах котрих хоча б один із двох заступників має великі розміри. Проте деякі навіть тризаміщєні етилену спроможні вступати в реакцію полімеризації, наприклад трифторетілен. Це пов'язано з палимо, що обсяг атома фтору близький до обсягу атома водню.
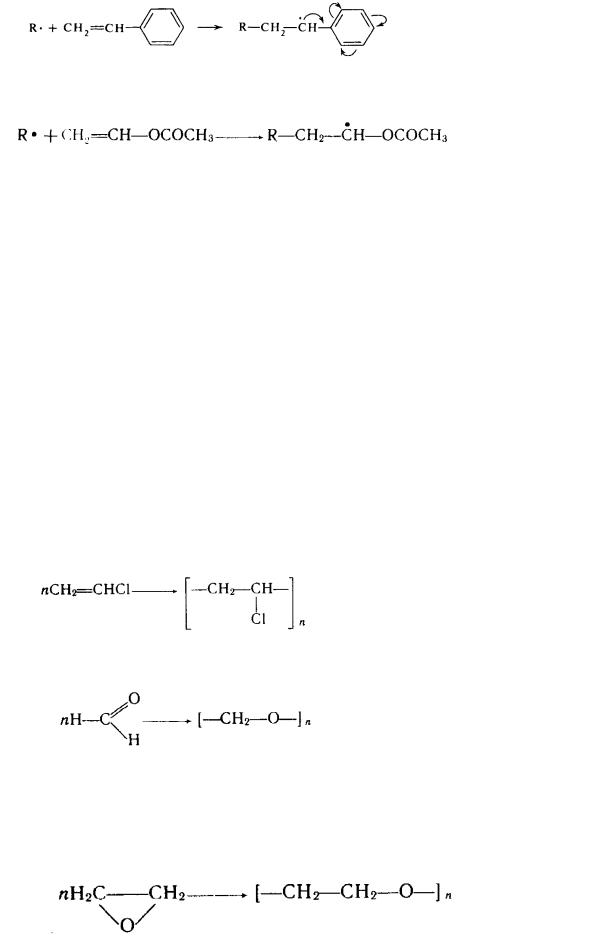
На реакційну спроможність мономера впливають індуктивний ефект і ефект сполучення, що вишиваються дією заступників. Дійсно, спроможність непредельних мономерів до полімеризації залежить також і від природи заступників, їхній числа, розташування в молекулі мономера подвійних зв'язків. Введення в молекулу етилену різноманітних по своїй електронній природі груп, що заміщають, викликає поляризацію подвійного зв'язку, що веде до збільшення реакційної спроможності мономера. Як буде показано, процес полімеризації часто пов'язаний із виникненням вільних радикалів, що реагують із мономерами (радикальна полімеризація). При цьому з вільним радикалом, що володіє электрофільними властивостями, легше буде реагувати саме поляризована, а виходить, реакціонноспособна молекула мономера. Приєднання радикала відбувається в першу чергу по місцю підвищеної електронної щільності. Але швидкість реакції полімеризації залежить також і від активності самого радикала. Проте вільні радикали, що утворилися з активних мономерів, завжди малоактивні. Це пов'язано з палимо, що ефект сполучення дозволяє неспареному електрону в радикалі розподілитися по всій молекулі:
207
активний мономер (стирол) |
неактивний радикал |
Мономері, не активовані сполученням, утворять найбільше активні вільні радикали:
малоактивний мономер активний радикал (вінілацетат)
Таким чином, чим менше ефект сполучення в мономері, тобто чим менше його молекула поляризована, палимо більше активність радикала, що утвориться з нього. Оскільки ефект сполучення більше позначається на активності радикала, чим на реакційній спроможності мономера, швидкість радикальної полімеризації залежить головною уявою від активності радикала.
Деякі фізичні властивості найбільше мономерів , що часто зустрічаються , приведені в табл. 17.
ЛАНЦЮГОВА ПОЛІМЕРИЗАЦІЯ
Існують два основних засоби одержання високомолекулярних з'єднань: полімеризація і поліконденсація.
Реакція з'єднання молекул мономера, що протікає за рахунок розірвання кратних зв'язків і сопроводжующа не виділення побічних низькомолекулярних продуктів, тобто приводяща елементного складу мономера , що не до зміни,
У ланцюгову полімеризацію вступають в основному ненасычені мономери, у яких подвійний зв'язок знаходиться між вуглецевими атомами:
вінілхлорид полівенилхлорід
або між вуглецем і будь-яким іншим атомом:
формальдегід поліметиленоксид
У першому випадку утворяться карбоцепні полімери, у другому - гетероцепні.
Можлива полімеризація і насичені з'єднання циклічної будівлі з гетероатомому циклі. Циклізація цих з'єднань відбувається з розмиканням циклу, у результаті чого утвориться гетероцепної лінійний полімер:
оксид етілену поліетіленоксид

208
Як і будь-яка хімічна реакція, полімеризація починається з розірвання одних хімічних зв'язків і виникнення інших. Таке розірвання, як відомо, може відбуватися або по гетеролітичному, або по гомолітичному механізмі. У першому випадку утворяться іони, а в другі-вільні радикали. Полімеризація, що протікає через утворення іонів, називається іонною полімеризацією, а йде з участю вільних радикалів - радикальної. Таким чином, радикальна й іонна полімеризація різняться природою активного центру, що починає і веде макромолекулярний ланцюг.
Радикальна полімеризація
Радикальна полімеризація - один із поширених засобів синтезу полімерів. Активним центром такої полімеризації є вільний радикал. Як і всякий ланцюговий процес, радикальна полімеризація протікає через трьох основні стадії.
1 ініциювання (утворення активного центру). На цій стадії відбувається ініциюваннє молекули мономера з утворенням первинного вільного радикала (ДО^), що легко взаємодіє з різноманітними ненасыченими з'єднаннями (мономерами) :
У залежності від засобу утворення вільних радикалів, що починають реакційний ланцюг, розрізняють декілька видів полімеризації: термічну, фотохімічну, радіаційну й ініційовану.
При термічній полімеризації вільні радикали утворяться з мономерів під дією високих температур (700—1000°С). що відбувається при цьому розірвання подвійного зв'язку в молекулі призводить до появи бірадикалу:
котрий, взаімодействуя з молекулою мономера
утворить більш складаний бірадикал. Він, у свою чергу, перетворюється потім у мономакрорадикал. Випливає, проте, відзначити, що термічна полімеризація не має поки широкого практичного значення, тому що її швидкість порівняно невелика.
Фотохімічна полімеризація ініціюється при освітленні молекул мономера. Збуджена в такий спосіб молекула мономера взаємодіє в результаті співудари з другою молекулою з утворенням бірадикалу, що потім діспропорціонірує в два монорадікали:
Радіаційна полімеризація протікає при дії на мономери ? -, β -, γ -та R- випромінювання. Вільні радикали , що утворяться , ініціюють потім реакцію
209
полімеризації.
Проте найбільше поширеним і часто застосовуваним на практику методів полімеризації є ініційована полімеризація. Смердота активується з'єднаннями, що легко розпадаються на вільні радикали в умовах полімеризації. Такі
з'єднання називаються ініціаторами полімеризації. Смердоти містять у своїх молекулах хитливі хімічні зв'язки (О-О, N-N. §-8, О-N і ін.), що розриваються при набагато меншій енергії, чим це потрібно для утворення вільного радикала
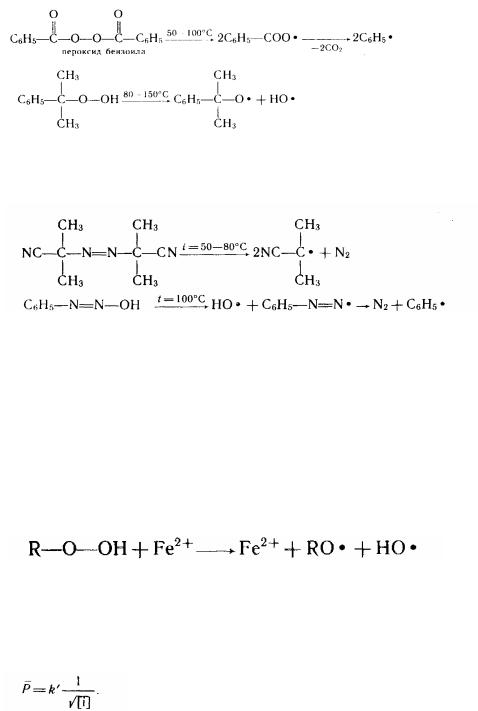
змолекули мономера (при її активації). Ініціаторами можуть бути органічні пероксіди і гідропероксиди, деякі азо- і діазосполучення й інші речовини:
гідропероксид ізопропіл бензолу (гіпериз)
діазогідрат Швидкість розпаду ініціатора на вільні радикали можна збільшити не тільки
підвищенням температур, але і добавкою в реакційне середовище спеціальних восстановлювачей - промоторів і активаторів. Промоторі збуджують хімічну реакцію, діючи тільки на початку процесу, а активаторі підтримують активність каталізатора (ініціатора) протягом усього процесу. Ці речовини сприяють утворенню вільних радикалів з ініціаторів при більш низьких температурах (окисно-відбудовне ініциюваннє). Роль таких добавок можуть виконувати солі Fe2+ і інших металів, а також пірогаллол, третинні амини , аскорбінова кислота й ін. :
Кількість вводимого ініціатора звичайно невелике (0,1-1%). Загальна швидкість радикальної полімеризації зростає пропорційно кореню квадратному з концентрації ініціатора: v=kv[i], де [i]-концентрація ініціатора. У тієї ж час середній ступінь полімеризації (Р) обернено пропорційна кореню квадратному з цього розміру:
Таким чином, при збільшенні концентрації ініціатора пришвидшується процес радикальної (ініційованої) полімеризації з одночасним зниженням середнього

210
щабель полімеризації.
2.Ріст ланцюга. Реакція росту ланцюга полягає в багатократному приєднанні молекул мономера до усложніння щораз радикалу зі зберіганням вільного електрона в кінцевої ланкі макромолекулы , що рості. Іншими словами, що рості макромолекулярний ланцюг винний залишатися в період її росту вільним макрорадикалом:
Урезультаті таких послідовних реакцій приєднання подвійний зв'язок мономера перетворюється в просту, що супроводжується виділенням енергії за рахунок різниці енергій σ - і π -зв'язків.
3.Обрив ланцюга. Кінець росту ланцюга пов'язаний із зникненням вільного електрона в останньої ланки макромолекули. Частіше усього це відбувається в результаті з'єднання між собою двох радикалів (реакція рекомбінації), що призводить до виникнення ланцюга, що не спроможна до подальшого росту:
Проте вільні радикали (макрорадикали), приходячи винятково реакційноспособними частками, взаємодіють не тільки з мономерами, але і з розчинником, різноманітними домішками і з макромолекулами , що образовалися. При цьому неподілений електрон (активний центр) може перейти на будь-яку іншу молекулу, наприклад молекулу розчинника, що, перетворюючись у радикал, дає початок новій макромолекули:
Такі реакції називаються реакціями передачі ланцюга. У даному випадку передача ланцюга відбувається через розчинник - чотирьоххлористий вуглець. Можливість такої передачі збільшується з підвищенням температур полімеризації. При цьому швидкість реакції полімеризації не зменшується, але, оскільки реакційний ланцюг розпадається отут на декілька молекулярних ланцюгів, ступінь полімеризації полімеру , що утвориться , помітно знижується. Змінюючи в такий спосіб співвідношення кількості мономера і розчинника, можна одержувати полімери з різноманітною молекулярною масою. Речовини, через які здійснюється передача ланцюга і регулюється середня молекулярна маса полімеру, називаються регуляторами. У якості регуляторів застосовують чотирьоххлористий вуглець, тіоли , тіогліколеву кислоту й ін.
Реакції обриву і передача ланцюга часто використовуються в практичних цілях для стабілізації мономерів при їхньому збереженні. Це необхідно для запобігання передчасної полімеризації мономерів і для керування процесом полімеризації в цілому. Для цього часто використовують інгібітори (стабілізатори), що при взаємодії з вільними радикалами утворять малоактивні частки, не спроможні надалі ініціювати процес полімеризації.
