
- •Міністерство освіти і науки україни
- •Скопійовано з оригіналу-макета, наданого автором
- •1. Математичне моделювання хіміко-технологічних процесiв
- •1.1. Загальні поняття
- •1.2. Класифікація моделей.
- •1.3. Фізичне моделювання
- •1. 4. Математичне моделювання
- •Знак ( –) при коефіцієнтах порівнянь означає, що потік спрямований з
- •1. 5. Засоби складання математичних моделей.
- •1. 5. 1. Емпiричний засіб
- •Загальна оцінка експериментальних засобів.
- •Приклад
- •1.5.2. Експериментально - аналітичний засіб
- •1. 5. 3. Теоретичний засіб
- •1. 5. 4. Зіставлення засобів побудови математичних моделей
- •5. 5. Вірогідність та простота моделі
- •5. 6. Рішення порівнянь математичного опису
- •5. 7. Перевірка адекватності та iдентифікація моделі
- •5. 8. Вибір математичної моделі
- •2.Моделювання Хімічних Реакторів
- •2. 1. Модель реактора ідеального змішування
- •2. 1. 1 Модель різ для опису стаціонарного режиму
- •2. 1. 2. Модель різ при протечі деяких реакцій
- •2. 1. 3. Дослідження моделі різ
- •2. 1. 4. Побудова q - t -діаграми і дослідження стійкості стаціонарних режимів різ
- •2. 1. 5 Умова стійкостi
- •2. 1. 6. Вплив вхідних параметрів на стаціонарні режими. Побудова статичних характеристик різ
- •2. 2. Реактор ідеального витиснення (рів)
- •2. 2. 1. Математична модель рів
- •2. 2. 2. Дослідження рів.
- •1.Зміна ступені перетворення при iзотермічному режимі
- •2.Зміна ступеня перетворення при адiабатичному режимі
- •2. 2. 3. Зіставлення різ та рів
- •2. 3. 5. Ячеєчна модель
- •2. 4. Дифузійна модель зподовжнім переносом речовини та тепла
- •2.5. Двохпараметрична дифузійна модель
- •3. Побудова математичнОї моделі каталітичного реактора
- •3. 1. Етапи побудови математичної моделі
- •3. 2. Структурний аналіз
- •3. 3. Моделювання процесу на одному зерні каталiзатора
- •3.4 Теоретична оптимiзація.
- •3. 5. Попередній вибір типу реактора .
- •3. 6. Моделювання процесу в шару каталiзатора.
- •4. Усталеність реакторних схем
- •4.1 Методи дослідження усталеності
- •4.2 Усталеність простих схем
- •4.3 Усталеність промислових реакторів.
- •5. Методи оптимізації технологічних процесів
- •5.1. Постановказадачіоптимізації
- •5.2. Цільова функція і її властивості
- •5.2.1. Нормалізація незалежних перемінних
- •5.2.2. Геометрична інтерпретація цільової функції
- •5.2.3. Особливі крапки і лінії цільової функції
- •5.2.4. Глобальний і локальний оптимуми
- •5.3. Методи рішення задач оптимізації
- •5.4.Аналітичні засоби
- •5.5. Загальна характеристика засобів рішення задач нелiнійного програмування
- •5.6. Градiєнтні методи рішення задач оптимiзації
- •5.6.1. Градієнт цільової функції
- •5.6.2. Обчислення похідних цільової функції
- •5.6.3. Засіб релаксації.
- •5.6.4. Метод градієнту
- •5. 6. 5. Засіб найскорішого спуска
- •5.7. Безградiєнтні методи рішення задач оптимiзації
- •5. 7. 1. Метод сканiрованiя
- •5. 7. 2. Метод локалiзації екстремума
- •5. 7. 3. Метод "золотого перетину"
- •5. 7. 4. Метод покоординатного спуска Гаусса - Зейделя
- •5. 7. 5. Метод Хука - Джiвса
- •5. 7. 6. Метод сканiрованiя
- •5. 7. 7. Симплексний метод
- •5.7.8. Метод Нелдера-Мида
- •5.8. Методи випадкового пошуку
- •5.8.1. Метод сліпого пошуку
- •5.8.2. Метод випадкових напрямків
- •5.8.3. Метод випадкових напрямків зі зворотним кроком
- •5.8.4. Одержання випадкових чисел
- •5.8.4.1. Метод добутків
- •5.8.4.2. Метод відрахувань
- •5.8.4.3. Одержання псевдовипадкових послідовностей з ірраціональних чисел
- •5.9. Порівняння різних методів рішення задач оптимізації методами нелінійного програмування
- •Література
2. 1. 4. Побудова q - t -діаграми і дослідження стійкості стаціонарних режимів різ
Однією із основних характеристик хімічного реактора є його стійкість,тобто спроможність вертатися до вихідного стаціонарного стану після усунення зовнішніх збуреннь. Для дослідження стійкості РІЗ широко використовують діаграму залежності тепловиделення і тепловідводу від температури (Q-T діаграму).
Спершу розглянемо залежність швидкості реакції, яка протікає в РІЗ, на прикладі єдиної необоротної реакції 1-го порядку. Швидкість реакції в розмірному виді виражається наступною залежністю:
W=K C = K0e–E/RT C (2.12)
Значення концентрації C в реакторі залежить від величини концентрації на вході C0і температури в реакторі T. Із рівнення матеріального балансу для стаціонарного режиму (2.7) слідує, що C = C0/(1+K) = C0/(1+K0 e–E/RT ) (2.13)
 де t =
V/Q - час контакту,c.
де t =
V/Q - час контакту,c.
Підставляя (2.13) в (2.12),остаточно одержимо :
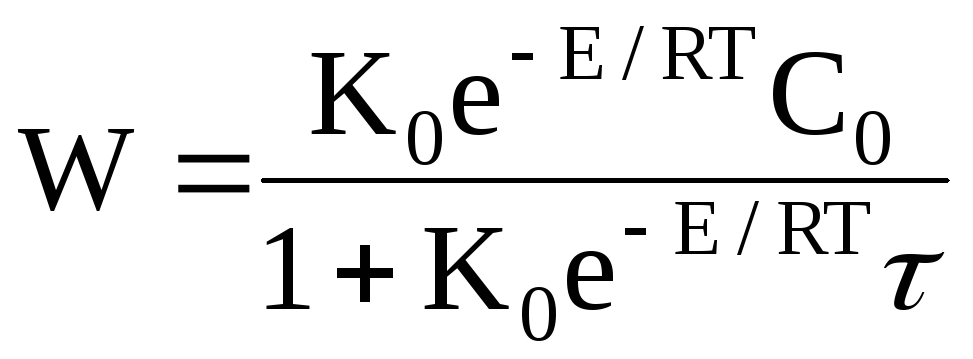 (2.14)
(2.14)
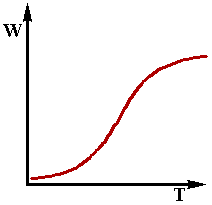
Графік залежності (2.14) має наступний вид (див. рис.2.2):
Рис 2.2
При малих значеннях температури T другий доданок в знаменнику
зневажливо малий по зрівнянню з одиницею.Тоді :
![]() (2.15)
(2.15)
В цій області з підвищенням температури швидкість реакції зростає по закону Аррейнiуса(нижня вітка графіка).
При великих температурах,навпаки, другий доданок в знаменнику формули (2.14) стає набагато більше одиниці.Тоді :
W0=C0 (2.16)
де = V/Q - час контакту.
Фізичний зміст залежності (2.16) достатньо зрозуміло. При високих температурах реакція протікає настільки хутко, що реагує практично вся речовина,що надходить в апарат.В цьому режимі швидкість реакції W практично не залежить від температури (верхня вітка графіку).
Аналогічний вид мають ці залежності і в безрозмірної формі. Для побудови Q-T-діаграми розглянемо рівнення енергетичного балансу в безрозмірної формі (2.10). В стаціонарному режимі накопичування тепла дорівнює нулю. Запишемо рівнення енергетичного балансу у наступному виді:
![]() (2.17)
(2.17)
Позначимо ліву частину порівняння qR-виділення тепла,тобто кількість тепла,що виділяється при протечі хімічної реакції в одиницю часу, а праву – qT-отвод тепла,тобто кількість тепла, що отводиться через стінку холодильника із струмом. В стаціонарному режимі виділення і отвод тепла дорівнюються між собю qR= qT.
Перетворюємо вираз для розрахунку величини теплоотводу q :
![]()
Остаточно :
![]() (2.18)
(2.18)
де a = BX+X.
Вираз для розрахунку величини тепловиділення qR:
![]()
 Характер залежностей (2.18) і (2.19) від
температури наступнийвираз
(2.18) становить порівняння прямої
лінії, причому q зростає, коли збільшується.У виразі (2.19)АД- коеффiциєнт,який не залежить від
температури, так що залежність qRвідмає такий вид,
як функція W = f (T) (рівняння
2.14), відрізняясь лише
масштабом (рис. 2.3).
Характер залежностей (2.18) і (2.19) від
температури наступнийвираз
(2.18) становить порівняння прямої
лінії, причому q зростає, коли збільшується.У виразі (2.19)АД- коеффiциєнт,який не залежить від
температури, так що залежність qRвідмає такий вид,
як функція W = f (T) (рівняння
2.14), відрізняясь лише
масштабом (рис. 2.3).
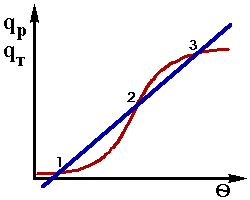
Лінії залежностей qRіqTвід температури пересікаються в трьох крапках - 1, 2 і 3. В цих крапках при температурах q1, q2, q3 процес стаціонарен, тому що дотримується умова стаціонарностi qR=qTабо d/dt' = 0.
Як видно із графіку (рис.2.3) в наданій сітуаці
при одніх і отих же значеннях вхідних параметрів
Рис.2.3. можливі три різноманітних стаціонарних
режима, що забезпечують не тільки значення різноманітних вихідних параметрів, але і відрізняються по стійкостi.
Розглянемо спершу стаціонарний режим 3, що відповідає режиму роботи при температурі 3. Так як швидкості виділення і отвода тепла однакові, оте поки температуране зміниться, режим залишається стаціонарним. Припустимо, що внаслідок випадкового обурення змінюється значення x і відбувається зміщення на величину. При цьому за рахунок прискорення швидкості реакції зростає швидкість виділення тепла; це зростання діється по лінії, яка відповідає кривої тепловиділення. Одночасно, за рахунок збільшеннярізницітемператур між температурами в реакторі і теплоносія зростає швидкість відведення тепла, це зростання діється по лінії тепловідводу.
В крапці 3 лінія тепловідвода минає з більш великим кутом наклона,чим лінія тепловиділення. Тому при температурі3+ швидкість відвода виявляється вищою,ніж швидкість його виділення. В цих умовах, після зняття обуренняреактор почне охолоджуватися. Охолодження буде тривати до отих пор, поки температура в реакторі не стане дорівняної3. При цій температурі швидкості від вода і виділення тепла знову зрівняються і режим знов стане стаціонарним.
Навпаки, якщо внаслідок обурення (=–) реактор почне охолоджуватися, оте після зняття обурення (тому що швидкість виділення тепла при цих умовах перевищує швидкість тепловідводу) реактор знову почне нагріватися до досягнення в ньому температури, яка дорівнює3.
Таким чином, стаціонарний режим в крапці 3 вертається до вихідного стану після зняття зовнішніх обурень, можна сказати що режим стійкий.
Спроможність системи (реактора) вертатися до вихідного стаціонарного стану після зняття обурень називається стійкiстью.
Інакше кажучи, вихідний стаціонарний режим є стійким, якщо після усунення джерел порушення режиму будь-які малі відхилення з течією часу прагнуть до нуля. Якщо ж значення відхилень наростають в часу, оте вихідний стаціонарний режим нестійкій.
При температурі 1, відповідній стаціонарному режиму 1, з погляду стійкiстi картина повністю аналогична розглянутому вище режиму в крапці 3, тому що і в цьому випадку лінія тепловідвода іде круче, чим лінія тепловиділення і вихідний стаціонарний режим стійкий.
Тепер розглянемо режим в крапці 2. Тут наклон лінії тепловідвода менш, чим лінії тепловиділення. Але також, як і в крапках 1 і 3, qR= qTі якщо немає обурень, режим буде стаціонарним. Хай сталося випадкове обурення і температура1підвищілася на величину. При температурі=+швидкість виділення тепла стає більше, ніж швидкість тепловідвода. І тому після зняття обурення реактор буде не охолоджуватися,а нагріватися, віддаляясь від вихідного стану. Нагрів буде тривати до отих пор, поки знов швидкість тепловиділення не буде дорівняної швидкості тепловідвода, т. є. реактор досягне нового стаціонарного стану - при температурі3. Аналогічно, при заперечливих обуреннях реактор буде самопроiзвольно охолоджуватися до отих пор,поки не досягне стійкого стаціонарного стану при температурі.
Проведений аналіз показав, що із трьох можливих в наданих умовах стаціонарних режимів тільки два :1- при низькій температурі і, відповідно, малої швидкості реакції) і 3-при високій температурі і великої швидкості реакції є стійкимi, а третій - при проміжних значеннях температури і швидкості реакції (крапка 2) - нестійкий.
