
- •Міністерство освіти і науки україни
- •Скопійовано з оригіналу-макета, наданого автором
- •1. Математичне моделювання хіміко-технологічних процесiв
- •1.1. Загальні поняття
- •1.2. Класифікація моделей.
- •1.3. Фізичне моделювання
- •1. 4. Математичне моделювання
- •Знак ( –) при коефіцієнтах порівнянь означає, що потік спрямований з
- •1. 5. Засоби складання математичних моделей.
- •1. 5. 1. Емпiричний засіб
- •Загальна оцінка експериментальних засобів.
- •Приклад
- •1.5.2. Експериментально - аналітичний засіб
- •1. 5. 3. Теоретичний засіб
- •1. 5. 4. Зіставлення засобів побудови математичних моделей
- •5. 5. Вірогідність та простота моделі
- •5. 6. Рішення порівнянь математичного опису
- •5. 7. Перевірка адекватності та iдентифікація моделі
- •5. 8. Вибір математичної моделі
- •2.Моделювання Хімічних Реакторів
- •2. 1. Модель реактора ідеального змішування
- •2. 1. 1 Модель різ для опису стаціонарного режиму
- •2. 1. 2. Модель різ при протечі деяких реакцій
- •2. 1. 3. Дослідження моделі різ
- •2. 1. 4. Побудова q - t -діаграми і дослідження стійкості стаціонарних режимів різ
- •2. 1. 5 Умова стійкостi
- •2. 1. 6. Вплив вхідних параметрів на стаціонарні режими. Побудова статичних характеристик різ
- •2. 2. Реактор ідеального витиснення (рів)
- •2. 2. 1. Математична модель рів
- •2. 2. 2. Дослідження рів.
- •1.Зміна ступені перетворення при iзотермічному режимі
- •2.Зміна ступеня перетворення при адiабатичному режимі
- •2. 2. 3. Зіставлення різ та рів
- •2. 3. 5. Ячеєчна модель
- •2. 4. Дифузійна модель зподовжнім переносом речовини та тепла
- •2.5. Двохпараметрична дифузійна модель
- •3. Побудова математичнОї моделі каталітичного реактора
- •3. 1. Етапи побудови математичної моделі
- •3. 2. Структурний аналіз
- •3. 3. Моделювання процесу на одному зерні каталiзатора
- •3.4 Теоретична оптимiзація.
- •3. 5. Попередній вибір типу реактора .
- •3. 6. Моделювання процесу в шару каталiзатора.
- •4. Усталеність реакторних схем
- •4.1 Методи дослідження усталеності
- •4.2 Усталеність простих схем
- •4.3 Усталеність промислових реакторів.
- •5. Методи оптимізації технологічних процесів
- •5.1. Постановказадачіоптимізації
- •5.2. Цільова функція і її властивості
- •5.2.1. Нормалізація незалежних перемінних
- •5.2.2. Геометрична інтерпретація цільової функції
- •5.2.3. Особливі крапки і лінії цільової функції
- •5.2.4. Глобальний і локальний оптимуми
- •5.3. Методи рішення задач оптимізації
- •5.4.Аналітичні засоби
- •5.5. Загальна характеристика засобів рішення задач нелiнійного програмування
- •5.6. Градiєнтні методи рішення задач оптимiзації
- •5.6.1. Градієнт цільової функції
- •5.6.2. Обчислення похідних цільової функції
- •5.6.3. Засіб релаксації.
- •5.6.4. Метод градієнту
- •5. 6. 5. Засіб найскорішого спуска
- •5.7. Безградiєнтні методи рішення задач оптимiзації
- •5. 7. 1. Метод сканiрованiя
- •5. 7. 2. Метод локалiзації екстремума
- •5. 7. 3. Метод "золотого перетину"
- •5. 7. 4. Метод покоординатного спуска Гаусса - Зейделя
- •5. 7. 5. Метод Хука - Джiвса
- •5. 7. 6. Метод сканiрованiя
- •5. 7. 7. Симплексний метод
- •5.7.8. Метод Нелдера-Мида
- •5.8. Методи випадкового пошуку
- •5.8.1. Метод сліпого пошуку
- •5.8.2. Метод випадкових напрямків
- •5.8.3. Метод випадкових напрямків зі зворотним кроком
- •5.8.4. Одержання випадкових чисел
- •5.8.4.1. Метод добутків
- •5.8.4.2. Метод відрахувань
- •5.8.4.3. Одержання псевдовипадкових послідовностей з ірраціональних чисел
- •5.9. Порівняння різних методів рішення задач оптимізації методами нелінійного програмування
- •Література
2. 4. Дифузійна модель зподовжнім переносом речовини та тепла
Далеко не завжди вдається описати процес,який протікає у промисловому реакторі, ідеальними моделями.Так,наприклад, для порівняно невеликих по довжині реакторів при малих лiнейних швидкістях потоку реакційної суміші для опису адiабатичного режиму протікання процесу не підходить ані РІЗ, ані РІВ. Очевидно, що ми маємо справу з деякою проміжною нагодою, де має місце неповне змішення по потоку, т.є. на режим ідеального витиснення накладається часткове перемішення. Це підтверджується iмпульснимi та разгонними характеристика ми дифузійної моделі,що показують реакцію об'єкту при нанесенні на вході iмпульсного або стрибкообразного обурення (рiс.2.19, 2.20)
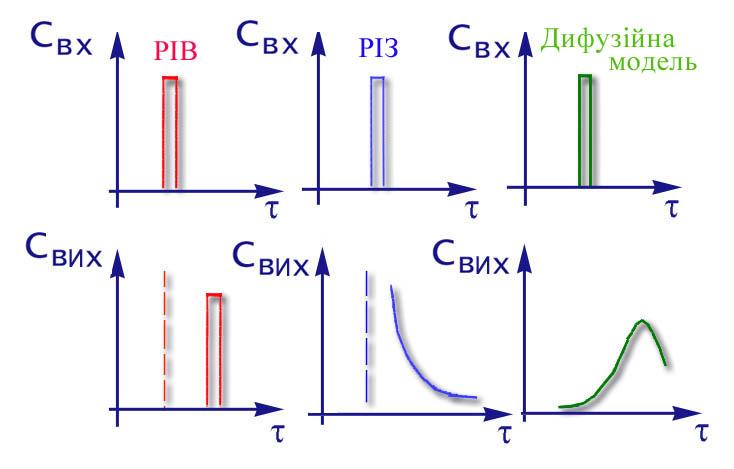 Рис
2.19. Iмпульсні характеристики
Рис
2.19. Iмпульсні характеристики
(τ- час перебування суміші у реакторі).
Спершу розглянемо одномірний випадок – перенос речовини здійснюється тільки у продольному напрямку. Така модель отримала назву однопараметрична дифузійна модель (рiс.2.21). Висновок рівнянь балансів здійснюється аналогічно РІВ.

Рис 2.20. Разгонні характеристики
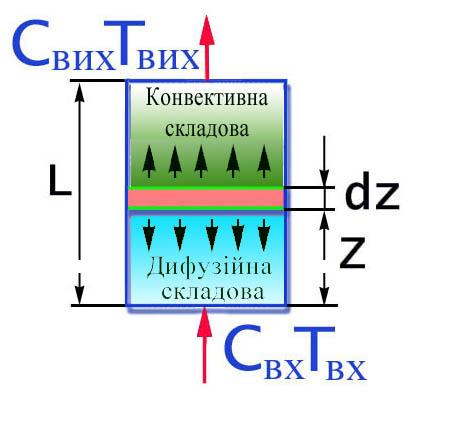
Характер процесів переносу визначається двома складовими:
1.конвективной – яка відповідна режиму ідеального витиснення;
2.дифузійної – яка описує гуртовий вплив різноманітних факторів,що виражаються у відході одніх часток потоку вперед і відставанні інших
Для опису другої складової використовуємо закон Фіка :
![]() (2.48) Рис.2.21
(2.48) Рис.2.21
де qм- кількість речовини, що дифундує у прямому та зворотному напрямку;
DL- ефективний коефіціент продольной дiффузii;
dc/dz- градієнт концентрації;
S - площа поперечного перетину.
Знак " - " у порівнянні (2.48) показує,що дифузійний потік завжди скерований вбік зменшення концентрації.
Складемо математичну модель дифузійної моделі.
Матеріальний баланс :
![]() (2.49)
(2.49)
У порівняннi (2.49) перші два доданка враховують перенос речовини через нижній кордон виділеного елементарного обсягу: перше - прихід за рахунок конвективного потоку, друге - унос за рахунок дифузійного потоку.Третій та четвертий доданок - перенос речовини через верхній кордон :третє - унос з конвективним потоком, четверте - прихід за рахунок дифузійного потоку. П'ятий доданок враховує зміну кількості речовини за рахунок хімічної реакції.
В правої частині - зміна кількості речовини у виділеному елементарному обсязі в часу. Після скорочення і ділення на SdZ одержимо :
![]() (2.50)
(2.50)
Порівняння (2.50) становить матеріальний баланс однопараметричної дифузійної моделі.Перший доданок враховує перенос речовини за рахунок конвективного потоку,другий - за рахунок дифузійного потоку, третій-за рахунок хімічної реакції.
Pівняння енергогетичного балансу складається аналогічно, а замість закона Фіка використовується закон Фур'є:
![]() (2.51)
(2.51)
де qТ- кількість теплоти,яка переноситься за рахунок теплопроводтностi;
L- ефективний коефіціент продольної теплопроводностi;
dT/dz- градієнт температур.
Знак " - " у (2.51) означає,що передача тепла здійснюється у сторону зменшення температури.
![]()
![]() (2.52)
(2.52)
Перетворив (2.52),одержимо порівняння енергетичного балансу :
![]() (2.53)
(2.53)
Порівняння кiнетики й початкові умови аналогічні моделі РIВ :
W = f(Т,С) (2.54)
Т = ТПОЧ(Z) С = CПОЧ(Z) (2.55)
Краєві (кордонні) умови необхідно задавати як на вході, так і на виході із реактора. Для висновку цих умов у загальному віпадку необхідно скласти матеріальний та тепловий баланси для вхідного та вихідного перетина реактора. На відміну від балансів, які виводяться для елементарного обсягу, в даному випадку не враховуються зміни за рахунок хімічної реакції та накопичування, тому що товщина шару dZ=0 та отже, доданкі, що містять dZ, також дорівнюють 0.
Спочатку розглянемо перетин Z=0 :
![]() (2.56)
(2.56)
![]() (2.57)
(2.57)
Після перетворень одержимо кордонні умови у наступному виді :
Z
= 0: ![]()
![]() (2.58)
(2.58)
При Z=L, т.є. на виході з реактора, як правило,швидкість хімічного перетворення вкрай мала,оскільки процес виходить або на повну, або на рівноважну міру перетворення.Отже, градієнти температур та концентрацій відсутні. Тому можна записати :
Z = L : dС/dZ=0; dТ/dZ=0; (2.59 )
