
- •Кожина Ольга Владимировна
- •Раздел 1. Белки
- •Тема 1 аминокислотный состав белка. Классификация и свойства аминокислот. Качественные реакции на белки и аминокислоты
- •Лабораторная работа №1 цветные реакции на белки и аминокислоты
- •1.4 Реакция на серусодержащие аминокислоты (реакция Фоля).
- •Контрольные вопросы:
- •Тема 2 физико-химические свойства белков. Методы осаждения белков. Высаливание и денатурация
- •Лабораторная работа №2 диализ растворов белков
- •Лабораторная работа №3 осаждение белков высаливанием
- •Лабораторная работа №4 осаждение белков при кипячении
- •Лабораторная работа №5 осаждение белков солями тяжелых металлов
- •Лабораторная работа №6 осаждение белков концентрированными минеральными кислотами
- •Лабораторная работа №7 осаждение белков органическими веществами
- •Контрольные вопросы:
- •Тема 3 количественное определение белка. Оценка на основании фотометрии продуктов цветной реакции. Построение калибровочных графиков
- •Лабораторная работа №8 количественное определение белка
- •Контрольные вопросы:
- •Тема 4 гидролиз белка. Характеристика пептидной связи
- •Лабораторная работа №9 кислотный гидролиз простого белка
- •Лабораторная работа №10 формоловое титрование (по Серенсену)
- •Контрольные вопросы:
- •Тема 5 хроматографическое разделение аминокислот
- •Лабораторная работа №11 хроматографическое разделение аминокислот на бумаге
- •Контрольные вопросы:
- •Раздел 2. Ферменты
- •Тема 6 ферменты как биологические катализаторы. Свойства ферментов
- •Лабораторная работа №12 специфичность действия ферментов
- •Лабораторная работа №13 термолабильность ферментов
- •Лабораторная работа №14 влияние реакции среды на действие ферментов слюны
- •Определение оптимума рН действия амилазы слюны
- •Лабораторная работа №15 влияние активаторов и ингибиторов на действие ферментов
- •Контрольные вопросы:
- •Тема 7 действие ферментов отдельных классов
- •Лабораторная работа №16 определение активности пепсина
- •Лабораторная работа №17 действие пепсина на белок фибрин
- •Лабораторная работа №18 обнаружение каталазы в крови
- •Лабораторная работа №19 действие липазы на жиры
- •Лабораторная работа №20 действие пероксидазы крови
- •Контрольные вопросы:
- •Тема 8 витамины, как структурные компоненты ферментов
- •Лабораторная работа №21 качественные реакции на жирорастворимые витамины
- •Лабораторная работа №22 качественные реакции на витамины группы в
- •Лабораторная работа №23 качественные реакции на витамин с
- •Лабораторная работа №24 количественное определение витамина с
- •Контрольные вопросы:
- •Раздел 3. Нуклеиновые кислоты и их обмен
- •Тема 9 структура и функции нуклеиновых кислот. Нуклеопротеиды
- •Лабораторная работа №25 выделение дезоксирибонуклеопротеидов (днп) из тканей
- •1. Экстракция и выделение днп из тканей.
- •Лабораторная работа №26 гидролиз нуклеопротеидов
- •2. Качественные реакции на составные части нуклеопротеидов.
- •Контрольные вопросы:
- •Раздел 4. Углеводы и их обмен
- •Тема 10 углеводы. Восстанавливающая способность углеводов
- •Лабораторная работа №27 качественное определение глюкозы
- •Лабораторная работа №28 качественное определение фруктозы
- •Лабораторная работа №29 обнаружение восстанавливающей способности углеводов
- •Контрольные вопросы:
- •Лабораторная работа №31 обнаружение молочной кислоты в мышечной ткани
- •Лабораторная работа №32 количественное определение пировиноградной кислоты
- •Контрольные вопросы:
- •Раздел 5. Липиды и их обмен
- •Тема 12 структура и функции липидов
- •Лабораторная работа № 33 качественное определение липидов сыворотки крови
- •Лабораторная работа №34 сравнение ненасыщенности жиров
- •Лабораторная работа №35 обнаружение стеролов
- •Лабораторная работа №36 качественные реакции на холестерин
- •1. Реакция Либермана-Бурхарда.
- •2. Реакция Сальковского.
- •Контрольные вопросы:
- •Лабораторная работа №38 качественные реакции на желчные кислоты
- •Контрольные вопросы:
- •Раздел 6. Гормоны
- •Тема 14 регуляция обмена веществ. Гормоны
- •Лабораторная работа №39 качественные реакции на инсулин
- •Лабораторная работа №39 качественное определение адреналина
- •Контрольные вопросы:
- •Раздел 7. Энергетический обмен
- •Лабораторная работа №42 обнаружение над в дрожжах
- •Контрольные вопросы:
- •Список литературы
- •Содержание
Контрольные вопросы:
Объясните факторы устойчивости коллоидного раствора белка.
От чего зависит заряд белка в водном растворе?
Что такое изоэлектрическая точка белка? Какой заряд будут иметь водные растворы белка с избыточным количеством свободных карбоксильных групп?
Какой заряд будут иметь водные растворы белка с избыточным количеством аминогрупп? В какой среде будет ИЭТ такого белка?
Чем обусловлены реакции осаждения белков? При каких температурных условиях возможно осаждение белков?
Что такое обратимое и необратимое осаждение белков?
Что такое денатурация белка? Дайте характеристику денатурирующим агентам?
Что происходит с белковой молекулой при высаливании?
Тема 3 количественное определение белка. Оценка на основании фотометрии продуктов цветной реакции. Построение калибровочных графиков
Наиболее распространенным методом количественного определения белка является метод, основанный на биуретовой реакции, с последующей фотометрией цветных продуктов реакции. Биуретовая реакция открывает пептидную связь в белке.
Метод оценки количества вещества базируется на использовании калибровочного графика, а также концентрации стандартных проб, обрабатываемых параллельно с опытными в одинаковых с ними условиях.
Построение калибровочного графика:
1. Построение калибровочной кривой начинается с приготовления ряда разведений стандартного раствора исследуемого вещества. Стандартный раствор содержит вещество в известной концентрации. Разведения стандартного раствора должны охватывать диапазон физиологических концентраций и выходить за пределы их минимальных и максимальных величин.
(!) Например, при исследовании содержания белка в сыворотке крови концентрация стандартного вещества (альбумина) должна быть в интервале от 40 до 120 г/л (при физиологической концентрации общего белка 65-85 г/л).
Ряд калибровочных разведений получают путем разбавления основного стандартного раствора.
2. Затем ведут обработку стандартных растворов аналогично опытным пробам. Измеряют оптическую плотность калибровочных растворов и опытной пробы на одном и том же приборе. Измерения оптической плотности начинают со стандартного раствора наименьшей концентрации.
3. Усредненные (соответствующие отдельным концентрациям) значения оптической плотности - D (абсорбции - А, экстинкции - Е) наносят на миллиметровую (калибровочную) бумагу. На оси абсцисс (горизонтальной) с соблюдением одинаковых интервалов в равномерно возрастающей концентрации откладывают показатели содержания вещества в стандартном растворе; на оси ординат (вертикальной) - соответствующие им величины оптической плотности (рисунок 5).
Зависимость между концентрацией вещества в стандартных (калибровочных) пробах и оптической плотностью, соответствующей этим пробам, отражается линией, построенной по точкам. Строить калибровочный график следует не менее чем по пяти точкам.
Калибровочная кривая прокладывается таким образом, чтобы по возможности большее число точек (например, 3 из 5) лежало на линии, а остальные располагались близ нее, равномерно отклоняясь в ту и другую стороны. Отдельные точки, значительно смещающиеся от калибровочной кривой и обычно являющиеся результатом грубой ошибки в определении, исключаются из учета.
Расположение кривой определяют так, чтобы она исходила из нулевой отметки под углом ~45 ° к осям координат: при этом достигается наибольшая точность измерений. Последней способствует также выбор оптимального, достаточно крупного масштаба.
Определение количества вещества в опытной пробе с использованием калибровочного графика:
1. Определение оптической плотности раствора вещества с неизвестной концентрацией (опытной пробы). Исследование проводят против контроля, либо, если опытная проба слабоокрашенная, смотрят против дистиллированной воды.
2. Полученное значение откладывают на калибровочном графике путем опускания перпендикуляров: - с оси ординат на калибровочную кривую; - с кривой на ось абсцисс.
3. Полученное в результате значение концентрации на оси абсцисс и является искомой концентрацией.
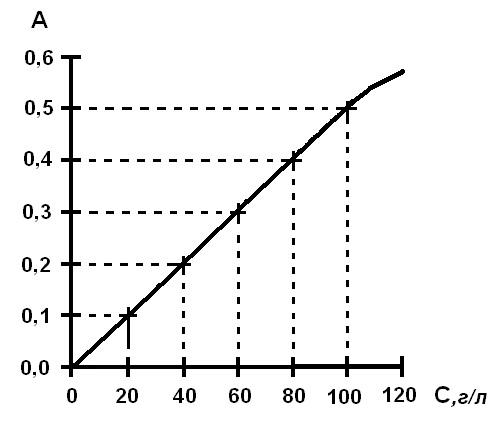
Рисунок 5. Схема построения калибровочного графика.
