
- •Глава 2. Молекулы
- •Механическая модель физической молекулы
- •Подходы к построению волновой функции
- •Вопросы для самоконтроля
- •2.1. Метод вс
- •2.1.1. Построение базисного набора
- •2.1.2. Описание молекулы водорода методом вс
- •Симметрия волновой функции
- •Энергетические характеристики молекулы водорода
- •Влияние межъядерного расстояния
- •2.1.3. Общая формулировка метода вс
- •2.1.4. Теория резонанса
- •Вопросы для самоконтроля
- •2.2. Метод мо
- •2.2.1. Молекулярные орбитали
- •Вопросы для самоконтроля
- •2.2.2. Описание молекулы водорода методом мо
- •Вычисление энергии в методе мо
- •Орбитальные энергии
- •Конфигурационное взаимодействие
- •2.2.3. Общая формулировка метода мо
- •Канонические мо
- •Локальные характеристики молекулы в методе кмо
- •Электронная плотность атомов
- •Порядок химической связи
- •Индекс свободной валентности
- •Молекулярные диаграммы
- •Поляризуемости
- •Вопросы для самоконтроля
- •2.2.4. Метод мо Хюккеля
- •Молекула этилена
- •Молекула циклобутадиена
- •Общие решения в методе Хюккеля
- •Молекулы с гетероатомами в методе мох
- •Система параметров Стрейтвизера
- •Вопросы для самоконтроля
- •2.2.5. Метод лмо
- •Гибридизация ао
- •Эффекты сопряжения
- •Индуктивные эффекты
- •Вопросы для самоконтроля
- •2.3. Ядерный остов молекул
- •Вопросы для самоконтроля
- •2.4. Спиновые состояния ядерного остова
- •Вопросы для самоконтроля
- •Рекомендуемая литература Основная
- •Дополнительная
- •Типовые задачи
Энергетические характеристики молекулы водорода
Располагая выражениями для волновых функций, можно вычислить энергию молекулы в каждом из трех возможных состояний по стандартной формуле: Е= Ф*НФdv. Для этого нужно знать явный вид оператора Гамильтона, который для молекулы водорода имеет вид:
Н = Нa + Hb + Hab
где НaиНb— операторы Гамильтона для отдельных атомов водорода, содержащих электроны № 1 и № 2, соответственно.
Нa = (–2/2m1)12 – e2/r1a и Нb = (–2/2m2)22 – e2/r2b
Оператор Нabсодержит члены, описывающие взаимодействие между атомами (энергии притяжения электронов к "чужим" ядрам (1aи2b), а также энергии межэлектронного и межъядерного отталкивания) и относится сразу к обоим атомам.
Нab = – e2/r1b – e2/r2а + е2/r12 + e2/rab
Рассмотрим для примера волновую функцию основного состояния
Ф = D1(АВ + ВА) + D2(AA + BB).
Вклад ионных РФ существенно меньше, чем ковалентных (D2 <<D1). Поэтому, в первом приближении, можно ограничиться учетом только ковалентных форм и взять приближенное выражение для волновой функции:
Ф D(АВ + ВА).
Вначале найдем величину коэффициента D. Это можно сделать из условия нормировки.
Ф*Ф dv = D 2 (AB + BA)*(AB + BA) dv = D2 [ (A*B* AB) dv +
+ (A*B* BA) dv + (B*A* AB) dv + (B*A* BA) dv ] = 1
В этом выражении имеется четыре интеграла. Рассмотрим первый из них. В подынтегральном выражении два сомножителя относятся к первому электрону, а два — ко второму. Такие интегралы можно представить в виде произведения более простых интегралов, каждый из которых включает только координаты только первого или только второго электрона. В результате шестимерный интеграл распадается на два трехмерных, каждый из которых представляет собой стандартное условие нормировки для атомных орбиталей. Поскольку атомные орбитали АиВнормированы, оба интеграла-сомножителя оказываются равными 1.
(A*B* AB) dv = [A*(1)A(1) B*(2)B(2) dv1 dv2 =
= A*(1)A(1) dv1 B*(2)B(2) dv2 = 1 1 = 1
Проанализируем второй интеграл:
(A*B* BA) dv = [A*(1)B(1) B*(2)A(2) dv1 dv2 =
= A*(1)B(1) dv1 B*(2)A(2) dv2 = s s = s 2
Трехмерные интегралы-сомножители (s) в этом выражении называютсяинтегралами перекрывания. Величина такого интеграла определяется величиной области перекрывания, в которой обе атомные орбитали (АиВ) заметно отличаются от нуля.

Очевидно, что s0, когда ядрааиbудаляются друг от друга, иs1, когда ядра сближаются.
Третий интеграл построен точно так же, как и второй, а четвертый — так же, как первый. В итоге выражение для нормировки приобретает вид:
Ф*Ф dv = D2 [ 1 + s 2 + s 2 + 1] = 1
Отсюда получаем для нормировочного множителя и волновой функции:
D = 1/(2 + 2s 2)1/2 и Ф (АВ + ВА)/(2 + 2s 2)1/2
Подставим это выражение в формулу для вычисления энергии:
Е = Ф*НФ dv = [1/(2 + 2s 2)] (АВ + ВА)*Н(АВ + ВА) dv
Раскрыв скобки в подынтегральном выражении, получим вместо одного сложного интеграла четыре более простых.
(АВ + ВА)*Н(АВ + ВА) dv = (АВ)*Н(АВ) dv + (АВ)*Н(ВА) dv +
+ (ВА)*Н(АВ) dv + (ВА)*Н(ВА) dv = I + II + III + IV
Проанализируем эти интегралы. Для начала можно отметить, что по структуре интегралы попарно равны друг другу: I=IVиII=III, и поэтому достаточно детально рассмотреть только два из них, напримерIиII.
Подставляя в интеграл Iвыражение для гамильтониана, получим сумму трех еще более простых интегралов:
(АВ)*Н(АВ) dv = (АВ)* (Нa + Hb + Hab) (АВ) dv =
= (АВ)*(Нa)(АВ) dv + (АВ)*(Нb)(АВ) dv + (АВ)*(Нab)(АВ) dv
Оператор Гамильтона в первом интеграле действует только на волновые функции типа А. Волновые функции типаВдля оператораНавыступают как простые числовые множители и их можно выносить за знак оператора. Это дает возможность разбить первый из трех интегралов в произведение двух трехмерных интегралов-сомножителей:
(АВ)*(На)(АВ) dv = В*B dvb А*(На)А dva
Первый сомножитель представляет собой условие нормировки для атомной орбитали Ви поэтому равен 1. Второй сомножитель представляет собой энергию, которую имеет электрон, принадлежащий атому водорода с ядрома(ЕНa) и находящийся в состоянииА. Второй интеграл построен аналогично первому и равен энергии, которую имеет электрон, принадлежащий атому водорода с ядромb(ЕНb) и находящийся в состоянииВ.
Наконец, третий интеграл содержит гамильтониан, описывающий оба электрона сразу. Поэтому этот интеграл нельзя разложить в произведение двух одноэлектронных и его нужно рассматривать как некоторую энергию, характеризующую взаимодействие двух атомов водорода. Эта энергия называется кулоновским интегралом(Jab), который можно представить и в более детальной записи:
(АВ)*(Нab)(АВ) dv = (АВ)*(– e2/r1b – e2/r2а + е2/r12 + e2/rab)(АВ) dv =
= (АВ)*(– e2/r1b)(АВ) dv + (АВ)*(– e2/r2а)(АВ) dv +
+ (АВ)*(е2/r12)(АВ) dv + (АВ)*(e2/rab)(АВ) dv =
= (В*B)dv2 A*(– e2/r1b)(А) dv1 + (A*A)dv1 B*(– e2/r1b)(B) dv2 +
+ (АВ)*(е2/r12)(АВ) dv + (e2/rab) (А*A)dv1 (B*В) dv2 =
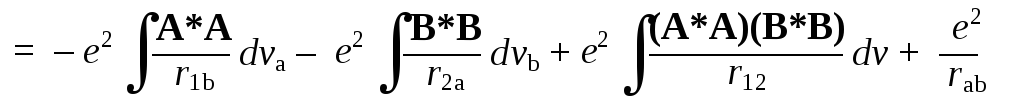
Произведение e(A*A)dvaпредставляет собой электрический зарядdqa, локализованный в малом объемеdva, принадлежащем атому На. Произведениеdqae/r1b, стоящее под знаком первого интеграла, — это потенциальная энергия взаимодействия заряженного объемаdvaэлектронного облака, созданного электроном № 1 с ядром атома Нb. Поэтому первый интеграл представляет собой полную энергию кулоновского притяжения электрона № 1, расположенного на орбиталиA, к ядруb; второй — энергию кулоновского притяжения электрона, расположенного на орбиталиB, к ядруa; третий — энергию кулоновского отталкивания двух электронных облаков, а четвертый — энергию кулоновского отталкивания двух ядер. Кулоновский интеграл, следовательно, отражает все электростатические взаимодействия между составными частями двух атомов, ядра которых сближены на расстояниеrab. Таким образом, для интегралаIполучаем следующую оценку:
I = ЕНa + ЕНb + Jab = 2EH + J
Перейдем к анализу интеграла II. Подставляя в этот интеграл выражение для гамильтониана, получим, как и в предыдущем случае, сумму трех простых интегралов:
(АВ)*Н(ВА) dv = (АВ)* (Нa + Hb + Hab) (ВА) dv =
= (АВ)*(Нa)(ВА) dv + (АВ)*(Нb)(ВА) dv + (АВ)*(Нab)(ВА) dv
Первый из этих интегралов может быть разложен в произведение двух одноэлектронных:
(АВ)*(Нa)(ВА) dv = В*А dvb А*(Нa)В dva
Первый сомножитель в этом выражении представляет собой интеграл перекрывания (s). Второй сомножитель можно преобразовать с учетом того, что гамильтониан являетсясамосопряженнымоператором, для которых выполняется правило:
А*НВ dv = В*Н*А dv
Атомная орбиталь А является собственной функцией для оператораНaи для нее выполняется соотношение:
НAА = НA*А = ЕНа А
Следовательно,
А*(Нa)В dva = В*Нa*А dva = В*ЕНаА dva =
= ЕНа В*А dv1a = ЕНа s
С учетом первого множителя получаем величину ЕНаs2. Второй интеграл устроен аналогично первому и поэтому равенЕНbs2.
Третий интеграл не поддается разложению на одноэлектронные сомножители и должен рассматриваться как характеристика межатомного взаимодействия. Этот интеграл называется обменным(Kab). Его, как и кулоновский, можно представить в более детальной записи:
(АВ)*(Нab)(ВA) dv = (АВ)*(– e2/r1b – e2/r2а + е2/r12 + e2/rab)(ВA) dv =
= (АВ)*(– e2/r1b)(ВA) dv + (АВ)*(– e2/r2а)(ВA) dv +
+ (АВ)*(е2/r12)(ВA) dv + (АВ)*(e2/rab)(ВA) dv =
= (В*A)dv2 A*(– e2/r1b)(B) dv1 + (A*B)dv1 B*(– e2/r1b)(A) dv2 +
+ (АВ)*(е2/r12)(ВA) dv + (e2/rab) (А*B)dv1 (B*A) dv2 =

Из формы интегралов в этом выражении видно, что они представляют собой особые кулоновские поправки к полной энергии молекулы. Они возникают вследствие того, что в области перекрывания плотность электронного облака молекулы не равна сумме плотностей двух исходных атомных электронных облаков. К этой сумме добавляется интерференционный вклад. Другими словами, в области перекрывания возникают два дополнительных электрических заряда (от каждого электрона), равные es(A*B)dv1, которые взаимодействуют и с ядрами молекулы, и между собой.
Можно сказать, что кулоновский интеграл ( J ) вычисляется в предположении, что сферически симметричная форма электронных облаков атомов (АиВ) при их вхождении в состав молекулы не изменилась. В действительности (вследствие интерференции в области перекрывания) оба эти облака деформированы:АА'иBB'. В результате энергия межатомных кулоновских взаимодействий оказалась вычисленной неправильно. Обменный интеграл представляет собой необходимую поправку.
В итоге получаем следующую оценку интеграла II:
II = ЕНа s2 + ЕНb s2 + K = 2 EH s2 + K
Теперь, с учетом равенств I=IVиII=III, запишем полное выражение для энергии молекулы:
Eg = (I + II + III + IV)/(2 + 2s2) = (2 EH + J + 2 EH s2 + K +
+ 2 EH s2 + K + 2 EH + J )/(2 + 2s2) =
= [4EH (1 + s2) + 2 (J + K)]/2(1 + s2) = 2 EH + (J + K)/(1 + s2)
Таким образом, энергия молекулы водорода представлена в виде суммы двух вкладов: 1) энергии двух атомов, из которых молекула образовалась, и 2) поправки на энергию межатомных взаимодействий. Из формулы видно, что эта поправка состоит из двух частей — кулоновскойиобменной. Их величины можно вычислить, зная явный вид орбиталейАиВ.
Следует подчеркнуть, что найденное выражение для энергии носит общий характер в методе ВС. Независимо от размера молекулы, энергия всегда представляется в виде суммы энергий изолированных атомов, из которых молекула образована, и поправок (кулоновских и обменных) на межатомные взаимодействия.
Аналогичные вычисления можно выполнить и для других состояний. Например, для триплетного возбужденного состояния с волновой функцией Фuполучим:
Eu = 2 EH + (J – K)/(1 – s2)
Нужно иметь в виду, что значение кулоновского интеграла положительно, а обменного — отрицательно. Поэтому энергия триплетного состояния выше, чем основного (Eu>Eg).
