
- •Глава 2. Молекулы
- •Механическая модель физической молекулы
- •Подходы к построению волновой функции
- •Вопросы для самоконтроля
- •2.1. Метод вс
- •2.1.1. Построение базисного набора
- •2.1.2. Описание молекулы водорода методом вс
- •Симметрия волновой функции
- •Энергетические характеристики молекулы водорода
- •Влияние межъядерного расстояния
- •2.1.3. Общая формулировка метода вс
- •2.1.4. Теория резонанса
- •Вопросы для самоконтроля
- •2.2. Метод мо
- •2.2.1. Молекулярные орбитали
- •Вопросы для самоконтроля
- •2.2.2. Описание молекулы водорода методом мо
- •Вычисление энергии в методе мо
- •Орбитальные энергии
- •Конфигурационное взаимодействие
- •2.2.3. Общая формулировка метода мо
- •Канонические мо
- •Локальные характеристики молекулы в методе кмо
- •Электронная плотность атомов
- •Порядок химической связи
- •Индекс свободной валентности
- •Молекулярные диаграммы
- •Поляризуемости
- •Вопросы для самоконтроля
- •2.2.4. Метод мо Хюккеля
- •Молекула этилена
- •Молекула циклобутадиена
- •Общие решения в методе Хюккеля
- •Молекулы с гетероатомами в методе мох
- •Система параметров Стрейтвизера
- •Вопросы для самоконтроля
- •2.2.5. Метод лмо
- •Гибридизация ао
- •Эффекты сопряжения
- •Индуктивные эффекты
- •Вопросы для самоконтроля
- •2.3. Ядерный остов молекул
- •Вопросы для самоконтроля
- •2.4. Спиновые состояния ядерного остова
- •Вопросы для самоконтроля
- •Рекомендуемая литература Основная
- •Дополнительная
- •Типовые задачи
Вопросы для самоконтроля
1. Дайте определение понятий "конфигурация" и "конфигурационное пространство". Определите размерность КП для некоторых простых молекул (ацетилен, метан, аммиак).
2. Почему полная энергия молекулы зависит от ее пространственной конфигурации. Что такое "поверхность потенциальной энергии"? Можно ли ППЭ изобразить графически?
3. Что такое "энергетический профиль"? Сколько таких профилей нужно построить для получения достаточно полного представления о виде ППЭ?
4. Какие характеристики молекулы можно найти, используя ее ППЭ?
5. Что представляет собой "топологический граф" молекулы? Как построить этот граф на основе ППЭ?
6. Что представляет собой "химическая форма"? Сколько химических форм может быть у молекулы? Чему соответствуют переходы от одной химической формы к другой?
7. Какие характеристики химического превращения можно извлечь из энергетического профиля элементарного акта?
8. Каким образом молекулы преодолевают энергетический барьер, разделяющий две химические формы? Откуда берется необходимая для этого энергия?
2.4. Спиновые состояния ядерного остова
В ряде случаев при описании строения молекул полезно учитывать тот факт, что многие атомные ядра имеют спиновой моментS. Каждый такой вектор характеризуется постоянным модулем |S| и набором допустимых ориентаций в пространстве. Величину модуля удобно выражать через спиновое квантовое числоS, а ориентации — через проекции вектора спина на некоторую ось (z), причем каждой такой проекции соответствует значение магнитного спинового числаMS.

Например, молекула водорода содержит два ядра. Каждое из них имеет спин, модуль которого задается спиновым числом S= 1/2. Каждый из этих векторов спина может находиться в одном из двух состояний:
состояние :S= 1/2;MS. = +1/2
состояние : S= 1/2;MS. = –1/2
Следовательно, ядерный остов молекулы водорода можно обнаружить в одном из четырех возможных состояний: ,,,. Если молекула изолирована от окружающей среды, то спиновая ядерная конфигурация практически не влияет на ее энергию и свойства. Если, однако, наложить на молекулу внешнее магнитное поле, то энергия молекулы будет существенно зависеть от ориентации ядерных спинов относительно внешнего поля. Причиной такой зависимости является то обстоятельство, что с каждым спиновым моментом ядра всегда связан магнитный момент. Взаимодействие каждого магнитного момента с магнитным полем, имеющим напряженностьН, приводит к изменению энергии на величинуЕ= –Н(при ориентации вектора "по полю") иЕ= +Н(при ориентации вектора "против поля").
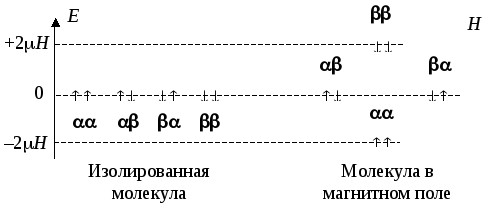
Расщепление единого энергетического уровня на подуровни приводит к возможности квантовых переходов при действии электромагнитного излучения. Эти переходы лежат в радиочастотной области спектра. Их исследование составляет содержание важного экспериментального метода изучения молекул — спектроскопии ЯМР(ядерного магнитного резонанса). Высокая эффективность ЯМР-спектроскопии обусловлена тем, что вид спектра очень чувствителен к особенностям химического строения молекулы, таким как распределение электронной плотности в окрестностях ядер, расстояния между ядрами и др. Для иллюстрации рассмотрим две изомерные молекулы: диметиловый эфир Н3С–О–СН3и этанол СН3–СН2–О–Н. Обе молекулы содержат по шесть протонов. В молекуле диметилового эфира все протоны химически эквивалентны (т.е. имеют одинаковое окружение). В молекуле этанола имеются три типа протонов, имеющих разное окружение. В результате разного строения молекул ЯМР-спектры диметилового эфира и этанола оказываются принципиально различными. Первый содержит один пик, а второй — три, причем их площади соотносятся как 3:2:1, в соответствии с числами протонов в составе метильной группы (СН3–), метиленовой группы (–СН2–) и гидроксильной группы (–ОН).
В общем случае число ядерных спиновых состояний может быть очень велико. Его можно выразить формулой-произведением:
N = (2S1 + 1)(2S2 +1) … (2Sn + 1)
где Si— спиновое числоi-го ядра. Соответственно, ЯМР-спектры многоядерных молекул весьма сложны. Тем не менее, они поддаются расшифровке, и из них можно извлечь важные сведения о строении молекулы. Во многих случаях ЯМР-спектроскопия является единственным методом, позволяющим добывать необходимую структурную информацию.
