
- •Глава 2. Молекулы
- •Механическая модель физической молекулы
- •Подходы к построению волновой функции
- •Вопросы для самоконтроля
- •2.1. Метод вс
- •2.1.1. Построение базисного набора
- •2.1.2. Описание молекулы водорода методом вс
- •Симметрия волновой функции
- •Энергетические характеристики молекулы водорода
- •Влияние межъядерного расстояния
- •2.1.3. Общая формулировка метода вс
- •2.1.4. Теория резонанса
- •Вопросы для самоконтроля
- •2.2. Метод мо
- •2.2.1. Молекулярные орбитали
- •Вопросы для самоконтроля
- •2.2.2. Описание молекулы водорода методом мо
- •Вычисление энергии в методе мо
- •Орбитальные энергии
- •Конфигурационное взаимодействие
- •2.2.3. Общая формулировка метода мо
- •Канонические мо
- •Локальные характеристики молекулы в методе кмо
- •Электронная плотность атомов
- •Порядок химической связи
- •Индекс свободной валентности
- •Молекулярные диаграммы
- •Поляризуемости
- •Вопросы для самоконтроля
- •2.2.4. Метод мо Хюккеля
- •Молекула этилена
- •Молекула циклобутадиена
- •Общие решения в методе Хюккеля
- •Молекулы с гетероатомами в методе мох
- •Система параметров Стрейтвизера
- •Вопросы для самоконтроля
- •2.2.5. Метод лмо
- •Гибридизация ао
- •Эффекты сопряжения
- •Индуктивные эффекты
- •Вопросы для самоконтроля
- •2.3. Ядерный остов молекул
- •Вопросы для самоконтроля
- •2.4. Спиновые состояния ядерного остова
- •Вопросы для самоконтроля
- •Рекомендуемая литература Основная
- •Дополнительная
- •Типовые задачи
Орбитальные энергии
В методе МО важное значение имеют орбитальные энергии (), каждая из которых равна энергии единственного электрона, образующего стационарное облако определенной формы (типаG,Uи др.), распределенное вокруг всего ядерного остова молекулы.
Орбитальные энергии можно легко вычислить, зная явный вид МО. Например, для четной орбитали типа G=СG (А+В) получим:
G = (CG)2 G(1)*(Н1)G(1) dv1 = (CG)2 (A + B)1*(Н1)(A + B)1 dv1 =
= (CG)2 A1*Н1A1dv1 + A1*Н1B1dv1 + B1*Н1A1dv1 + B1*Н1B1dv1 =
= (CG)2 ( + + + )
Аналогично, для нечетной орбитали Uполучим:U= (CU)2 (––+).
С учетом явного вида нормировочных множителей:

С помощью приведенных выражений орбитальная энергия электрона представляется в виде суммы более простых вкладов — (остовныйинтеграл) и(резонансныйинтеграл).
Остовный интеграл представляет собой энергию электрона, движение которого искусственно ограничено пределами одного атома. Ясно, что в таких условиях движение электрона описывается некоторой орбиталью атомного типа, и он образует одноцентровое электронное облако, которое, однако, находится под кулоновским влиянием всех ядер молекулы:
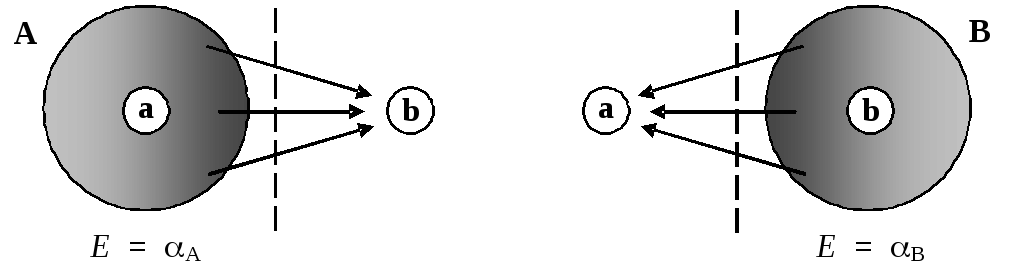
Для молекулы водорода оба остовных интеграла равны друг другу из-за симметрии молекулы (A=B). В случае несимметричных молекул разным атомам соответствуют и разные по величине остовные интегралы. Таким образом, остовные интегралы характеризуют химическую природу тех атомов, из которых построена молекула. Именно поэтому они особенно важны для решения химических задач.
Резонансные интегралы (), в отличие от остовных, являются двухцентровыми. Другими словами, каждый такой интеграл характеризует определенную пару атомов. Из вычислительной формулы:
AB = A* Н1B dv1 = A | Н1 | B
следует, что величина этого интеграла пропорциональна амплитуде вероятности некоторого события — того, что электрон из состояния Bс энергиейB перейдет в аналогичное состояниеАс энергиейА. Обратный переход характеризуется точно такой же амплитудой вероятности. ПоэтомуAB=BА, и нет необходимости вычислять два разных интеграладля заданной пары атомов (это верно даже в случае разных по природе атомов).
Резонансный интеграл имеет размерность энергии и представляет собой энергетическую поправку, смысл которой заключается в том, что электрон, способный переходить от одного атома к другому, обладает большей свободой и меньшей энергией, чем электрон, локализованный в пределах одного из атомов (подобно тому, как энергия частицы, запертой в потенциальном ящике, уменьшается при увеличении размера ящика). Это означает, что все резонансные интегралы имеют отрицательные значения: < 0.
Резонансные интегралы можно считать мерой интенсивности взаимодействий между одноядерными фрагментами молекулы (т.е., говоря химически языком, химических связей между атомами).
Располагая выражениями для орбитальных энергий, можно построить еще одну энергетическую диаграмму, которая обычно называется корреляционной(КД). Фактически КД представляет собой две энергетические диаграммы — атомную и молекулярную с общей шкалой энергии. Первая показывает доступные состояния для электрона в исходных атомах, а вторая — возможные состояния того же электрона, но уже в молекуле. Для молекулы водорода КД имеет следующий вид:

С помощью КД можно проследить изменения в полной энергии системы, которыми сопровождается образование молекулы из атомов или обратный процесс — ее диссоциация на атомы. При образовании молекулы электроны с атомных орбиталей переходят на молекулярные, что сопровождается уменьшением полной энергии. При разрушении молекулы электроны локализуются на атомных орбиталях, что сопровождается увеличением полной энергии. Очевидно, что увеличение энергии системы возможно только за счет внешних источников. Поэтому можно утверждать, что разрушение молекул — процесс всегда вынужденный, сопряженный с необходимостью затраты определенной порции энергии (энергии химической связи), величину которой можно легко вычислить из КД. Другими словами, с помощью КД можно описывать не только сами молекулы, но и их химические превращения (реакции). Например, реакции рекомбинации атомов водорода Н+Н=Н2будет соответствовать КД:
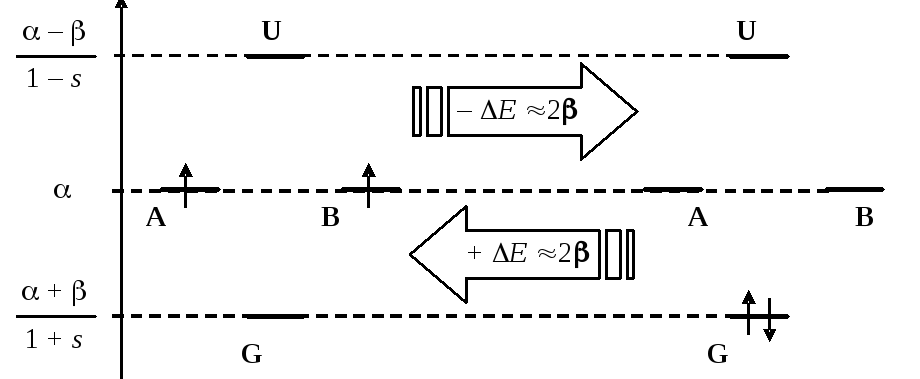
Левая часть диаграммы соответствует состоянию системы в виде двух отдельных атомов водорода (Н+Н), при этом оба электрона движутся по атомному типу (атомные орбиталиАиВ) и имеют энергию. Правая часть соответствует состоянию системы в виде устойчивой молекулы (Н2). Оба электрона движутся по молекулярному типу (молекулярные спин-орбиталиGиG) и имеют энергии+(т.к.s<< 1). Следовательно, прочность химической связи в молекуле водорода можно считать приблизительно равной удвоенному значению резонансного интеграла (Е2).
После вычисления электронной энергии молекулы по описанной выше методике, к ней добавляют энергию отталкивания ядер:
Eполн = Eэл + e2/rab
Полученная в результате полная энергия молекулы зависит от межъядерного расстояния примерно так же, как и в методе ВС:

Располагая такой зависимостью, можно оценить равновесное расстояние между ядрами r* (длину химической связи) и энергию образования молекулы из атомов (т.е. прочность химической связи).
