
- •Глава 2. Молекулы
- •Механическая модель физической молекулы
- •Подходы к построению волновой функции
- •Вопросы для самоконтроля
- •2.1. Метод вс
- •2.1.1. Построение базисного набора
- •2.1.2. Описание молекулы водорода методом вс
- •Симметрия волновой функции
- •Энергетические характеристики молекулы водорода
- •Влияние межъядерного расстояния
- •2.1.3. Общая формулировка метода вс
- •2.1.4. Теория резонанса
- •Вопросы для самоконтроля
- •2.2. Метод мо
- •2.2.1. Молекулярные орбитали
- •Вопросы для самоконтроля
- •2.2.2. Описание молекулы водорода методом мо
- •Вычисление энергии в методе мо
- •Орбитальные энергии
- •Конфигурационное взаимодействие
- •2.2.3. Общая формулировка метода мо
- •Канонические мо
- •Локальные характеристики молекулы в методе кмо
- •Электронная плотность атомов
- •Порядок химической связи
- •Индекс свободной валентности
- •Молекулярные диаграммы
- •Поляризуемости
- •Вопросы для самоконтроля
- •2.2.4. Метод мо Хюккеля
- •Молекула этилена
- •Молекула циклобутадиена
- •Общие решения в методе Хюккеля
- •Молекулы с гетероатомами в методе мох
- •Система параметров Стрейтвизера
- •Вопросы для самоконтроля
- •2.2.5. Метод лмо
- •Гибридизация ао
- •Эффекты сопряжения
- •Индуктивные эффекты
- •Вопросы для самоконтроля
- •2.3. Ядерный остов молекул
- •Вопросы для самоконтроля
- •2.4. Спиновые состояния ядерного остова
- •Вопросы для самоконтроля
- •Рекомендуемая литература Основная
- •Дополнительная
- •Типовые задачи
Вопросы для самоконтроля
1. Опишите процедуру построения волновой функции молекулы методом МО, укажите основные стадии этой процедуры.
2. Дайте определение понятиям "молекулярная орбиталь" и "молекулярная спин-орбиталь". В чем различие между ними? Чем молекулярные орбитали отличаются от атомных? Какие молекулярные орбитали называются "каноническими"?
3. Почему атомные орбитали можно использовать в качестве базиса для анализа молекулярных орбиталей?
4. В чем содержание требования ортонормированности МО?
5. Какие условия накладывает на вид МО наличие у молекулы определенной пространственной симметрии?
2.2.2. Описание молекулы водорода методом мо
Для иллюстрации метода МО полезно рассмотреть его применение для описания молекулы водорода. В случае двухядерной молекулы Н2атомный базис состоит всего из двух АО, которые обозначим, как и в методе ВС, буквамиAиB. Тогда любая МО должна выражаться линейной комбинацией типа:
= CA A + CB B
Учет пространственной симметрии молекулы приводит к условию: |CA|2= |CB|2, которое выполняется в двух случаях:
CA= +CBиCA= –CB
Следовательно, можно построить всего две МО — одну четную (G) и одну нечетную (U):G=Cg(A+B) иU=Cu(A–B). Их нормировочные множители можно найти стандартным путем (см. раздел 2.1.2.). Они равны:
Cg = 1/(2 + 2s)1/2 и Cu = 1/(2 – 2s)1/2
Дополнив полученные МО спиновыми множителями или, получим четыре вариантамолекулярных спин-орбиталей(МСО):G,G,U,U.
При сближении атомов водорода их электроны, движущиеся в соответствии с атомными типами АиВ, вынуждены перейти к молекулярным типам движения, в качестве которых и выступают найденные четыре МСО. Поскольку электронов в молекуле Н2всего два, заселены будут только две из четырех МСО. Следовательно, существует несколько вариантов состояния молекулы, а именно — шесть.
|
Номер состояния |
1 |
2 |
3 |
4 |
5 |
6 |
|
состояние электрона № 1 |
G |
G |
G |
G |
G |
U |
|
состояние электрона № 2 |
G |
U |
U |
U |
U |
U |
Для каждого варианта можно построить глобальную волновую функцию в виде определителя Слэтера. Например, для первого варианта волновая функция будет иметь вид (без учета нормировочного множителя):
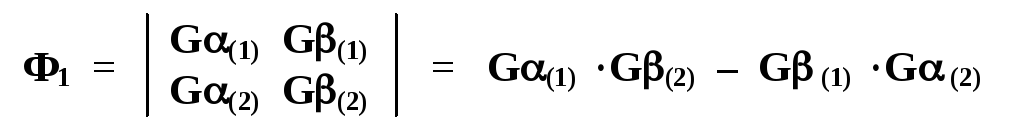
Запишем вид остальных функций, придерживаясь стандартного соглашения (первый сомножитель относится к электрону № 1, второй — к электрону № 2 и т.д.).
|
1 |
2 |
Глобальная волновая функция |
|
G |
G |
Ф1 = G G – G G = [GG]( – ) |
|
G |
U |
Ф2 = G U – U G = [GU – UG]() |
|
G |
U |
Ф3 = G U – U G |
|
G |
U |
Ф4 = G U – U G |
|
G |
U |
Ф5 = G U – U G = [GU – UG]( ) |
|
U |
U |
Ф6 = U U – U U = [UU]( – ) |
Все эти волновые функции обладают нужной для выполнения принципа Паули перестановочной антисимметричностью, поскольку построены в виде определителя Слэтера. Глобальные волновые функции, однако, должны кроме этого, обладать и подходящей пространственной симметрией, например, быть либо четными, либо нечетными. Для проверки этой характеристики, необходимо отделить пространственные части от спиновых и подействовать на пространственные части оператором инверсии.
Из таблицы видно, что функции Ф3иФ4не разделены на пространственный и спиновой сомножители. Поэтому для них невозможно определить тип пространственной симметрии. Обойти эту трудность можно посредством известного приема — симметризации — заменить "неправильные" функцииФ3иФ4на их сумму и разность, обладающие симметрией:
Ф'3=Ф3+Ф4 = [GU–UG](+)
Ф'4=Ф3+Ф4 = [GU+UG](–)
Теперь можно установить пространственную симметрию всех глобальных волновых функций:
|
Ф |
Пространственный множитель |
Тип симметрии |
Спиновой множитель |
S |
MS |
|
Ф1 |
GG |
четный (g) |
– |
0 |
0 |
|
Ф2 |
GU – UG |
нечетный (u) |
|
1 |
+1 |
|
Ф'3 |
GU – UG |
нечетный (u) |
+ |
1 |
0 |
|
Ф'4 |
GU + UG |
нечетный (u) |
– |
0 |
0 |
|
Ф5 |
GU – UG |
нечетный (u) |
|
1 |
–1 |
|
Ф6 |
UU |
четный (g) |
– |
0 |
0 |
Видно, что волновые функции Ф2,Ф'3иФ5образуют триплет: их пространственные множители одинаковы, а спиновые состояния отличаются ориентацией вектора глобального спина молекулы.
Фu= (1/2)0,5(GU–UG)[C1() +C2(+) +C3()]
